人教版(2019)選擇性必修1《第2章 化學反應速率與化學平衡》2023年單元測試卷
發布:2024/8/16 12:0:1
一、選擇題
-
1.下列說法正確的是( )
A.放熱反應一定是自發反應 B.熵增的反應不一定是自發反應 C.固體溶解一定是熵減小的過程 D.非自發反應在任何條件下都不能發生 組卷:312引用:13難度:0.8 -
2.NH3和純凈的O2在一定條件下發生反應:4NH3(g)+3O2(g)?2N2(g)+6H2O(g),現向一容積不變的2L密閉容器中充入4mol NH3和3mol O2,4min后,測得生成的H2O占混合氣體體積的40%,則下列表示此段時間內該反應的平均速率不正確的是( )
A.v(O2)=0.225 mol?L-1min-1 B.v(H2O)=0.375 mol?L-1min-1 C.v(N2)=0.125 mol?L-1min-1 D.v(NH3)=0.250 mol?L-1min-1 組卷:143引用:10難度:0.7 -
3.t℃時,某一氣態平衡體系中含有X(g)、Y(g)、Z(g)、W(g)四種物質,此溫度下發生反應的平衡常數表達式為:K=
,有關該平衡體系的說法正確的是( )c(X)?c2(Y)c2(Z)?c2(W)A.升高溫度,平衡常數K增大 B.增大壓強,W(g)質量分數增加 C.升高溫度,若混合氣體的平均相對分子質量變小,則正反應是放熱反應 D.增大X(g)濃度,平衡向正反應方向移動 組卷:55引用:7難度:0.7 -
4.下列有關說法正確的是( )
A.△H>0、△S<0的反應在任何條件下都能自發進行 B.對于二氧化硫的催化氧化反應(△H<0),反應溫度越低越好 C.合成氨生產中,為提高氫氣的轉化率,可增加氮氣的量 D.使用催化劑可以提高工業生產中合成氨的產率 組卷:38引用:3難度:0.8 -
5.硝酸生產中,500℃時,NH3和O2可能發生如下反應:
①4NH3 (g)+5O2 (g)?4NO (g)+6H2O (g)△H=-9072kJ?mol-1 K=1.1×1026
②4NH3 (g)+4O2 (g)?2N2O (g)+6H2O (g)△H=-1104.9kJ?mol-1 K=4.4×1028
③4NH3 (g)+3O2 (g)?2N2 (g)+6H2O (g)△H=-1269.02kJ?mol-1 K=7.1×1034
其中,②、③是副反應.若要減少副反應,提高單位時間內NO的產率,最合理的措施是( )A.增大O2濃度 B.使用合適的催化劑 C.減小壓強 D.降低溫度 組卷:160引用:7難度:0.7 -
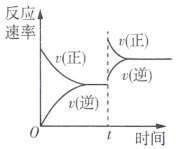 6.一定條件下在一恒容密閉容器中發生反應:N2(g)+3H2(g)?2NH3(g)△H<0,反應速率隨時間的變化情況如圖所示,t時僅改變某一條件,該條件可能是( )
6.一定條件下在一恒容密閉容器中發生反應:N2(g)+3H2(g)?2NH3(g)△H<0,反應速率隨時間的變化情況如圖所示,t時僅改變某一條件,該條件可能是( )A.加入適當催化劑 B.升高溫度 C.增大反應物的濃度 D.增大壓強 組卷:44引用:3難度:0.5
三、解答題
-
19.氮氧化物NOx(主要指NO和NO2)會形成酸雨、光化學煙霧,破壞臭氧層,是大氣主要污染物之一,有效去除大氣中的NOx是環境保護的重要課題。
(1)研究氮氧化物與懸浮在大氣中海鹽粒子的相互作用時,涉及如下反應:
2NO2(g)+NaCl(s)?NaNO3(s)+ClNO(g) K1△H1<0 (Ⅰ)
2NO(g)+Cl2(g)?2ClNO(g) K2△H2<0 (Ⅱ)
①4NO2(g)+2NaCl(s)?2NaNO3(s)+2NO(g)+Cl2(g)的平衡常數K=(用K1、K2表示)。
②為研究不同條件對反應(Ⅱ)的影響,在恒溫條件下,向2 L恒容密閉容器中加入0.2 mol NO和0.1 mol Cl2,10 min時反應(Ⅱ)達到平衡。測得10 min內v(ClNO)=7.5×10-3mol?L-1?min-1,則平衡后NO的轉化率α1=。其他條件保持不變,反應(Ⅱ)在恒壓條件下進行,平衡時NO的轉化率α2α1(填“>”“<”或“=”),平衡常數K2(填“增大”“減小”或“不變”)。
(2)NO能與N2O反應生成N2和NO2,反應的能量變化如圖所示,若生成1 mol N2,其△H=kJ?mol-1。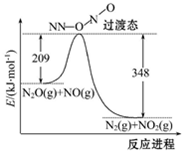
(3)NH3催化還原氮氧化物(SCR)技術是目前應用最廣泛的煙氣氮氧化物脫除技術。反應原理如圖甲所示。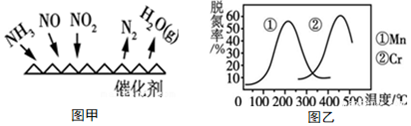
由圖甲可知,SCR技術中的氧化劑為。當NO2與NO的物質的量之比為1:1時,與足量氨氣在一定條件下發生脫氮反應。該反應的化學方程式為。
②圖乙是不同催化劑Mn和Cr在不同溫度下對應的脫氮率,由圖可知工業選取的最佳催化劑為。
(4)利用電化學裝置可消除氮氧化物污染,變廢為寶。圖丙裝置實現的能量轉化形式是。圖丁為電解NO制備NH4NO3的裝置,該裝置中陽極的電極反應式為。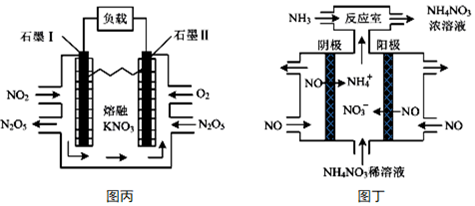 組卷:36引用:3難度:0.5
組卷:36引用:3難度:0.5 -
20.李克強總理在(2018年國務院政府工作報告》中強調“今年二氧化硫、氮氧化物排放量要下降3%.研究煙氣的脫硝(除NOx)脫硫(除SO2)有著積極的環保意義
Ⅰ.汽車排氣管上安裝“催化轉化器”,其反應的熱化學方程式為2NO(g)+2CO(g)?2CO2(g)+N2(g)△H=-746.50kJ/mol
T℃時,將等物質的量的NO和CO充入容積為2L的密閉容器中若溫度和體積不變,反應過程中NO的物質的量隨時間的變化關系如圖所示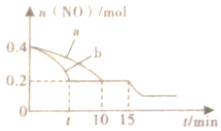
(1)圖中a、b分別表示在相同溫度下,使用質量相同但表面積不同的催化劑時,達到平衡過程中a(NO)的變化曲線,其中表示催化劑表面積較大的曲線是(填“a”或“b”)。
(2)在a曲線所示反應中,0-10min內,v(CO)=mol/(L?min);T℃時,該反應的化學平衡常數K=
(3)15min時,n(NO)發生圖中所示變化,則改變的條件可能是(填字母)。
A.充入入少量COB.將N2液化移出體系C升高溫度D.加入催化劑
Ⅱ.已知下列反應:①5O2(g)+4NH3(g)=6H2O(g)+4NO(g)△H1
②N2(g)+O2(g)=2NO(g)△H2
③2NO(g)+O2(g)=2NO2(g)△H3
(1)在高效催化劑作用下可發生反應8NH3(g)+6NO2(g)7N2(g)+12H2O(g),利用該反應對NO2進行處理則該反應的△H=催化劑(用△H1、△H2、△H3表示)
(2)某溫度下,向某恒容密閉容器中充入一定量的NH3和NO2,按照(1)的原理模擬污染物的處理。若容器中觀察到(填字母),可判斷該反應達到平衡狀態
A.混合氣體顏色不再改變
B.混合氣體的密度不再改變
C.混合氣體摩爾質量不再改變
D.NH3和NO2的物質的量之比為4:3
(3)將一定比例的O2、NH3和NO2的混合氣體,勻速通入圖(a)所示裝有催化劑的反應器中充分進行反應。反應相同時間NOx,的去除率隨反應溫度的變化曲線如圖(b)所示。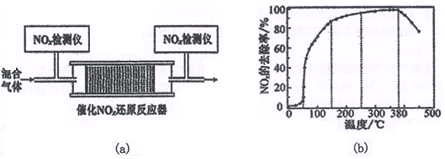
在50~250℃范圍內隨著溫度的升高,NOx的去除率先迅速上升后上升緩慢,其中去除率迅速上升段的主要原因是組卷:25引用:2難度:0.5


