2022-2023學(xué)年寧夏吳忠三中九年級(下)期中化學(xué)試卷
發(fā)布:2024/7/10 8:0:8
一、選擇(本題共11小題,每小題2分,共22分。)
-
1.下列各圖所示變化中,屬于物理變化的是( )
A. 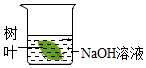
制作葉脈書簽B. 
鉆木取火C. 
比較硬度D. 
酸雨的腐蝕組卷:273引用:11難度:0.5 -
2.下列物質(zhì)的化學(xué)式,俗名及所屬類別的對應(yīng)關(guān)系正確的是( )
A.NaOH 燒堿 鹽 B.CO2固體 干冰 氧化物 C.NaHCO3 小蘇打 酸 D.Hg 水銀 非金屬 組卷:52引用:12難度:0.9 -
3.學(xué)習(xí)化學(xué)過程中需要經(jīng)常做實(shí)驗(yàn)。下列實(shí)驗(yàn)操作正確的是( )
A. 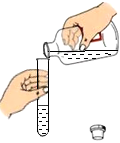
傾倒液體B. 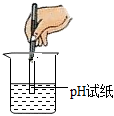
測溶液pHC. 
過濾D. 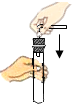
塞緊橡膠塞組卷:9引用:2難度:0.7 -
4.物質(zhì)的性質(zhì)決定用途,下列說法錯誤的是( )
A.焦炭具有還原性,用于冶煉金屬 B.氫氧化鈉具有堿性,可以使用改良酸性土壤 C.常溫下氮?dú)饣瘜W(xué)性質(zhì)穩(wěn)定,可以作保護(hù)氣 D.鎂能在空氣中燃燒發(fā)出耀眼的白光,可用于制造照明彈 組卷:1引用:2難度:0.5 -
5.下列實(shí)驗(yàn)現(xiàn)象描述錯誤的是( )
A.鐵絲在氧氣中劇烈燃燒、火星四射、生成黑色固體四氧化三鐵 B.鐵釘放入硫酸銅溶液中,鐵釘表面析出一層紫紅色物質(zhì),溶液由藍(lán)色逐漸變?yōu)闇\綠色 C.二氧化碳通入紫色石蕊溶液,紫色石蕊溶液變紅 D.碳還原氧化銅時,黑色粉末中出現(xiàn)紅色物質(zhì) 組卷:36引用:2難度:0.6 -
6.如圖是某化學(xué)反應(yīng)的微觀模型示意圖,據(jù)此分析錯誤的是( )

A.示意圖中的各物質(zhì)均屬于化合物 B.反應(yīng)的本質(zhì)是原子的重新組合過程 C.元素的種類沒有發(fā)生變化 D.反應(yīng)前后原子數(shù)目沒有變化 組卷:26引用:2難度:0.5
四、實(shí)驗(yàn)探究(共16分)(除化學(xué)方程式每空2分外,其余每空1分)
-
17.在探究鐵、銅、鋅、銀的金屬活動性順序時,某小組做了如下三個實(shí)驗(yàn):(所用金屬均已打磨,形狀與大小和稀鹽酸的用量均相同)
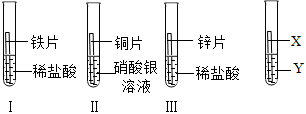
(1)實(shí)驗(yàn)Ⅰ現(xiàn)象是。
(2)一段時間后,可觀察到實(shí)驗(yàn)Ⅱ現(xiàn)象是銅表面有銀白色金屬出現(xiàn),溶液變藍(lán)色,反應(yīng)的化學(xué)方程式是。
(3)乙和丙兩位同學(xué)認(rèn)為上述三個實(shí)驗(yàn)不能夠得出四種金屬活動性順序,原因是沒有驗(yàn)證鐵與銅的活動性強(qiáng)弱;并在上述實(shí)驗(yàn)的基礎(chǔ)上,補(bǔ)充了一個實(shí)驗(yàn)(如圖所示),實(shí)現(xiàn)了探究目的。他們的實(shí)驗(yàn):X是金屬,Y是溶液。組卷:90引用:2難度:0.5 -
18.某化學(xué)興趣小組的同學(xué)分兩組對CO2和NaOH的反應(yīng)進(jìn)行探究。
提出問題:怎樣證明氫氧化鈉溶液和二氧化碳發(fā)生了反應(yīng)?
(1)實(shí)驗(yàn)設(shè)計:同學(xué)們寫出該反應(yīng)的化學(xué)方程式:。
并根據(jù)反應(yīng)原理進(jìn)行實(shí)驗(yàn)
第一組的同學(xué)設(shè)計了如圖所示的A、B兩實(shí)驗(yàn),實(shí)驗(yàn)現(xiàn)象為A中試管內(nèi)液面上升;B中氣球鼓起。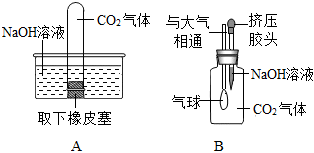
(2)第一組同學(xué)認(rèn)為自己的實(shí)驗(yàn)方案可以證明NaOH和CO2發(fā)生了化學(xué)反應(yīng),但第二組同學(xué)認(rèn)為第一組同學(xué)的實(shí)驗(yàn)不夠嚴(yán)謹(jǐn),其理由是。若利用B裝置,要得到科學(xué)嚴(yán)謹(jǐn)?shù)慕Y(jié)論,需補(bǔ)做的對比實(shí)驗(yàn)是。
(3)第一組同學(xué)經(jīng)過反復(fù)討論認(rèn)為可通過向A、B實(shí)驗(yàn)反應(yīng)后的溶液中滴加酚酞溶液來確定NaOH與CO2的反應(yīng)是否發(fā)生,第二組同學(xué)又提出反對意見,認(rèn)為該方法不可行,理由是。
第二組實(shí)驗(yàn)方案如下:
(4)利用圖Ⅱ裝置進(jìn)行實(shí)驗(yàn),測得裝置內(nèi)壓強(qiáng)變化情況如圖Ⅲ所示。①首先注入瓶中的藥品是(填“水”或“氫氧化鈉溶液”)。②對比曲線中段和段,可證明二氧化碳能與氫氧化鈉發(fā)生反應(yīng)。
(5)拓展延伸同學(xué)們經(jīng)過反思,設(shè)計并進(jìn)行了如圖所示的實(shí)驗(yàn),觀察到瓶中產(chǎn)生,再次證明氫氧化鈉溶液與二氧化碳發(fā)生了反應(yīng),寫出與氯化鋇溶液發(fā)生反應(yīng)的化學(xué)方程式:。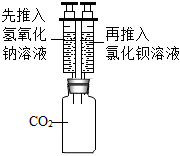 組卷:34引用:2難度:0.4
組卷:34引用:2難度:0.4


