魯科版(2019)必修第二冊《1.3.2 研究同主族元素的性質》2021年同步練習卷(4)
發布:2024/11/12 13:30:2
一、選擇題(共9小題,每小題3分,滿分27分)
-
1.下列有關堿金屬元素和鹵素的說法中,錯誤的是( )
A.溴單質與H2的反應比碘單質與H2的反應更劇烈 B.堿金屬元素中,鋰原子失去最外層電子的能力最弱;鹵素中,氟原子得電子的能力最強 C.鉀與水的反應比鈉與水的反應更劇烈 D.隨核電荷數的增加,堿金屬元素和鹵素的熔沸點都逐漸降低 組卷:189引用:20難度:0.9 -
2.鐳是元素周期表中第七周期第ⅡA族元素,關于其敘述不正確的是( )
A.鐳的金屬性比鈣弱 B.單質能與水反應生成H2 C.在化合物中呈+2價 D.碳酸鐳難溶于水 組卷:82引用:27難度:0.7 -
3.下列物質:①水;②氫氟酸;③燒堿溶液;④濃硫酸;⑤氧化鈣;⑥濃硝酸;⑦碳酸鈉固體。其中,在一定條件下能與SiO2反應的是( )
A.②③⑤⑦ B.①③⑤⑥ C.①④⑥ D.全部 組卷:18引用:2難度:0.8
二、解答題(共2小題,滿分0分)
-
10.堿金屬元素是指ⅠA族中除H以外的金屬元素,完成下列問題:
(1)下列有關比較不正確的是。(填序號)
①原子半徑:K>Na>Li
②單質還原性:K>Na>Li
③離子氧化性:Cs+>Rb+>K+
④堿性:LiOH<NaOH<KOH
(2)銫位于元素周期表第6周期ⅠA族,根據銫在元素周期表中的位置,推斷下列內容:
①銫原子核外共有個電子層,最外層電子數為。
②銫單質與水劇烈反應,放出色氣體,生成的溶液可使紫色石蕊溶液顯色。
③預測銫單質的還原性比鈉單質的還原性。(填“弱”或“強”)組卷:13引用:1難度:0.6 -
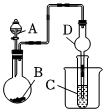 11.根據如圖所示裝置回答以下問題。已知:①KMnO4常溫下與濃鹽酸反應可制得Cl2;②H2SiO3不溶于水。
11.根據如圖所示裝置回答以下問題。已知:①KMnO4常溫下與濃鹽酸反應可制得Cl2;②H2SiO3不溶于水。
(1)利用如圖裝置可以驗證元素非金屬性的變化規律。圖中A裝置的名稱是。干燥管D的作用是。
(2)實驗室中現有藥品Na2S、KMnO4、濃鹽酸、MnO2,請選擇合適藥品設計實驗驗證氯的非金屬性強于硫:燒瓶中發生反應的離子方程式為。裝置C中的實驗現象為有淡黃色沉淀生成,離子方程式為。
(3)若要用此裝置證明酸性:HNO3>H2CO3>H2SiO3,進而證明非金屬性:N>C>Si,從以下所給物質中選出甲同學設計的實驗所用到的物質:①稀HNO3;②稀鹽酸;③碳酸鈣;④Na2SiO3溶液;⑤SiO2
試劑A與C分別為(填序號);試管中發生反應的離子方程式為。
有同學認為此實驗不能說明N、C、Si的非金屬性強弱,你認為原因。組卷:83引用:3難度:0.5


