2020-2021學年陜西省延安市寶塔四中高一(下)期末化學試卷
發布:2024/4/20 14:35:0
一、選擇題(本大題共16小題,每小題3分,計48分。每小題只有一個選項是符合題意的)
-
1.下列關于太能、氫能和生物質能的說法不正確的是( )
A.大自然利用太陽能最成功的是植物的光合作用 B.生物質能來源于植物及其加工產品所貯存的能量 C.利用藍綠藻等低等植物和微生物在陽光作用下使水分解產生氫氣并放出熱量 D.用高壓氫氣、氧氣制作氫氧燃料電池也是氫能源利用的一種重要方式 組卷:66引用:3難度:0.8 -
2.下列屬于一次電池的是( )
A.鎳氫電池 B.鋅錳干電池 C.鋰離子電池 D.鉛蓄電池 組卷:19引用:1難度:0.5 -
3.X和Y是短周期元素,二者能形成化合物X2Y3,若Y的原子序數為n,則X的原子序數不可能是( )
A.n-8 B.n-3 C.n-1 D.n+5 組卷:39引用:7難度:0.7 -
4.下列化學用語正確的是( )
A.H2、D2、T2互為同素異形體 B.M2+核外有a個電子、b個中子,M的核素符號 M:a+b+2a+2C.H2O2的電子式: 
D.用電子式表示Na2S的形成過程:2  +
+ →
→ 組卷:4引用:1難度:0.7
組卷:4引用:1難度:0.7 -
5.下列說法不正確的是( )
A.一個反應經過的步驟越多,放出的熱量越多 B.在特定條件下,反應熱等于焓變 C.一個化學反應的焓變與反應途徑無關 D.應用蓋斯定律,可計算某些難以測定的反應焓變 組卷:2引用:1難度:0.7 -
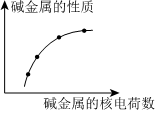 6.如圖表示第ⅠA族金屬(即堿金屬)的某些性質與核電荷數的變化關系,則下列各性質中不符合圖示關系的是( )
6.如圖表示第ⅠA族金屬(即堿金屬)的某些性質與核電荷數的變化關系,則下列各性質中不符合圖示關系的是( )A.金屬性 B.與水反應的劇烈程度 C.陽離子的氧化性 D.原子半徑 組卷:71引用:5難度:0.8 -
7.下列事實與電化學無關的是( )
A.紅熱的鐵絲與水接觸,表面形成黑色的保護層 B.鐵制自來水管不能與銅制水龍頭連接 C.白鐵表面有劃損時,也能阻止鐵被腐蝕 D.家用炒菜鐵鍋用水清洗放置后,出現紅棕色的銹漬 組卷:1引用:1難度:0.6
二、非選擇題(本大題共5小題,計52分)
-
20.甲醇作為燃料,在化石能源和可再生能源時期均有廣泛的應用前景。
Ⅰ.甲醇可以替代汽油和柴油作為內燃機燃料
(1)汽油的主要成分之一是辛烷[C8H18(l)]。已知:25℃、101kPa時,1molC8H18(l)完全燃燒生成氣態二氧化碳和液態水,放出5518kJ熱量。該反應的熱化學方程式為。
(2)已知:25℃、101kPa時,CH3OH(g)+O2(g)═CO2(g)+2H2O(l) ΔH=-726.5kJ/mol,則相同質量的甲醇和辛烷分別完全燃燒時,放出熱量較多的是32。
(3)已知:CH3OH(g)+O2(g)═CO(g)+2H2O(g) ΔH=-393kJ?mol-1,該反應相關化學鍵鍵能數據如下表:
則X=化學鍵 O=O C-O C≡O H-O C-H E/(kJ?mol-1) X 343 1076 465 413 。
Ⅱ.甲醇的合成
(4)以CO2(g)和H2(g)為原料合成甲醇,反應的能量變化如圖所示。
①補全上圖:圖中A處應填。
②該反應需要加入銅一鋅基催化劑。加入催化劑后,該反應的ΔH(填“變大”、“變小”或“不變”)。
(5)已知:CO(g)+O2(g)═CO2(g) ΔH1=-283kJ/mol;12
H2(g)+O2(g)═H2O(g) ΔH2=-242kJ/mol;12
CH3OH(g)+O2(g)═CO2(g)+2H2O(g) ΔH3=-676kJ/mol。32
以CO(g)和H2(g)為原料合成甲醇的反應為CO(g)+2H2(g)═CH3OH(g),該反應的ΔH=kJ/mol。組卷:7引用:1難度:0.7 -
 21.如圖所示,C、D、E、F都是惰性電極,A、B為電源。將電源接通后,向乙中滴入酚酞溶液,在F極附近顯紅色,D質量增加。
21.如圖所示,C、D、E、F都是惰性電極,A、B為電源。將電源接通后,向乙中滴入酚酞溶液,在F極附近顯紅色,D質量增加。
(1)AB作為電源,可以利用多種原電池來提供電能,興趣小組同學設計如下電源:
①小紅同學設計利用反應“Cu+2Fe3+=Cu2++2Fe2+”制成化學電池來提供電能,該電池的負極材料是,電解質溶液是。
②小秦同學設計將鋁片和銅片用導線相連,一組插入濃硝酸中,一組插入燒堿溶液中,分別形成了原電池,在這兩個原電池中,負極分別為(填字母)。
A.鋁片、銅片
B.銅片、鋁片
C.鋁片、鋁片
D.銅片、銅片
(2)若甲中裝有足量的硫酸銅溶液,工作一段時間后,停止通電,欲使溶液恢復到起始狀態,可向溶液中加入(填字母)。
A.Cu
B.Cu2(OH)2CO3
C.Cu(OH)2
D.CuCO3
(3)通電后乙中發生的總反應方程式為。
(4)欲用丙裝置給銅鍍銀,則金屬銀應為(填“G”或“H”)極,反應一段時間后(用CO、氧氣燃料電池作電源)銅制品質量增加43.2g,理論上消耗氧氣的質量為g。組卷:24引用:2難度:0.5


