2022-2023學年湖南省長沙一中高一(上)期中化學試卷
發布:2024/4/20 14:35:0
一、選擇題(本題共10小題,每小題3分,共30分,在每小題給出的四個選項中,只有一項是符合題目要求的)
-
1.近年來我國大力弘揚中華優秀傳統文化體現了中華民族的文化自信。下列有關說法不正確的是( )
A.成語“百煉成鋼”、“水滴石穿”中均涉及了氧化還原反應 B.《本草經集注》中記載了區分硝石(KNO3)和樸消(Na2SO4)的方法:“以火燒之,紫青煙起,乃真硝石也”,二者也可以利用“焰色試驗”區分 C.侯氏制堿法的工藝過程中應用了物質溶解度的差異 D.《荷塘月色》中“薄薄的青霧浮起在荷塘里”中的“青霧”屬于膠體 組卷:14引用:1難度:0.8 -
2.通過研究物質分類,可以發現物質的變化規律,下列有關物質的分類正確的是( )
A.堿:NaOH、純堿、熟石灰 B.堿性氧化物:Fe2O3、Na2O2、CaO C.酸性氧化物:CO2、SO2、SO3 D.電解質:氫氧化鐵、稀鹽酸、干冰 組卷:26引用:2難度:0.8 -
3.常溫下,下列各組離子在指定溶液中能大量共存的是( )
A.酸性溶液中:Na+、NH4+、Cl-、SO42- B.加入Na2O2的溶液中:K+、SO32-、Cl-、OH- C.無色透明的溶液中:Cu2+、Mg2+、NO3-、Cl- D.含NaHSO4的溶液中:K+、CO32-、NO3-、NH4+ 組卷:25引用:1難度:0.7 -
4.下列離子方程式正確的是( )
A.Cl2通入水中:Cl2+H2O═2H++Cl-+ClO- B.過量的CO2與澄清石灰水反應:OH-+CO2═HCO3- C.鈉與硫酸銅溶液反應:2Na+Cu2+═Cu+2Na+ D.鈉與水反應:Na+H2O═Na++OH-+H2↑ 組卷:21引用:1難度:0.7 -
5.下列氯化物中,既能由金屬和氯氣直接反應制得,又能由金屬和鹽酸反應制得的是( )
A.CuCl2 B.FeCl2 C.FeCl3 D.AlCl3 組卷:731引用:110難度:0.9 -
6.下列說法正確的是( )
A.MnO2+4HCl(濃) MnCl2+Cl2↑+2H2O中,氧化劑和還原劑的個數之比為1:4△B.2H2S+SO2═3S+2H2O中,氧化產物和還原產物的質量之比為1:1 C.5NH4NO3═4N2↑+2HNO3+9H2O中,發生氧化反應和發生還原反應的氮元素的質量之比為3:5 D.3Cu2S+22HNO3═6Cu(NO3)2+10NO↑+3H2SO4+8H2O中,每生成1個NO轉移3個電子 組卷:65引用:1難度:0.5
三、非選擇題(本題共4小題,共54分)
-
17.鈉及其化合物在化工生產和日常生活中都有廣泛的用途。
Ⅰ.目前,世界多數國家采用電解熔融氯化鈉的方法來生產金屬鈉:2NaCl(熔融)2Na+Cl2↑。已知物質A、B、C、D、E、F、G有如圖轉化關系(部分反應條件及產物已省略):電解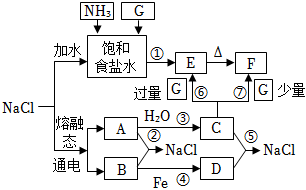
(l)寫出物質A、B在加熱條件下發生反應②的實驗現象:。
(2)反應①~⑦中屬于氧化還原反應的是(填序號)。
(3)F的飽和溶液中通入足量G的離子方程式為。
Ⅱ.化學膨松劑可以使食品變得松軟或酥脆。某興趣小組為測定潮濕環境中長期存放的碳酸氫鈉膨松劑中NaHCO3的含量,設計了以下實驗,并按如圖所示連接裝置(氣密性良好,各裝置中的試劑皆為足量)。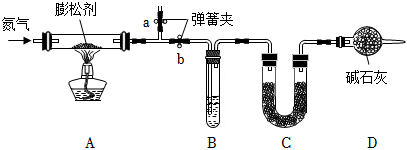
已知:在潮濕的環境中NaHCO3會慢慢變為Na2CO3?10H2O。
(4)寫出膨松劑中NaHCO3受熱分解的化學方程式:。
(5)若A裝置中反應管右側有水珠,則測得的NaHCO3含量將(填“偏高”“偏低”或“無影響”)。
(6)若膨松劑的質量為wg,反應后C裝置增加的質量為mg,則膨松劑中NaHCO3的質量分數為(用含w、m的代數式表示)。組卷:94引用:3難度:0.6 -
18.高鐵酸鉀(K2FeO4)是一種新型、高效、無毒的多功能水處理劑。K2FeO4為紫色固體,微溶于KOH溶液,具有強氧化性,在酸性或中性溶液中快速產生O2,在堿性溶液中較穩定;Fe3+遇KSCN溶液顯紅色。
(1)制備K2FeO4。
①裝濃鹽酸的儀器名稱是。
②請寫出A中制備氯氣的化學方程式:,D中的離子方程試:。
③B中裝的藥品是。
④C中,氯氣先與KOH反應生成次氯酸鉀,次氯酸鉀再與氫氧化鐵和KOH反應生成高鐵酸鉀(K2FeO4),在該反應體系中,71g氯氣完全反應后理論上最多可生成高鐵酸鉀g。
(2)探究K2FeO4的性質。取C中紫色溶液,加入稀硫酸,產生黃綠色氣體,得溶液a,經檢驗氣體中含有Cl2。為證明K2FeO4能否氧化Cl-而產生Cl2,設計以下方案:
①由方案Ⅰ中溶液變紅可知a中含有Fe3+,該離子的產生能否判斷它是由K2FeO4被Cl-還原形成的,并說明理由?方案Ⅰ 取少量溶液a,滴加KSCN溶液至過量,溶液呈紅色。 方案Ⅱ 用KOH溶液充分洗滌C中所得固體,再用KOH溶液將K2FeO4溶出,得到紫色溶液b。取少量b,滴加鹽酸,有Cl2產生。 。
②使用時經常通過高鐵酸鉀與稀硫酸反應生成氧氣的量來測高鐵酸鉀的純度。請寫出該測定過程中反應的離子方程式:。組卷:36引用:2難度:0.5


