2021-2022學年江西省吉安市吉安縣三中、泰和二中、安福二中、井大附中高二(上)期中化學試卷
發布:2024/4/20 14:35:0
一、選擇題(每小題只有一個選項符合題意,每小題3分,共48分。)
-
1.化學與社會、生產、生活密切相關,下列說法不正確的是( )
A.純堿可用來清洗油污 B.海水淡化可以解決淡水危機,用光催化分解代替電解水制氫氣可實現節能環保 C.我國油品從國V汽油升級到國Ⅵ汽油,有助于減少酸雨、霧霾,提高空氣質量 D.天然氣、沼氣和太陽能分別屬于化石能源、可再生能源和二次能源 組卷:12引用:3難度:0.8 -
2.25℃、101kPa下,碳、氫氣、甲烷和葡萄糖的燃燒熱依次是393.5kJ/mol、285.8kJ/mol、890.3kJ/mol、2800kJ/mol,則下列熱化學方程式正確的是( )
A.C(s)+ O2(g)═CO(g)△H=-393.5kJ/mol12B.2H2(g)+O2(g)═2H2O(g)△H=+571.6kJ/mol C.CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3kJ/mol D. C6H12O6(s)+3O2(g)═3CO2(g)+3H2O(l)△H=-1400kJ/mol12組卷:153引用:34難度:0.7 -
3.下列事實不能用勒夏特列原理解釋的是( )
A.H2、I2、HI混合氣體加壓后顏色變深 B.溫度過高對合成氨不利 C.紅棕色的NO2加壓后顏色先變深后變淺 D.常溫下,將1mLpH=3的醋酸溶液加水稀釋至l00mL,測得其pH<5 組卷:17引用:3難度:0.5 -
4.將CaCO3放入密閉的真空容器中,反應:CaCO3 (s)?CaO(s)+CO2(g)達到平衡。保持溫度不變,縮小容器容積,體系重新達到平衡,下列說法正確的是( )
A.平衡常數減小 B.CaO物質的量不變 C.CO2濃度不變 D.平衡正向移動 組卷:29引用:6難度:0.5 -
5.高氯酸、硫酸、硝酸和鹽酸都是強酸,其酸性在水溶液中差別不大。表是某溫度下這四種酸在冰醋酸中的電離常數,由表格數據判斷以下說法中不正確的是( )
酸 HClO4 H2SO4 HCl HNO3 Ka 1.6×10-5 6.3×10-9 1.6×10-9 4.2×10-10 A.相同條件下在冰醋酸中,硝酸是這四種酸中最弱的酸 B.在冰醋酸中,這四種酸都沒有完全電離 C.在冰醋酸中,硫酸的電離方程式為H2SO4?H++HSO4-、HSO4-?H++SO42- D.電解質的強弱與所處的溶劑無關 組卷:88引用:4難度:0.7 -
6.下列事實不能用來判斷醋酸為弱電解質的是( )
A.常溫下測定相同濃度醋酸和鹽酸溶液的pH B.常溫下比較形狀相同大小相同的鎂條與相同濃度的鹽酸與醋酸反應的速率大小 C.比較相同體積、相同濃度的鹽酸和醋酸分別與0.1mol?L-1氫氧化鈉溶液反應所消耗的氫氧化鈉溶液的體積 D.相同溫度下比較相同濃度的鹽酸和醋酸的導電能力 組卷:30引用:2難度:0.5 -
7.某科研團隊研制出“TM-LiH(TM表示過渡金屬)”雙催化劑體系,顯著提高了在溫和條件下氮氣和氫氣合成NH3的效率,原理示意如下:
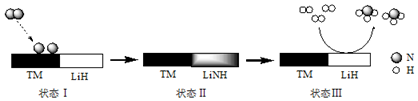
下列分析不合理的是( )A.狀態Ⅰ,吸收能量并有N≡N鍵發生斷裂 B.合成NH3總反應的原子利用率是100% C.“TM-LiH”能降低合成氨反應的△H D.生成NH3:2LiNH+3H2═2LiH+2NH3 組卷:181引用:19難度:0.5
二、填空題:(5個小題,共52分)
-
20.H2O2不穩定、易分解,Fe3+、Cu2+等對其分解起催化作用,為比較Fe3+和Cu2+對H2O2分解的催化效果,某化學研究小組同學分別設計了圖1圖2兩種實驗裝置.
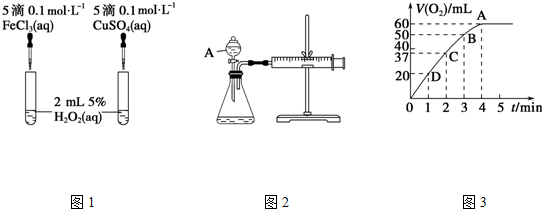
(1)若利用圖1實驗,可通過觀察現象,從而定性比較得出結論.有同學提出將FeCl3改為Fe2(SO4)3更為合理,其理由是,寫出H2O2在二氧化錳催化作用下發生反應的化學方程式:,若利用圖2實驗可進行定量分析,圖中儀器A的名稱為,實驗時均以生成40mL氣體為準,其他可能影響實驗的因素均已忽略,實驗中還需要測量的數據是.
(2)將0.1mol MnO2粉末加入50mL H2O2溶液中,在標準狀況下放出氣體的體積和時間的關系如圖3所示,解釋反應速率變化的原因:,H2O2初始物質的量濃度為(保留兩位有效數字).
(3)為了加深同學們對影響反應速率因素的認識,老師讓同學完成如下實驗:在上述實驗裝置的錐形瓶內加入6.5g鋅粒,通過分液漏斗加入40mL 2.5mol?L-1的硫酸,10s時收集產生的H2的體積為44.8mL(標準狀況),用硫酸表示10s內該反應的速率為mol?L-1?s-1(假設反應前后溶液的體積不變).組卷:54引用:4難度:0.3 -
21.用酸堿中和滴定法測定某燒堿的純度。
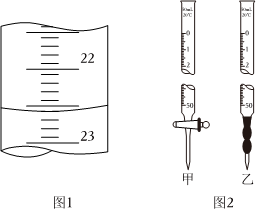
(1)滴定管的使用:如圖1是滴定管中的液面,其讀數為mL。
(2)配制待測液:將1.70g含有少量雜質(不與鹽酸反應)的固體燒堿樣品配制成200mL溶液。
(3)滴定
①盛裝0.2000mol?L-1鹽酸標準液應該用圖2的(甲或乙)滴定管。
②滴定時,先向錐形瓶中加2~3滴甲基橙作為指示劑;滴定過程中兩眼應注視,當時為滴定終點。
③有關數據記錄如下:
(4)純度計算:燒堿樣品的純度為滴定序號 待測液體積(mL) 消耗鹽酸標準液的體積(mL) 滴定前 滴定后 1 20.00 0.50 20.70 2 20.00 6.00 26.00 。
(5)對下列幾種假定情況的討論(填“偏高”“偏低”或“無影響”):
①若用蒸餾水沖洗錐形瓶,則會使測定的結果。
②若在滴定過程中不慎將數滴酸液滴在錐形瓶外,則會使測定結果。
③若剛見到指示劑局部的顏色有變化就停止滴定,則會使測定結果。組卷:11引用:2難度:0.5


