2023年湖南省百校聯考高考化學摸底試卷
發布:2024/4/20 14:35:0
一、選擇題:本題共14小題,每小題3分,共42分。在每小題給出的四個選項中,只有一項是符合題目要求的。
-
1.從日常生活到科技前沿,化學無處不在。下列說法正確的是( )
A.熱水泡茶涉及萃取、分液等操作 B.天然奶油、黃油等是從牛奶或羊奶中提取出的半固態物質,屬于蛋白質 C.速滑競賽服使用聚氨酯材料可減少空氣阻力,聚氨酯是高分子材料 D.用于制造“山東艦”上艦載機降落攔阻索的特種鋼,屬于新型無機非金屬材料 組卷:122引用:5難度:0.9 -
2.下列實驗操作或裝置(略去部分夾持儀器)正確的是( )
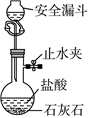
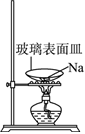
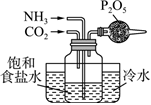
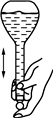
A.制取少量CO2 B.鈉的燃燒 C.制備NaHCO3 D.配制一定物質的量濃度的溶液 A.A B.B C.C D.D 組卷:65引用:3難度:0.5 -
3.已知氯化1-乙基-3-甲基咪唑(
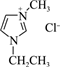 )被廣泛應用于有機合成和聚合反應、分離與提純以及電化學研究中。下列說法錯誤的是( )
)被廣泛應用于有機合成和聚合反應、分離與提純以及電化學研究中。下列說法錯誤的是( )A.電負性:Cl>C>H B.五元環處于同一平面,則兩個氮原子的雜化方式分別為sp3、sp2 C.1mol氯化1-乙基-3-甲基咪唑中含有σ鍵數目為16NA D.氯化1-乙基-3-甲基咪唑中的化學鍵類型:離子鍵、共價鍵 組卷:75引用:2難度:0.6 -
4.綠柱石(X3Z2W6Y18)是一種重要的礦物。X、Y、Z、W為短周期元素,原子序數依次增加,且價電子數和為15。X、Z、W處于相鄰的主族,X2+和Z3+的電荷與半徑之比相近,導致兩元素性質相似。下列說法正確的是( )
A.第一電離能:Z<W,第二電離能:Z>W B.原子半徑:Z>W>Y>X C.XY是堿性氧化物,WY2是酸性氧化物 D.已知W、Y都可與氫氣生成氫化物,電負性Y>W>H 組卷:119引用:4難度:0.7 -
5.下列工業生產過程中所發生反應的離子方程式,不正確的是( )
A.海水提鎂中用石灰乳沉鎂:Mg2++2OH-═Mg(OH)2↓ B.海水提溴中用SO2水溶液富集溴:SO2+Br2+2H2O═4H++SO42-+2Br- C.氯堿工業中電解飽和食鹽水:2Cl-+2H2O H2↑+Cl2↑+2OH-電解D.侯氏制堿法中獲取碳酸氫鈉:NH3+H2O+CO2+Na+═NaHCO3↓+NH4+ 組卷:57引用:2難度:0.7 -
6.二氧化鍺常用作有機物的催化劑以及半導體的原料。一種從ZnO煙塵(主要成分為ZnO?GeO2,含ZnS、PbO2、CaO、FeO等雜質)中提純二氧化鍺的工藝流程如圖。

已知:GeO2?nH2O在濃鹽酸中的溶解度很低。
下列說法正確的是( )A.在濾液中加入ZnO固體調pH,先得Fe(OH)3沉淀,后得Zn(OH)2沉淀 B.“沉鍺”后分離出單寧與Ge4+的產物所用玻璃儀器為玻璃棒、分液漏斗、燒杯 C.GeCl4水解的離子方程式為Ge4++(n+2)H2O═GeO2?nH2O+4H+ D.“水解”操作時為保證GeCl4,水解徹底進行,需加入過量高純水 組卷:31引用:2難度:0.7
二、非選擇題:共4小題,共58分。
-
17.我國科學家首次實現了二氧化碳到淀粉的人工合成,關鍵的一步是利用化學催化劑將高濃度CO2還原成CH3OH。CO2催化加氫制CH3OH的反應體系中,發生的主要反應如下。
Ⅰ.CO2(g)+3H2(g)?CH3OH+H2O(g)ΔH1
Ⅱ.CO2(g)+H2(g)?CO(g)+H2O(g)ΔH2
Ⅲ.CO(g)+2H2(g)═CH3OH(g)ΔH3
回答下列問題:
(1)已知上述反應Ⅰ、Ⅱ、Ⅲ的平衡常數K與溫度T的關系為:lnK1=x+,lnK2=y+AT,lnK3=z+BT(x、y、z、A、B、C均為常數,A、C均大于零,B小于零)。則反應Ⅰ的活化能Ea(正)CTEa(逆),的數值范圍是ΔH1ΔH3。
(2)反應Ⅰ可能的反應歷程如圖所示。已知:方框內包含微粒種類及數目、微粒的相對總能量;TS表示過渡態、*表示吸附在催化劑上的微粒。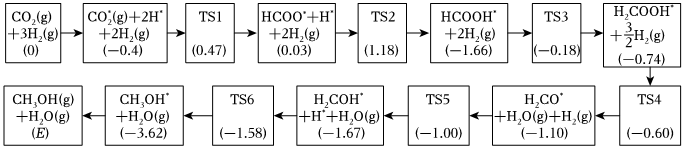
則反應歷程中決速步驟的反應方程式為。
(3)在催化劑作用下,將1molCO2和2molH2的混合氣體充入一恒容密閉容器中進行反應,達平衡時,CO2的轉化率和容器中混合氣體的平均相對分子質量隨溫度變化如圖。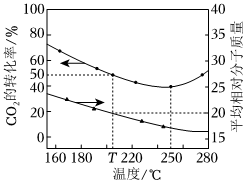
①250℃后,隨溫度升高,平衡時混合氣體的平均相對分子質量幾乎不變的原因是。
②T℃時,反應的初始壓強為p0,平衡時甲醇的選擇性(生成甲醇消耗的CO2在CO2總消耗量中占比)為,反應Ⅰ的平衡常數Kp=(Kp為以分壓表示的平衡常數,分壓=總壓×物質的量的分數)。若再向密閉容器中通入CO2和H2O(g),使二者分壓均增大0.1p0,則H2的轉化率(填“增大”“減小”或“不變”)。組卷:68引用:2難度:0.5 -
18.化合物Ⅰ是一種治療抑郁癥的藥物,一種合成路線如圖。

已知:ⅰ.R1CHO+CH2(COOH)2R1CH=CHCOOH①吡啶△②H+R2OOCCH2CN催化劑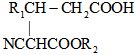
ⅱ.R4OHCH3SO2Cl三乙胺R4OR3R3OHNaH
回答下列問題:
(1)A的名稱為,C中官能團有種。
(2)B→C反應的化學方程式為。
(3)C→D的反應類型為,G的結構簡式為。
(4)M的分子式為C7H6O3,則M的結構簡式為,則M的同分異構體中,滿足下列條件的有種。
①遇FeCl3溶液變紫色;
②只含一個環狀結構;
③1mol該有機物與足量金屬鈉反應生成1molH2。
(5)已知ⅰ.R1CH=CH42R1CHO+R2CHO;①O3②Zn,H2O
ⅱ.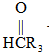 H2O2乙酸
H2O2乙酸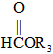
根據相關信息,寫出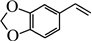 為主要原料制備M的合成路線:。組卷:29引用:1難度:0.5
為主要原料制備M的合成路線:。組卷:29引用:1難度:0.5


