2022-2023學年廣東省廣州市番禺中學高二(上)期末化學試卷
發布:2024/11/30 12:0:2
一、選擇題(本題共16小題,每小題3分,共48分。每小題的四個選項中,只有一項符合題目要求。)
-
1.下列依據熱化學方程式得出的結論正確的是( )
A.已知2H2(g)+O2(g)═2H2O(g)ΔH=-483.6kJ?mol-1;則氫氣的燃燒熱為241.8kJ?mol-1 B.已知 C(石墨,s)═C(金剛石,s)ΔH>0;則金剛石比石墨穩定 C.已知NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)ΔH=-57.4kJ?mol-1;則含20.0gNaOH的稀溶液與稀鹽酸完全中和,放出28.7kJ的熱量 D.已知2C(s)+2O2(g)═2CO2(g)ΔH1,2C(s)+O2(g)═2CO(g)ΔH2;則ΔH1>ΔH2 組卷:116引用:8難度:0.5 -
2.下列表示正確的是( )
A.中子數為176的某核素: Ts176117B.基態鋅原子的價層電子排布式:3d104s2 C.26Fe3+的結構示意圖: 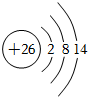
D.基態氮原子的軌道表示式: 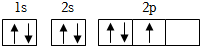 組卷:468引用:10難度:0.5
組卷:468引用:10難度:0.5 -
3.2molA與2molB混合于2L的密閉容器中,發生如下反應2A(g)+3B(g)?2C(g)+ZD(g)若2s后,A的轉化率為50%,測得v(D)=0.25 mol?L-1?s-1,下列推斷正確的是( )
A.v (C)=v (D)=0.25 mol?L-1?s-1 B.Z=3 C.B的轉化率為25% D.C的體積分數為20% 組卷:19引用:3難度:0.6 -
4.已知NO2和N2O4可以相互轉化:2NO2(g)?N2O4(g)(正反應為放熱反應).現將一定量NO2和N2O4的混合氣體通入一體積為2L的恒溫密閉容器中,反應物物質的量隨時間變化關系如圖所示,則下列說法錯誤的是( )
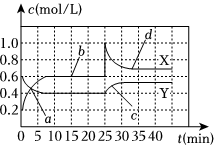
A.前10min內用NO2表示的化學反應速率v(NO2)=0.02mol/(L?min) B.反應進行至25min時,曲線發生變化的原因可以是向容器中添加NO2(g) C.若要達到與最后相同的化學平衡狀態,在25min時還可以采取的措施是添加N2O4(g) D.a、b、c、d四個點中,表示化學反應處于平衡狀態的點成是b和d 組卷:53引用:4難度:0.7 -
5.一定溫度下,恒容容器中下列敘述不能作為可逆反應A(g)+3B(g)?2C(g)達到平衡標志的是( )
①C的生成速率與C的消耗速率相等
②單位時間內生成amolA,同時生成3amolB
③A、B、C的濃度不再變化
④C的物質的量不再變化
⑤混合氣體的總壓強不再變化
⑥混合氣體的總物質的量不再變化
⑦單位時間消耗amolA,同時生成3amolB
⑧A、B、C的分子數之比為1:3:2A.⑤⑥ B.④⑦ C.①③ D.②⑧ 組卷:237引用:2難度:0.6 -
6.常溫下,某溶液中由水電離出的c(OH-)=1×10-5mol?L-1,則該溶液中的溶質是( )
A.CH3COONa B.NaOH C.NH3?H2O D.KI 組卷:67引用:1難度:0.8
二、解答題(共4小題,滿分52分)
-
19.ⅥA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表現出多種氧化態,含ⅥA族元素的化合物在研究和生產中有許多重要用途。請回答下列問題:
S單質的常見形式為S8,其環狀結構如圖所示,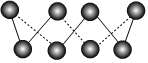
(1)S原子價電子排布式。S原子的核外不同運動狀態的電子數是個,能量最高的3p軌道是電子云的形狀是。
(2)S8的S原子采用的軌道雜化方式是。
(3)氣態SeO3分子的空間立體構型為,離子的VSEPR模型為SO2-3。
(4)H+可與H2O形成H3O+,H3O+中H-O-H鍵角比H2O中H-O-H鍵角(填大或小)。組卷:16引用:1難度:0.6 -
20.磷酸鋅常用作氯化橡膠合成高分子材料的阻燃劑。工業上利用燒渣灰(主要含ZnO,還含少量FeO、Al2O3、CuO及SiO2Al3+)為原料制取磷酸鋅的工藝流程如圖所示:
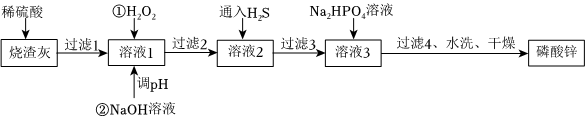
已知:①[Zn3(PO4)2]在水中幾乎不溶,其在水中的溶解度隨溫度的升高而降低;
②“溶1”中幾種金屬離子開始沉淀與沉淀完全的pH如表所示:
(1)燒渣灰加入稀硫酸時,請寫出ZnO與反應的稀硫酸離子方程式金屬離子 Fe3+ Cu2+ Zn2+ 開始沉淀的pH 3.0 2.2 5.4 6.5 完全沉淀的pH 5.0 3.6 6.7 8.5 。
(2)加入H2O2的作用。
(3)經過濾2得到濾渣的主要成分是Fe(OH)3和Al(OH)3,則用NaOH溶液調節pH的范圍是。
(4)加入Na2HPO4溶液發生反應的離子方程式為。
(5)洗滌磷酸鋅沉淀時應選用(填“冷水”或“熱水”),確認磷酸鋅洗滌干凈的操作是。
(6)通入H2S是為了除銅離子,25℃時,當通入H2S達到飽和時測得溶液的pH=1,c(H2S)=0.1mol?L-1,此時溶液中c(Cu2+)=6.3×10-15mol?L-1,則CuS的溶度積Ksp=(已知:25℃時,H2S的電離平衡常數Ka1=1×10-7,Ka2=1×10-15)。組卷:29引用:1難度:0.4


