2021-2022學(xué)年安徽省滁州市定遠(yuǎn)縣育才學(xué)校高二(下)第二次月考化學(xué)試卷
發(fā)布:2024/4/20 14:35:0
一、選擇題(本大題共16小題每小題3分,滿分48分)
-
1.下列各組原子中,彼此化學(xué)性質(zhì)一定相似的是( )
A.最外層都只有一個(gè)電子的X、Y原子 B.原子核外M層上僅有兩個(gè)電子的X原子與N層上僅有兩個(gè)電子的Y原子 C.2p軌道上有三個(gè)未成對(duì)電子的X原子與3p軌道上有三個(gè)未成對(duì)電子的Y原子 D.原子核外電子排布式為1s2的X原子與原子核外電子排布式為1s22s2的Y原子 組卷:39引用:2難度:0.7 -
2.下表是A、B、C、D、E、F六種短周期元素的部分化合價(jià)、電負(fù)性和原子半徑數(shù)據(jù)。下列說法正確的是 ( )
元素 A B C D E F 化合價(jià) +1 -2 -1 -2 -1 +1 電負(fù)性 2.1 2.5 3.0 3.5 4.0 0.9 原子半徑/nm 0.037 0.102 0.099 0.073 0.071 0.154 A.F與A的單質(zhì)均為金屬 B.A2D2、F2D2都是含有非極性鍵的離子化合物 C.氧化物對(duì)應(yīng)水化物的酸性:B<C<E D.簡(jiǎn)單陰離子的還原性:E<C<B 組卷:6引用:3難度:0.6 -
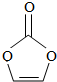 3.碳酸亞乙烯酯是鋰離子電池低溫電解液的重要添加劑,其結(jié)構(gòu)如圖,下列有關(guān)該物質(zhì)的說法正確的是( )
3.碳酸亞乙烯酯是鋰離子電池低溫電解液的重要添加劑,其結(jié)構(gòu)如圖,下列有關(guān)該物質(zhì)的說法正確的是( )A.分子式為C3H2O3 B.分子中含6個(gè)σ鍵 C.分子中只有極性鍵 D.8.6g該物質(zhì)完全燃燒得到6.72LCO2 組卷:848引用:33難度:0.9 -
4.共價(jià)鍵具有飽和性和方向性。下列有關(guān)敘述中,不正確的是( )
A.共價(jià)鍵的飽和性是由成鍵原子的未成對(duì)電子數(shù)決定的 B.共價(jià)鍵的方向性是由成鍵原子軌道的方向性決定的 C.共價(jià)鍵的方向性決定了分子的空間結(jié)構(gòu) D.所有共價(jià)鍵都具有方向性 組卷:37引用:5難度:0.7 -
5.已知1~18號(hào)元素的離子aW3+、bX+、cY2-、dZ-都具有相同的電子層結(jié)構(gòu),下列關(guān)系正確的是( )
A.質(zhì)子數(shù)c>d,離子的還原性Y2->Z- B.氫化物的穩(wěn)定性H2Y>HZ C.原子半徑X<W,第一電離能X<W D.電負(fù)性Z>Y>W(wǎng)>X 組卷:194引用:29難度:0.7 -
6.下列有關(guān)化學(xué)鍵的比較一定錯(cuò)誤的是( )
A.鍵能:C-N<C=N<C≡N B.鍵長(zhǎng):I-I>Br-Br>Cl-Cl C.分子中的鍵角:H2O>CO2 D.相同元素原子間形成的共價(jià)鍵鍵能:σ鍵>π鍵 組卷:65引用:7難度:0.7
二、填空題(本大題共4小題,滿分52分)
-
19.氯吡苯脲是一種常用的膨大劑,其結(jié)構(gòu)簡(jiǎn)式為
 ,它是經(jīng)國(guó)家批準(zhǔn)使用的植物生長(zhǎng)調(diào)節(jié)劑。
,它是經(jīng)國(guó)家批準(zhǔn)使用的植物生長(zhǎng)調(diào)節(jié)劑。
(1)氯元素基態(tài)原子核外電子的未成對(duì)電子數(shù)為。
(2)氯吡苯脲晶體中,氮原子的雜化軌道類型有,羰基碳原子的雜化軌道類型為。
(3)已知,可用異氰酸苯酯與2-氯-4-氨基吡啶反應(yīng)生成氯吡苯脲:
反應(yīng)過程中,每生成1mol氯吡苯脲,斷裂molσ鍵,斷裂mol π鍵。
(4)膨大劑能在動(dòng)物體內(nèi)代謝,其產(chǎn)物較為復(fù)雜,其中有H2O、NH3、CO2等。
①請(qǐng)用共價(jià)鍵的相關(guān)知識(shí)解釋H2O分子比NH3分子穩(wěn)定的原因:。
②H2O、NH3、CO2分子的空間結(jié)構(gòu)分別是,中心原子的雜化類型分別是。組卷:62引用:8難度:0.5 -
20.已知A、B、C、D、E都是周期表中前四周期的元素,它們的核電荷數(shù)依次增大。其中A、B、C是同一周期的非金屬元素。化合物DC為離子化合物,D形成的二價(jià)陽離子與C形成的簡(jiǎn)單陰離子具有相同的電子層結(jié)構(gòu)。AC2為非極性分子。B、C的簡(jiǎn)單氫化物的沸點(diǎn)比它們同主族相鄰周期元素的氫化物的沸點(diǎn)高。E是前四周期中原子核外電子排布中未成對(duì)電子數(shù)最多的元素。請(qǐng)根據(jù)以上情況,回答下列問題:
(1)A、B、C的電負(fù)性由小到大的順序?yàn)?(用對(duì)應(yīng)元素符號(hào)表示,下同)
(2)A的氫化物中有一種組成為A2H2的分子,其中A原子的軌道雜化類型為,1molA2H2所含σ鍵的數(shù)目為。
(3)寫出化合物AC2的電子式:。
(4)E的價(jià)電子排布式是。
(5)B的最高價(jià)氧化物對(duì)應(yīng)的水化物的稀溶液與D的單質(zhì)反應(yīng)時(shí),B被還原到最低價(jià),該反應(yīng)的化學(xué)方程式是。組卷:32引用:2難度:0.5


