2021-2022學年山東省濟南市章丘四中高一(下)第一次質檢化學試卷
發布:2024/11/14 14:30:2
一、單選題(每題只有一個選項,每題3分,共30分)
-
1.設NA為阿伏加德羅常數值。下列有關敘述正確的是( )
A.標準狀況下,2.24L三氧化硫中含原子數為0.4NA B.100g質量分數17%的H2O2水溶液中極性鍵數目為NA C.常溫常壓下,8.4g碳酸氫鈉中含離子數為0.3NA D.標準狀況下,20g的D2O中所含質子數目和中子數目均為10NA 組卷:6引用:1難度:0.6 -
2.已知質量數為A的某陽離子Rn+,核外有X個電子,則核內中子數為( )
A.A-x B.A-x-n C.A-x+n D.A+x-n 組卷:153引用:49難度:0.9 -
3.某元素甲氣態氫化物與該元素最高價氧化物的水化物反應生成鹽,乙元素的簡單離子半徑在第三周期中最小,丙元素和丁元素同主族且原子序數丙是丁的兩倍,下列說法正確的是( )
A.食品包裝袋中可以用甲的氣態氫化物做保護氣 B.1mol乙的單質在標準狀況下和濃硝酸反應后,生成的氣體約為67.2L C.丙和丁的常見單質的沸點,丙的高 D.乙和丁形成的化合物做的坩堝可以用來熔融NaOH 組卷:5引用:2難度:0.5 -
4.類推是一種常采用的科研和學習方法,下列類推結論合理的是( )
A.由單質鐵和氯氣反應生成FeCl3,推出單質鐵和碘單質反應生成FeI3 B.由元素周期表中從上到下,鹵族元素單質熔沸點逐漸升高,推出堿金屬元素單質熔沸點逐漸升高 C.最高價氧化物的水化物的酸性,由N的強于P的,推出F的強于Cl的 D.由Na在常溫下與水劇烈反應,推出Cs在常溫下也能與水劇烈反應 組卷:4引用:1難度:0.8 -
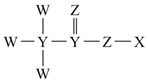 5.一種殺蟲劑的分子結構如圖所示。其中X、Y、Z、W是原子序數依次增大的短周期元素,且X、Y、W處于不同周期,只有Y的單質常溫下呈固態,Y原子的核外電子總數等于Z原子的最外層電子數。下列有關說法錯誤的是( )
5.一種殺蟲劑的分子結構如圖所示。其中X、Y、Z、W是原子序數依次增大的短周期元素,且X、Y、W處于不同周期,只有Y的單質常溫下呈固態,Y原子的核外電子總數等于Z原子的最外層電子數。下列有關說法錯誤的是( )A.簡單氫化物的沸點:Z>Y B.Y、Z同周期且兩者可形成兩種常見的氣態化合物 C.含氧酸的酸性:W>Y D.1molW的單質溶于足量的水中,充分反應后轉移電子小于1mol 組卷:6引用:2難度:0.6 -
6.在無機非金屬材料中,硅一直扮演著主要的角色。請你利用元素周期律的相關知識,預測硅及其化合物的性質。下列說法不正確的是( )
A.晶體硅的導電性介于導體和絕緣體之間,是良好的半導體材料 B.SiO2是酸性氧化物,可以與水反應:SiO2+H2O═H2SiO3 C.Na2SiO3可溶于水,在水溶液中電離方程式為:Na2SiO3═2Na++SiO32- D.在高溫下,能發生反應SiO2+Na2CO3═Na2SiO3+CO2↑,但是不能證明H2SiO3的酸性大于碳酸 組卷:37引用:2難度:0.6
三、非選擇題(共3個大題)
-
 17.食品添加劑中可能存在的部分短周期元素的最高正化合價或最低負化合價與原子序數的關系如圖所示。已知:x為非金屬元素,d元素的最外層電子數為內層電子數的3倍。
17.食品添加劑中可能存在的部分短周期元素的最高正化合價或最低負化合價與原子序數的關系如圖所示。已知:x為非金屬元素,d元素的最外層電子數為內層電子數的3倍。
(1)x、e、d三種元素形成的離子化合物的電子式為。
(2)圖中g元素所在元素周期表中的位置,f元素形成的最高價氧化物與NaOH溶液反應的離子方程式為。元素h的氣態氫化物穩定性比元素g的氣態氫化物穩定性(填“強”或“弱”)。
(3)d、e、f、g元素的簡單離子半徑由小到大的順序為(用化學式表示)。
(4)x和d組成的化合物中,既含有極性共價鍵又含有非極性共價鍵的是(填電子式)。組卷:3引用:2難度:0.6 -
18.氮化硅是一種性能優異的無機非金屬材料,它的熔點高,硬度大,電絕緣性好,化學性質穩定,但生產成本較高。不溶于酸(氫氟酸除外)。高溫下氧氣及水蒸氣能明顯腐蝕氮化硅。一種用工業硅(含少量鐵、銅的單質及氧化物)和N2(含少量O2)合成氮化硅的工藝流程如圖:
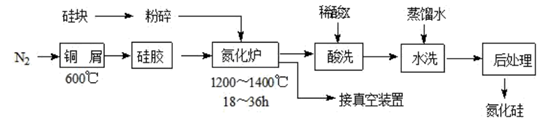
(1)N2凈化時,銅屑的作用是;硅膠的作用是。
(2)X可能是(選填:“鹽酸”、“硝酸”、“硫酸”、“氫氟酸”)。
(3)如何說明氮化硅產品已用水洗干凈?。
(4)推測氮化硅可能有哪些用途:(填字母)。
a.制作切削刀具
b.制作坩堝
c.制作耐高溫軸承
(5)工業上還可以采用化學氣相沉積法,在H2的環境中,使SiCl4與N2在高溫下反應生成Si3N4沉積在石墨表面,該反應的化學方程式為。組卷:7引用:1難度:0.5


