2022-2023學年福建省莆田市荔城區九年級(上)期末化學試卷
發布:2024/12/6 2:0:2
一、選擇題。本卷共10小題,每小題3分,共30分。在每小題給出的四個選項中,只有一個選項符合題目要求。
-
1.物質的性質決定用途,下列說法不正確的是( )
A.氮氣--化學性質穩定,可制取氮肥 B.氫氣--有可燃性,可用作燃料 C.氧氣--有助燃性,可用作煉鋼 D.二氧化碳--促進植物光合作用,可用作氣體肥料 組卷:6引用:1難度:0.6 -
2.下列圖示實驗操作中,正確的是( )
A. 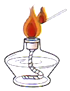
B. 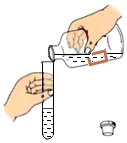
C. 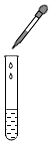
D. 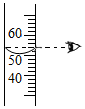 組卷:492引用:35難度:0.8
組卷:492引用:35難度:0.8 -
3.下列所列變化趨勢中不準確的是( )
A. 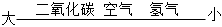
密度(通常狀況)B. 
硬度C. 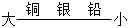
導電性D. 
金屬活動性組卷:25引用:1難度:0.6 -
4.泡騰片放入水中,產生很多氣泡。其原理是,泡騰片中的檸檬酸(C6H8O7)和碳酸氫鈉(NaHCO3)在水中發生了如下反應:C6H8O7+3NaHCO3═C6H5O7Na3+3H2O+3X↑,其中X的化學式是( )
A.CO B.CO2 C.O2 D.H2 組卷:48引用:6難度:0.6 -
5.布洛芬具有良好的解熱鎮痛功效,它的化學式為(C13H18O2)。下列敘述不正確的是( )
A.布洛芬組成元素有3種 B.碳、氫、氧元素質量比為13:18:2 C.1個布洛芬分子由13個碳原子、18個氫原子和2個氧原子構成 D.布洛芬中氫元素的質量分數為8.7% 組卷:12引用:2難度:0.7 -
6.《天工開物》中關于寶石的部分記載如下:凡水晶出深山穴內瀑流石醇之中,水晶的主要成分為SiO2,其結構與金剛石相似,下列關于水晶的說法不正確的是( )
A.難溶于水 B.常溫下化學性質穩定 C.質地堅硬 D.其主要成分由離子構成 組卷:24引用:1難度:0.6
二、非選擇題。本卷共8題,共70分。
-
 17.興趣小組的同學對鋁的某些性質進行相關探究。
17.興趣小組的同學對鋁的某些性質進行相關探究。
【實驗回顧】
(1)鋁與稀鹽酸反應。
①用圖1所示裝置制取氫氣。
②用B裝置收集氫氣的最佳時機是。
(2)在金屬活動性順序里,金屬能否置換出鹽酸和稀硫酸中的氫,判斷的依據是。
【提出問題】
鋁能否與水反應生成氫氣?
【查閱資料】
【交流與討論】物質 鈉與水 鋁與水 汞與水 能否發生反應 能反應 能反應 不反應
鋁在空氣中與氧氣反應,表面生成一層致密的氧化鋁薄膜,起到保護膜的作用。
(3)除去鋁表面氧化鋁薄膜的方法(舉一例)。除上述方法外,還可以將鋁片浸入氯化汞(HgCl2)溶液中,形成鋁汞齊(鋁汞合金)破壞鋁表面致密的氧化膜且防止其重新生成。
【實驗探究】
(4)將鋁片完全沒入氯化汞(HgCl2)溶液中1分鐘左右,取出,立即用流水沖洗干凈后加入到蒸餾水中(如圖2),其表面生成大量氣泡、周圍出現白色沉淀。鋁與氯化汞溶液發生置換反應的化學方程式為。
(5)在導管口處涂肥皂水,發現導管口有氣泡形成,當氣泡離開導管后,氣泡(填“下沉”或“上升”),用燃著的木條點燃氣泡,發出爆鳴聲。
【實驗結論】
鋁能與水反應生成氫氣。
【實驗反思】
(6)圖2裝置圖,在鋁與水反應的過程中。若關閉導管上的活塞K,反應停止,其原理是。若再次打開活塞K,反應繼續,產生氣泡。鋁未能生成氧化鋁,其原因是。
汞有毒,會污染環境,興趣小組的同學用硫粉處理單質汞,用飽和硫化鈉溶液處理使用過的氯化汞廢液。組卷:39引用:3難度:0.6 -
18.在煤中加入適量的生石灰制成供居民采暖用的“環保煤”,以減少二氧化硫的排放,減輕二氧化硫對空氣的污染。“環保煤”燃燒時生石灰吸收二氧化硫的化學方程式為:2CaO+2SO2+O2
2CaSO4。請回答下列問題:若煤廠一次共加入含氧化鈣80%的生石灰樣品70t,則理論上最多可吸收二氧化硫多少噸?高溫組卷:16引用:1難度:0.5


