2022-2023學年重慶市高二(上)期末化學試卷
發布:2024/4/20 14:35:0
一、選擇題(共16小題,每小題3分,滿分48分)
-
1.下列各能層不包含d能級的是( )
A.O能層 B.P能層 C.M能層 D.K能層 組卷:179引用:5難度:0.9 -
2.如圖是第三周期11~17號元素某些性質變化趨勢的柱形圖,下列有關說法中正確的是( )
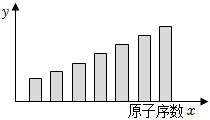
A.y軸表示的可能是第一電離能 B.y軸表示的可能是電負性 C.y軸表示的可能是原子半徑 D.y軸表示的可能是形成基態離子轉移的電子數 組卷:260引用:20難度:0.9 -
3.設NA為阿伏加德羅常數的數值,下列有關敘述正確的是( )
A.1.2gNaHSO4晶體中含有的離子總數為0.02NA B.0.1mol白磷(P4)或四氯化碳中所含的共價鍵數目均為0.4NA C.足量Fe粉投入1L1mol?L-1稀HNO3中,轉移的電子數為3NA D.25℃時,1.0LpH=13的Ba(OH)2溶液中含有的OH-數目為0.2NA 組卷:12引用:1難度:0.8 -
4.元素周期表中共有18縱列,從左到右排為18列,第1列為堿金屬元素(氫元素除外),第18列為稀有氣體元素,則下列說法正確的是( )
A.第9列元素中沒有非金屬元素 B.第15列元素原子的最外層電子排布式是ns2np5 C.最外層電子排布式為ns2的元素一定在第2列 D.第14列元素中未成對電子數是同周期元素中最多的 組卷:77引用:4難度:0.6 -
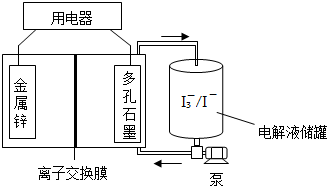 5.鋅碘液流電池具有高電容量、對環境友好、不易燃等優點,可作為汽車的動力電源。該電池采用無毒ZnI2水溶液作電解質溶液,放電時將電解液儲罐中的電解質溶液泵入電池,其裝置如圖所示。下列說法不正確的是( )
5.鋅碘液流電池具有高電容量、對環境友好、不易燃等優點,可作為汽車的動力電源。該電池采用無毒ZnI2水溶液作電解質溶液,放電時將電解液儲罐中的電解質溶液泵入電池,其裝置如圖所示。下列說法不正確的是( )A.M是陽離子交換膜 B.充電時,多孔石墨接外電源的正極 C.充電時,儲罐中的電解液導電性不斷增強 D.放電時,每消耗1molI3-,有1 molZn2+生成 組卷:121引用:6難度:0.7 -
6.某原子最外層電子排布為2s22p3,則該原子( )
A.核外有5個電子 B.核外有3種能量不同的電子 C.最外層電子占據3 個軌道 D.最外層上有3 種運動狀態不同的電子 組卷:115引用:3難度:0.7
二、解答題(共4小題,滿分0分)
-
19.為了探究原電池和電解池的工作原理,某研究性學習小組分別用下圖所示的裝置進行實驗。據圖回答問題:
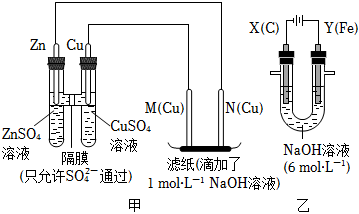
I.用圖甲所示裝置進行第一組實驗時:
(1)在保證電極反應不變的情況下,不能替代Cu作電極的是(填字母)。
A石墨 B.鎂 C.銀 D.鉑
(2)實驗過程中,SO42-(填“從左向右”“從右向左”或“不”)移動;濾紙上能觀察到的現象是。
II.該小組同學用圖乙所示裝置進行第二組實驗時發現,兩極均有氣體產生,且Y極處溶液逐漸變成紫紅色;停止實驗觀察到鐵電極明顯變細,電解液仍然澄清。查閱資料知,高鐵酸根(FeO42-)在溶液中呈紫紅色。請根據實驗現象及所查信息,回答下列問題:
(3)電解過程中,X極處溶液的OH-濃度(填“增大”“減小”或“不變)。
(4)電解過程中,Y極發生的電極反應為。
(5)電解進行一段時間后,若在X極收集到672 mL氣體Y電板(鐵電極)質量減小0.28g,則在Y極收集到氣體為mL(均已折算為標準狀況時氣體體積)。
(6)K2FeO4-Zn也可以組成堿性電池,K2FeO4在電池中作為正極材料,其電池反應總反應式為2K2FeO4+3Zn═Fe2O3+ZnO+2K2ZnO2,該電池正極發生 的電極反應式為。組卷:37引用:5難度:0.4 -
20.尿酸(HUr)屬于一元弱酸,是嘌呤的最終代謝產物。當人體內尿酸過高時,會引起高尿酸血癥、痛風等疾病。常溫下,Ka(HUr)=4.0×10-6,回答下列問題:
(1)常溫下,Ur-的水解常數Kh=。
(2)常溫下,0.01mol?L-1HUr溶液的pH約為(已知lg2=0.3)。
(3)下列溶液中水的電離程度由大到小的順序為(填序號)。
①向水中加入少量的尿酸(HUr)
②向水中加入少量的氯化鈉
③向水中加入少量的尿酸鈉(NaUr)
(4)設計兩種實驗方案,證明尿酸(HUr)是弱酸:、。
(5)NaUr溶液與鹽酸恰好完全反應后的溶液中,下列關系式正確的是(填標號)。
A.c(Na+)=c(Ur-)+c(HUr)
B.c(Ur-)>c(Cl-)>c(OH-)
C.c(Na+)+c(H+)=c(Ur-)+c(OH-)
D.c(H+)=c(Ur-)+c(OH-)
(6)寒冷季節,人體關節滑液中形成NaUr晶體,會誘發關節疼痛,請用化學平衡理論解釋關節保暖減輕疼痛的原因。組卷:23引用:2難度:0.7


