2023年黑龍江省大慶市讓胡路區景園中學中考化學一模試卷
發布:2024/4/20 14:35:0
一、選擇題(本題共10小題,每小題4分,共40分,每題只有一個正確選項)
-
1.下列實驗中有關說法不正確的是( )
A. 
利用紅磷燃燒實驗驗證質量守恒定律,燃燒時氣球脹大不會影響實驗B. 
根據實驗現象呼出氣體中澄清石灰水變渾濁可證明呼出氣體中二氧化碳含量比空氣中高C. 
檢查裝置氣密性時,看到導管口有均勻連續的氣泡冒出,說明氣密性良好D. 
稀釋濃硫酸時,玻璃棒攪拌的目的是使熱量迅速散失組卷:16引用:1難度:0.7 -
2.化學與社會、人類生活密切相關,下列歸納有錯誤的一項是( )
A.化學與生活 B.化學與安全 ①除冰箱異味——用活性炭
②除水垢——用飽和食鹽水
③除廚具油污——用洗潔精①重金屬中毒——喝鮮牛奶、豆漿等解毒
②煤氣泄漏——關閉氣閥,嚴禁煙火
③溶洞探險——先做燈火試驗C.化學與環境 D.化學與健康 ①減少汽車尾氣污染——使用乙醇汽油
②減少酸雨的發生——使用新能源
③減少水污染——使用無磷洗衣粉①缺鋅——發育不良
②缺碘——易患甲狀腺腫大
③缺鈣——易患佝僂病A.A B.B C.C D.D 組卷:42引用:2難度:0.7 -
3.建立模型是學習化學的重要方法,下列模型不正確的是( )
A. 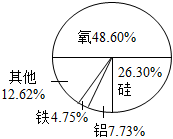
地殼中元素含量模型B. 
物質組成及構成模型C. 
物質分類D. 
滅火方法的目的模型組卷:59引用:7難度:0.4 -
4.下列指定反應的化學方程式正確的是( )
A.鋁的自我保護:4Al+3O2═2Al2O3 B.酸雨形成的原因:CO2+H2O═H2CO3 C.配制波爾多液:CaO+H2O+CuSO4═CaSO4+Cu(OH)2↓ D.小蘇打治療胃酸過多:Na2CO3+2HCl═2NaCl+CO2↑+H2O 組卷:25引用:2難度:0.5 -
5.類推是一種重要的學習方法。下列類推結論錯誤的是( )
①CO能與Fe2O3反應生成Fe,CO也能與CuO反應生成Cu
②NaOH溶液能使無色酚酞試液變紅色,Cu(OH)2也能使無色酚酞試液變紅色
③有機化合物含碳元素,則含碳元素的化合物一定是有機化合物
④溶液是均一穩定的,則均一穩定的液體一定是溶液
⑤堿溶液呈堿性,能使無色酚酞變紅,則呈堿性的溶液一定是堿溶液A.1個 B.2個 C.3個 D.4個 組卷:36引用:2難度:0.5 -
6.為達到實驗目的,下列實驗方案設計正確的是( )
選項 實驗目的 實驗方案 A 檢驗某物質中是否含有碳酸根離子 加稀鹽酸,觀察是否有氣泡冒出 B 除去KCl固體中混有的少量MnO2 加水溶解,過濾、洗滌、干燥 C 鑒別H2、CH4、CO三種氣體 分別點燃,觀察火焰顏色 D 鑒別稀硫酸、NaOH、Na2SO4三種溶液 分別滴入酚酞溶液后,再相互混合,觀察溶液顏色變化 A.A B.B C.C D.D 組卷:582引用:11難度:0.7
三、實驗題(本題共2小題,共21分)
-
17.氫氧化鈉暴露在空氣中會與二氧化碳反應而變質。
【提出問題】二氧化碳與氫氧化鈉溶液反應沒有明顯現象,從哪些視角可以證明CO2與NaOH溶液發生了反應?
【作出猜想】猜想一:從生成物的視角;猜想二:從的視角;
猜想三:從能量變化的視角……………。
【實驗探究1】第一組同學分別取反應后的溶液少許于試管中,按如下四種方案實驗:
A.滴加酚酞試液,若變紅則說明沒發生反應
B.滴加BaCl2溶液,若有白色沉淀生成,則說明發生了反應
C.滴加澄清石灰水,若有白色沉淀生成,則說明發生了化學反應
D.滴加足量的稀鹽酸,若產生能使澄清石灰水變渾濁的氣體,則說明發生了反應。
①該小組同學通過討論,一致認為方案是不正確的,原因是。
②若方案B正確,請寫出此方案涉及的化學反應方程式:。
【實驗探究2】第二組同學對二氧化碳的性質再探究。實驗步驟如下:
(1)圖1所示裝置的氣密性良好,三個250mL的燒瓶內收集滿CO2氣體,三個注射器內各裝有85mL的液體(分別是水、飽和石灰水、40%的氫氧化鈉溶液),連接好裝置和壓強傳感器。
(2)三位同學同時迅速將注射器內85mL的液體(水、飽和石灰水、40%的氫氧化鈉溶液)注入各自燒瓶中,關閉活塞。
(3)一段時間后,三位同學同時振蕩燒瓶,觀察燒瓶內氣壓隨時間變化的曲線(如圖2)。
①曲線2與曲線3差異較大的原因是。
②對比曲線1、2、3,不能得出的結論是(填序號)。
A.CO2能與水發生反應
B.1體積水約溶解1體積CO2
C.CO2能與NaOH溶液發生反應
D.檢驗CO2用飽和澄清石灰水較合適
E.吸收CO2用NaOH溶液較合適
【實驗探究3】化學反應常常件隨著能量的變化,第三組同學利用溫度傳感器獲得了實驗過程中溫度隨時間變化的曲線(如圖3),曲線Ⅲ為CO2與NaOH溶液的反應,曲線Ⅳ為CO2與水的反應。由此證明CO2與NaOH反應是反應(選填“吸熱”或“放熱”)。
【拓展延伸】查閱資料,已知Na2CO3溶液與CO2也會發生反應,化學方程式:Na2CO3+CO2+H2O═2NaHCO3。
當10g8%的NaOH溶液通入一定體積的CO2后,所得溶液中的溶質是Na2CO3和NaHCO3,則參加反應的CO2的體積范圍為(該狀況下,CO2的密度為2g/L)。組卷:164引用:2難度:0.3
四、計算題
-
18.根據如圖所示的實驗過程和提供的數據進行計算:

(1)原混合物中NaCl的質量;
(2)AgNO3溶液溶質質量分數。(精確到0.1%)組卷:233引用:9難度:0.5


