2022-2023學年陜西省西安市大聯考高一(下)期中化學試卷
發布:2024/4/20 14:35:0
一、本卷共25小題,每小題2分,共50分。在每小題給出的四個選項中,只有一項是符合要求的。
-
1.化學在生產和日常生活中有著重要的應用.下列說法正確的是( )
A.汽車的排氣管上裝有“催化轉化器”,使有毒的CO和NO反應生成N2和CO2 B.向煤中加入適量石灰石,使煤燃燒產生的SO2最終生成CaSO3,可減少對大氣的污染 C.高純度的硅單質廣泛用于制作光導纖維 D.大量燃燒化石燃料排放的廢氣中含CO2、SO2,從而使雨水的pH=5.6形成酸雨 組卷:118引用:13難度:0.9 -
2.下列說法正確的是( )
A.SO2有毒,不能用作食品添加劑 B.燃煤中加入生石灰可以減少SO2的排放 C.2molN2可與6molH2完全反應生成4molNH3 D.氨水中含有NH3?H2O和H2O 兩種分子 組卷:113引用:5難度:0.6 -
3.《本草圖經》中關于綠礬的分解有如下描述:“綠礬形似樸消(Na2SO4?10H2O)而綠色,取此物置于鐵板上,聚炭,封之囊袋,吹令火熾,其礬即沸,流出,色赤如融金汁者是真也.”對此段話的說明中肯定錯誤的是( )
A.綠礬的化學式為FeSO4?7H2O B.綠礬分解過程中沒有發生電子的轉移 C.“色赤”物質可能是Fe2O3 D.流出的液體中可能含有硫酸 組卷:115引用:12難度:0.9 -
4.陶瓷是火與土的結晶,是中華文明的象征之一,其形成、性質與化學有著密切的關系。下列說法錯誤的是( )
A.“雨過天晴云破處”所描述的瓷器青色,來自氧化鐵 B.聞名世界的秦兵馬俑是陶制品,由黏土經高溫燒結而成 C.陶瓷是應用較早的人造材料,主要化學成分是硅酸鹽 D.陶瓷化學性質穩定,具有耐酸堿侵蝕、抗氧化等優點 組卷:1814引用:37難度:0.8 -
5.在研究合成氨方法的歷史上,不同的研究者曾3次獲諾貝爾化學獎。合成氨大大提高了農作物的產量,同時也是制取硝酸、炸藥等的原料。下列說法中正確的是( )
A.N2和H2在點燃或光照條件下可合成NH3 B.NH3和HNO3溶于水后都能導電,故二者都是電解質 C.NH3遇到濃硝酸會發生反應產生大量白煙 D.由NH3制HNO3的過程中,氮元素被還原 組卷:110引用:5難度:0.7 -
6.硅的氧化物及硅酸鹽構成了地殼中大部分的巖石、沙子和土壤.在無機非金屬材料中,硅一直扮演著主角.下面幾種物質中含有硅單質的是( )
A.  瑪瑙
瑪瑙B.  光導纖維
光導纖維C.  太陽能電池板
太陽能電池板D.  水晶組卷:104引用:31難度:0.9
水晶組卷:104引用:31難度:0.9 -
7.下列制取SO2、驗證其漂白性、收集并進行尾氣處理的裝置和原理能達到實驗目的的是( )
A. 
制取SO2B. 
驗證漂白性C. 
收集SO2D. 
尾氣處理組卷:1546引用:73難度:0.9 -
8.2019年世界環境日中國主題為“藍天保衛站,我是行動者”,旨在引導社會各界自覺踐行綠色生活,共建美麗中國。下列現象與污染源對應不正確的是( )
A.酸雨——硫的氧化物、氮的氧化物 B.光化學煙霧——碳氫化合物、氮的氧化物 C.臭氧空洞——氟氯烴(如氟利昂) D.溫室效應——SO2 組卷:21引用:3難度:0.7 -
9.下列圖象分別表示有關反應的反應過程與能量變化的關系。據此判斷下列說法中正確的是( )
A. 
石墨轉變為金剛石是吸熱反應B. 
等質量的S(g)完全燃燒放出的熱量小于S(s)C. 
白磷比紅磷穩定D. 
CO(g)+H2O(g)═CO2(g)+H2(g)為吸熱反應組卷:61引用:5難度:0.7
二、本卷均為必考題,共4大題50分。請考生將答案寫在答題卡相應位置。
-
 28.運用化學反應原理研究化學反應有重要的意義。請回答下列問題:
28.運用化學反應原理研究化學反應有重要的意義。請回答下列問題:
(1)已知在25℃,101 kPa下,斷開1 mol H-H鍵要吸收436 kJ的能量,斷開1mol I-I鍵要吸收151 kJ的能量,斷開1 mol I-H鍵要吸收298 kJ的能量。
①通過以上數據計算當I2和H2反應生成2 molH-I時會放出9kJ的能量;若將1 mol I2和1 molH2置于密閉容器中,并在上述條件下反應,發現熱量實測值(恢復到25℃,101 kPa)遠小于上述計算值,你認為 最可能的原因是。
(2)一定條件下,甲烷與水蒸氣發生反應:CH4(g)+H2O(g)?CO(g)+3H2(g),工業上可利用此反應生產合成氨原料氣H2。
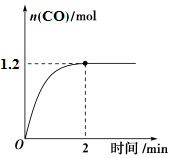
①一定溫度下,向2L恒容密閉容器中充入1.6 molCH4和2.4molH2O(g)發生上述反應,CO(g)的物質的量隨時間的變化如圖所示。0~2 min內的平均反應速率v(H2)=mol?L-1?min-1,平衡時CH4的轉化率為。[轉化率=×100%]n轉化n起始
②若要進一步提高該反應的化學反應速率,除了使用催化劑和升高溫度外,還可以采取的措施有(任寫一條)。
③下列能說明上述反應達到平衡狀態的是(填代號)。
a.v逆(CH4)=3v正(H2)
b.恒溫恒容時,容器內混合氣體的密度保持不變
c.CH4(g)、H2O(g)的濃度保持不變
d.CH4(g)、H2O(g)、CO(g)、H2(g)的物質的量之比為1:1:1:3
e.斷開3 mol H-H鍵的同時斷開2 mol O-H鍵組卷:31引用:2難度:0.3 -
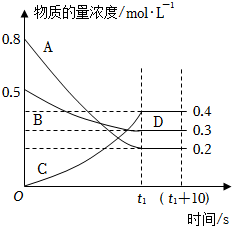 29.如圖表示在一定的溫度下,容積固定的密閉容器中,A、B、C三種氣體的物質的量濃度隨時間變化的情況。
29.如圖表示在一定的溫度下,容積固定的密閉容器中,A、B、C三種氣體的物質的量濃度隨時間變化的情況。
試回答下列問題:
(1)該反應的化學方程式為。
(2)0~t1s內氣體B的平均反應速率為。
(3)(t1+10)s時,B的物質的量分數為,此時v正(A)v逆(B)(填“>”“<”或“=”),D點是否處于平衡狀態(填“是”或“否”)。
(4)下列關于該反應的說法正確的是(填序號)。
a.到達t1時刻該反應已停止
b.在t1時刻之前,氣體B的消耗速率大于它的生成速率
c.在t1時刻,氣體C的正反應速率等于逆反應速率
(5)容器中(t1+10)s時的壓強與起始時的壓強之比為。組卷:64引用:6難度:0.4


