2020-2021學年新疆阿勒泰二中、布爾津縣高級中學等八校高二(上)期末化學試卷
發布:2024/4/20 14:35:0
一、選擇題(共25小題,每小題2分,滿分50分)
-
1.我國在探索太空、開發深海、建設高鐵、5G技術聯通等方面取得舉世矚目的成就,這些成就與化學有著密切聯系。下列說法正確的是( )
A.長征五號運載火箭箭體采用鋁合金是為了美觀耐用 B.大力發展太陽能、風能、氫能等新能源有利于生態文明建設 C.網絡強國戰略鋪設光纜線路超三千萬公里,光纜的主要成分是晶體硅 D.5G手機電池工作時,電池中化學能完全轉化為電能 組卷:26引用:6難度:0.7 -
2.下列變化過程,屬于放熱反應的是( )
①液態水變成水蒸氣 ②酸堿中和反應 ③濃H2SO4稀釋 ④固體NaOH溶于水 ⑤H2在Cl2中燃燒 ⑥食物腐敗.A.②③④⑤⑥ B.②③④ C.②⑤⑥ D.①③⑤ 組卷:748引用:27難度:0.9 -
3.氮氣與氫氣在催化劑表面發生合成氨反應的微粒變化歷程如圖所示.
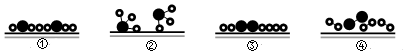
下列關于反應歷程的先后順序排列正確的是( )A.④③①② B.③④①② C.③④②① D.④③②① 組卷:239引用:3難度:0.5 -
4.下列依據熱化學方程式得出的結論正確的是( )
A.已知2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ?mol-1,則氫氣的燃燒熱為241.8kJ?mol-1 B.反應SO2(g)+2H2S(g)═3S(s)+2H2O(l)在常溫下能自發進行,則該反應的△H<0 C.已知2C(s)+2O2(g)═2CO2(g)△H=a、2C(s)+O2(g)═2CO(g)△H=b,則a>b D.已知C(石墨,s)═C(金剛石,s)△H>0,則金剛石比石墨穩定 組卷:123引用:4難度:0.5 -
5.實驗測得:101kPa時,1mol H2完全燃燒生成液態水,放出285.8kJ的熱量:1mol CH4完全燃燒生成液態水和CO2,放出890.3kJ的熱量。下列熱化學方程式的書寫正確的是( )
①CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=890.3kJ?mol-1
②CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890.3kJ
③CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3kJ?mol-1
④2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ?mol-1A.僅有②④ B.僅有④ C.僅有②③④ D.全部符合要求 組卷:76引用:7難度:0.7 -
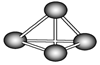 6.最近意大利科學家獲得了極具理論研究意義的N4分子。N4分子結構如圖所示,已知Ⅰ、斷裂1 mol N-N吸收167 kJ熱量,形成1 mol N≡N放出942 kJ熱量;Ⅱ、N2(g)+3H2(g)?2NH3(g)△H1=-92 kJ/mol,N4(g)+6H2(g)?4NH3(g)△H2(kJ/mol)根據以上信息和數據,下列說法正確的是( )
6.最近意大利科學家獲得了極具理論研究意義的N4分子。N4分子結構如圖所示,已知Ⅰ、斷裂1 mol N-N吸收167 kJ熱量,形成1 mol N≡N放出942 kJ熱量;Ⅱ、N2(g)+3H2(g)?2NH3(g)△H1=-92 kJ/mol,N4(g)+6H2(g)?4NH3(g)△H2(kJ/mol)根據以上信息和數據,下列說法正確的是( )A.△H2>0 B.N2分子比N4分子穩定 C.△H2=2△H1 D.△H2與方程式系數無關 組卷:48引用:5難度:0.8 -
7.在恒溫、體積為2L的密閉容器中進行反應:2A(g)?3B(g)+C(g),若反應物在前20s由3mol降為1.8mol,則前20s的平均反應速率為( )
A.v(A)=0.06mol?L-1?s-1 B.v(B)=0.045mol?L-1?s-1 C.v(C)=0.03mol?L-1?s-1 D.v(C)=0.06mol?L-1?s-1 組卷:363引用:2難度:0.6 -
8.反應:2A(g)+3B(g)?C(g)+4D(g),速率最快的是( )
A.v(A)=2.0mol?L-1?min-1 B.v(B)=4.0mol?L-1?min-1 C.v(C)=0.1mol?L-1?s-1 D.v(D)=0.3mol?L-1?s-1 組卷:69引用:5難度:0.7 -
9.對于可逆反應:2SO2(g)+O2(g)?2SO3(g),下列措施能使反應物中活化分子百分數、化學反應速率和化學平衡常數都變化的是( )
A.增大壓強 B.升高溫度 C.使用催化劑 D.多充入O2 組卷:415引用:95難度:0.9
二、解答題(共4小題,滿分50分)
-
28.常溫下,水溶液中的反應Fe3++SCN-?[Fe(SCN)]2+達到平衡時,c(SCN-)=0.10mol/L,c(Fe2+)=0.040mol/L;c[Fe(SCN)2+]=0.68mol/L.回答下列問題:
(1)加入少量KSCN固體后,平衡將向(“正”或“逆”)方向移動。
(2)該反應的平衡常數K為多少?。
(3)加水稀釋至原溶液體積的2倍,平衡將向(“正”或“逆”)方向移動。請通過相關計算說明。組卷:17引用:3難度:0.5 -
 29.用0.1500mol/L的HCl溶液滴定未知濃度的NaOH溶液,實驗數據如表所示,
29.用0.1500mol/L的HCl溶液滴定未知濃度的NaOH溶液,實驗數據如表所示,
回答下列問題:實驗編號 待測NaOH溶液的體積/mL HCl溶液的體積/mL 1 25.00 24.41 2 25.00 24.39 3 25.00 25.60
(1)實驗中,需要潤洗的儀器是:。(填寫儀器名稱)
(2)取待測液NaOH溶液25.00mL于錐形瓶中,使用酚酞做指示劑。滴定終點的判斷依據是。
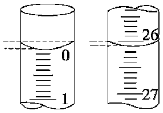
(3)若滴定開始和結束時,酸式滴定管中的液面如圖所示,則消耗鹽酸溶液的體積為mL。
(4)下列操作中會使所測結果偏高的是、偏低的是。
①酸式滴定管漏液;
②滴定前酸式滴定管尖嘴部分有氣泡,滴定過程中氣泡變小;
③滴定過程中,振蕩錐形瓶時,不小心將溶液濺出;
④滴定過程中,錐形瓶內加少量蒸餾水;
⑤用甲基橙作指示劑進行滴定時,溶液由橙色變紅色時停止滴定;
⑥用甲基橙作指示劑,溶液由黃色變橙色,5s后又變為黃色;
⑦讀酸式滴定管讀數時,滴定前仰視讀數。
(5)未知濃度的NaOH溶液的物質的量濃度為mol/L。組卷:36引用:2難度:0.5


