2012-2013學年山東省聊城市某重點高中高二(下)模塊化學試卷(3月份)
發布:2024/4/20 14:35:0
一、選擇題
-
1.欲將蛋白質從水中析出而又不改變它的性質,應加入( )
A.(NH4)2SO4溶液 B.酒精溶液 C.Pb(NO3)2溶液 D.NaOH溶液 組卷:112引用:31難度:0.5 -
2.下列生活中的化學小實驗不合理的是( )
A.用米湯檢驗加碘鹽中的碘酸鉀(KIO3) B.用食用醋除去熱水瓶中積存的水垢 C.用純堿(Na2CO3)溶液洗滌沾有油污的器具 D.用灼燒并聞氣味的方法共分化纖織物與純毛織物 組卷:18引用:8難度:0.9 -
3.下列4組連線中,完全正確的一組是( )
A. 
B. 
C. 
D.  組卷:31引用:15難度:0.7
組卷:31引用:15難度:0.7 -
4.下列化學用語的表述對應正確的是( )
A.碳酸氫鈉的電離方程式:NaHCO3═Na++H++CO32- B.用銅做陽極電解氯化銅溶液的離子方程式:Cu2++2Cl- Cu+Cl2↑電解C.硫化鈉水解的離子方程式:S2-+2H2O?H2S+2OH- D.碳酸鈣的溶解平衡:CaCO3(s)?Ca2+(aq)+CO32-(aq) 組卷:3引用:1難度:0.8 -
5.反應A+B→C(△H<0)分兩步進行 ①A+B→X (△H>0)②X→C(△H<0)下列示意圖中,能正確表示總反應過程中能量變化的是( )
A. 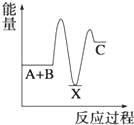
B. 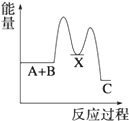
C. 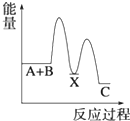
D. 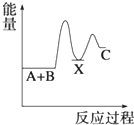 組卷:3368引用:157難度:0.9
組卷:3368引用:157難度:0.9 -
6.下列各組離子在指定的溶液中一定能大量共存的是( )
A.含有Fe3+的溶液: Na+、SCN-、Cl-、I- B.含有大量NO3-的溶液: H+、Fe2+、Cl-、SO42- C.常溫下,pH=12的溶液: K+、Cl-、SO32-、AlO2- D.c(H+)=0.1 mol?L-1的溶液: Na+、NH4+、SO42-、S2O32- A.A B.B C.C D.D 組卷:15引用:2難度:0.7 -
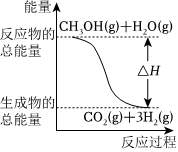 7.甲醇質子交換膜燃料電池中將甲醇蒸氣轉化為氫氣的兩種反應原理是
7.甲醇質子交換膜燃料電池中將甲醇蒸氣轉化為氫氣的兩種反應原理是
①CH3OH(g)+H2O(g)═CO2(g)+3H2(g)△H=+49.0kJ/mol
②CH3OH(g)+O2(g)═CO2(g)+2H2(g)△H=-192.9kJ/mol12
根據上述反應,下列說法正確的是( )A.反應①中的能量變化如圖所示 B.CH3OH轉變成H2的過程一定要吸收能量 C.1molCH3OH充分燃燒放出的熱量為192.9kJ D.可推知2H2(g)+O2(g)═2H2O(g)△H=-483.8 kJ/mol 組卷:22引用:24難度:0.5 -
8.下列說法與鹽的水解無關的是( )
①純堿溶液去油污
②實驗室配制FeCl3溶液時,往往在FeCl3溶液中加入少量的鹽酸
③用NaHCO3和Al2(SO4)3兩種溶液可作泡沫滅火劑
④在NH4Cl溶液中加入金屬鎂會產生氫氣
⑤草木灰與氨態氮肥不能混合施用.A.①③④ B.②③⑤ C.③④⑤ D.全有關 組卷:26引用:4難度:0.9
三、實驗題
-
25.DIS(Digital Information System)系統即數字化信息系統,它由傳感器、數據采集器和計算機組成。DIS系統為化學教學提供了全新的技術手段和教學平臺。某學習小組用DIS系統測定食用白醋中醋酸的物質的量濃度,以溶液的導電能力來判斷滴定終點。實驗步驟如下:
(1)用(填儀器名稱)量取10.00mL食用白醋,在(填儀器名稱)中用水稀釋后轉移到100mL(填儀器名稱)中定容,然后將稀釋后的溶液倒入試劑瓶中。
(2)量取20.00mL上述溶液倒入燒杯中,連接好 DIS系統(如圖1),向燒杯中滴加濃度為0.1000mol?L-1的氨水,計算機屏幕上顯示出溶液導電能力隨氨水體積變化的曲線(圖2)。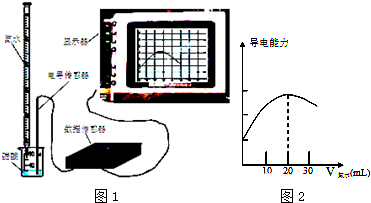
①用滴定管盛氨水前,滴定管要用潤洗2~3遍,潤洗的目的是。
②溶液導電能力隨氨水體積變化的原因是。
③食用白醋中醋酸的物質的量濃度是。組卷:4引用:2難度:0.6
四、計算題
-
26.維生素C(分子式為C6H8O6)具有較強的還原性,放置在空氣中易被氧化,其含量可通過在弱酸性溶液中用已知溶液的I2溶液進行滴定.該反應的化學方程式如下:C6H8O6+I2→C6H6O6+2HI
現欲測定某樣品中維生素C的含量,具體的步驟及測得的數據如下.取10mL 6mol?L-1CH3COOH,加入100mL蒸餾水,將溶液加熱煮沸后放置冷卻.精確稱取0.2000g樣品,溶解于上述冷卻的溶液中,加入1mL淀粉指示劑,立即用濃度為0.05000mol?L-1的I2溶液進行滴定,直至溶液中的藍色持續不褪為止,共消耗21.00mLI2溶液.
(1)為何加入的CH3COOH稀溶液要先經煮沸、冷卻后才能使用?
(2)計算樣品中維生素C的質量分數.組卷:23引用:4難度:0.1


