2015-2016學年河北省衡水市武邑中學高一(下)化學暑假作業(14)
發布:2024/4/20 14:35:0
一、選擇題(共12小題,每小題3分,滿分36分)
-
1.下列反應中生成物的總能量高于反應物的總能量的是( )
A.CO燃燒 B.H2SO4與NaOH反應 C.Ba(OH)2?8H2O晶體和NH4Cl晶體反應 D.生石灰與水作用 組卷:19引用:3難度:0.9 -
2.下列關于氯水的敘述中,正確的是( )
A.新制氯水中既有分子,又有離子 B.久置的氯水可以使干燥的有色布條褪色 C.新制氯水中滴加硝酸銀溶液,沒有任何現象 D.新制氯水在光照條件下,可以產生氣體,該氣體是氯氣 組卷:51引用:3難度:0.9 -
3.中國和瑞典的科學家共同發現了治療非典的新方法:吸入一氧化氮可快速改善重癥非典患者的缺氧狀況,緩解病情.病毒學研究同時證實,一氧化氮對非典病毒有直接抑制作用.下列有關NO的說法不正確的是( )
A.NO任意排放會造成大氣污染 B.汽車尾氣、制硝酸工廠的廢氣均含NO C.NO是造成光化學煙霧的唯一直接原因 D.NO分子所含電子總數為奇數 組卷:44引用:3難度:0.9 -
4.下列氯化物中,既能由金屬和氯氣直接反應制得,又能由金屬和鹽酸反應制得的是( )
A.CuCl2 B.FeCl2 C.FeCl3 D.AlCl3 組卷:728引用:110難度:0.9 -
5.下列說法中錯誤的是( )
A.對有氣體參加的化學反應,增大壓強,可使單位體積內活化分子百分數增加,故反應速率增大 B.升高溫度,一般可使活化分子的百分數增大,因而反應速率增大 C.活化分子之間發生的碰撞不一定為有效碰撞 D.加入適宜的催化劑,可使活化分子的百分數大大增加,從而增大化學反應的速率 組卷:7引用:3難度:0.7
二、非選擇題:
-
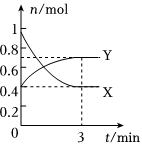 16.在一定溫度下,體積為2L的密閉容器中,NO2和N2O4之間發生反應:2NO2(g)(紅棕色)?N2O4g)(無色),如圖所示.
16.在一定溫度下,體積為2L的密閉容器中,NO2和N2O4之間發生反應:2NO2(g)(紅棕色)?N2O4g)(無色),如圖所示.
(1)曲線(填“X”或“Y”)表示NO2的物質的量隨時間的變化曲線.
(2)若降低溫度,則v(正),v(逆).(填“加快”或“減慢”或“不變”).
(3)若上述反應在甲、乙兩個相同容器內同時進行,分別測得甲中v(NO2)=0.3mol/(L?s),乙中v(N2O4)=6mol/(L?min),則中反應更快.
(4)在0到3min中內N2O4的反應速率為.
(5)下列敘述能說明該反應已達到化學平衡狀態的是(填標號);
A.v(NO2)=2v(N2O4)
B.容器內壓強不再發生變化
C.X的體積分數不再發生變化
D.容器內氣體原子總數不再發生變化
E.相同時間內消耗n mol的Y的同時生成2n mol的X
F.相同時間內消耗n mol的Y的同時消耗2n mol的X.組卷:163引用:12難度:0.3 -
 17.甲醇是一種重要的化工原料,有著重要的用途和應用前景。
17.甲醇是一種重要的化工原料,有著重要的用途和應用前景。
甲醇燃料電池(簡稱DMFC)由于結構簡單、能量轉化率高、對環境無污染,可作為常規能源的替代品而越來越受到關注。
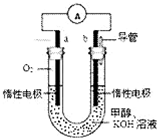
某實驗小組設計了如圖所示的甲醇燃料電池裝置。
①該電池工作時,通入氧氣的電極名稱為,電極反應式為。另一電極反應式為。氫氧根離子流向極(填正或負)
②工作一段時間后,測得溶液的堿性(填增強或減弱)。組卷:0引用:1難度:0.6


