2021-2022學(xué)年廣東省汕頭市潮陽區(qū)南僑中學(xué)高一(上)期中化學(xué)試卷
發(fā)布:2024/11/5 22:0:2
一.選擇題(本題包括18小題,每小題3分,共54分。每小題只有一個選項符合題意。)
-
1.下列實驗操作或事故處理正確的是( )
A.金屬Na著火,立即用水撲滅 B.實驗結(jié)束后,用嘴吹滅酒精燈 C.皮膚上不慎沾上濃NaOH溶液,立即用鹽酸沖洗 D.稀釋濃硫酸時,將濃硫酸沿器壁慢慢注入水中,并不斷攪拌 組卷:395引用:99難度:0.9 -
2.膠體區(qū)別于溶液最本質(zhì)的特征是( )
A.可以通過濾紙 B.有丁達爾效應(yīng) C.分散質(zhì)粒子因吸附而帶電荷 D.分散質(zhì)粒子的直徑大小 組卷:24引用:7難度:0.9 -
3.下列物質(zhì)中屬于電解質(zhì)的是( )
①氫氧化鈉 ②硫酸鋇 ③銅 ④蔗糖 ⑤二氧化硫.A.①② B.①②⑤ C.③④ D.①⑤ 組卷:47引用:23難度:0.9 -
4.與1mol NH3所含原子總數(shù)相同的是( )
A.1 mol O2 B.2 mol H2 C.1 mol H2O D.2 mol CO2 組卷:4引用:2難度:0.9 -
5.少量的金屬鈉長期暴露在空氣中,它的最終產(chǎn)物是( )
A.NaOH B.Na2CO3?10H2O C.Na2CO3 D.NaHCO3 組卷:290引用:38難度:0.9 -
6.以下說法正確的是( )
A.物質(zhì)所含元素化合價升高的反應(yīng)叫還原反應(yīng) B.在氧化還原反應(yīng)中,失去電子的元素化合價降低 C.物質(zhì)中某元素原子失去電子,則此物質(zhì)是氧化劑 D.還原劑中必定有一種元素被氧化 組卷:50引用:38難度:0.9 -
7.下列化學(xué)反應(yīng)的離子方程式中,不能用Ba2++
═BaSO4↓表示的是( )SO2-4A.氯化鋇溶液跟稀硫酸混合 B.硝酸鋇溶液跟稀硫酸混合 C.氫氧化鋇溶液跟硫酸銅溶液混合 D.氯化鋇溶液跟硫酸鈉溶液混合 組卷:7引用:2難度:0.8
二、填空題(本題包括4小題,共46分)
-
21.分析下面氧化還原反應(yīng)中化合價變化關(guān)系,直接在方程式中用雙線橋標出電子轉(zhuǎn)移的方向和數(shù)目,并在橫線上回答指定問題。
(1)3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O;
(2)氧化劑為,還原劑為,氧化產(chǎn)物,還原產(chǎn)物;
(3)被還原的元素為,被氧化的元素為,該反應(yīng)中硝酸既表現(xiàn)性,又表現(xiàn)性。組卷:4引用:1難度:0.7 -
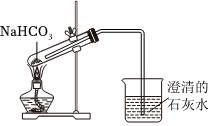 22.一學(xué)生設(shè)計如圖所示裝置進行NaHCO3的分解,并證實產(chǎn)物中有CO2產(chǎn)生。
22.一學(xué)生設(shè)計如圖所示裝置進行NaHCO3的分解,并證實產(chǎn)物中有CO2產(chǎn)生。
(1)試管中發(fā)生的化學(xué)反應(yīng)方程式是。
(2)指出該學(xué)生設(shè)計的裝置圖的錯誤之處(文字說明即可)。(至少2處)
(3)燒杯中發(fā)生反應(yīng)的離子方程式是。
(4)如果將16.8gNaHCO3加熱一段時間,然后將剩余固體溶于水,并加入足量的CaCl2溶液,最終得到白色沉淀5.0g,則NaHCO3分解百分率為,加CaCl2后反應(yīng)的離子方程式為。組卷:13引用:3難度:0.7


