2023年遼寧省沈陽二中高考化學模擬試卷(五)
發布:2024/5/15 8:0:8
一、選擇題(本題包括15小題,每小題3分,共45分,每小題只有一個選項符合題意)
-
1.化學與生產、生活密切相關,下列說法不正確的是( )
A.山梨酸鉀和苯甲酸鈉均可用作食品添加劑 B.移動通訊的核心部件芯片的主要成分是共價晶體 C.太陽能、風能、地熱能、氫能、海洋能均為新能源 D.市售食用油中加入微量叔丁基對苯二酚作氧化劑,以確保食品安全 組卷:39引用:1難度:0.6 -
2.下列化學用語或說法正確的是( )
A.Cu位于周期表d區 B.芒硝化學式:Na2SO4?10H2O C.用電子式表示H2O的形成過程: 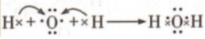
D.PH3的VSEPR模型名稱:三角錐形 組卷:54引用:1難度:0.8 -
3.用NA表示阿伏加德羅常數的值,下列說法正確的是( )
A.100g46%C2H5OH的水溶液中采取sp3雜化的原子數目為6NA B.0.1mol乙醇和0.2mol乙酸發生酯化反應,最多可生成乙酸乙酯分子數為0.1NA C.標準狀況下,5.6LCO2中所含σ鍵的數目為0.25NA D.常溫下,將2.7g鋁片投入足量的濃硫酸中,鋁失去的電子數為0.3NA 組卷:46引用:1難度:0.6 -
4.如圖為合成藥物M工藝過程中的某一步轉化關系(反應條件已省略)。
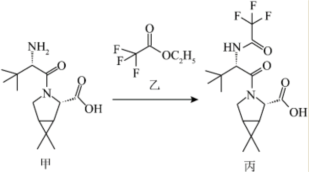
下列說法正確的是( )A.上述反應為取代反應,生成物有化合物丙和乙酸 B.化合物甲分子中含有4個手性碳原子 C.化合物甲和化合物丙均含有的官能團為氨基、酰胺基和酚基 D.丙在一定條件下可以分別與氫氧化鈉水溶液、鹽酸以及氫氣發生反應 組卷:38引用:1難度:0.5 -
5.下列實驗裝置和操作均正確的是( )
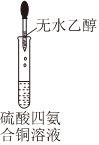
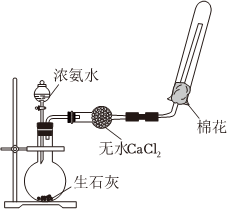
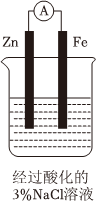
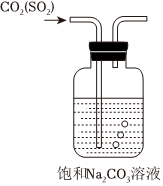
A.析出[Cu(NH3)4]SO4晶體 B.制取并收集氨氣 C.犧牲陽極法保護鐵 D.除去CO2中少量SO2 A.A B.B C.C D.D 組卷:60引用:6難度:0.6 -
6.某實驗小組要定量探究鐵銹蝕的因素,設計如圖所示實驗裝置,檢查氣密性,將5g鐵粉和2g碳粉加入三頸燒瓶,t1時刻,加入2mL飽和氯化鈉溶液后,再將一只裝有5mL稀鹽酸的注射器插到燒瓶上,采集數據。下列說法錯誤的是( )
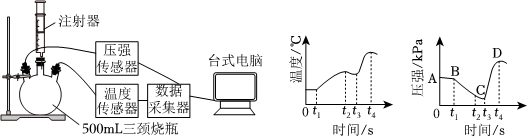
A.鐵發生銹蝕的反應是放熱反應 B.t2~t3溫度降低是因為反應速率減慢了 C.BC段壓強減小是因為鐵和氧氣直接反應生成了氧化鐵 D.t3~t4壓強變大是因為發生了鐵的析氫腐蝕 組卷:81引用:4難度:0.7
二、解答題(共4小題,滿分55分)
-
18.研究CO2的轉化可實現碳的循環利用。在反應器內CO2和H2在催化劑作用下可發生如下反應:
Ⅰ.CO2(g)+3H2(g)?CH3OH(g)+H2O(g)ΔH1
Ⅱ.CO2(g)+H2(g)?CO(g)+H2O(g)ΔH2=+41.2kJ?mol-1
(1)反應Ⅰ的歷程如圖所示,其中吸附在催化劑表面上的物種用*標注。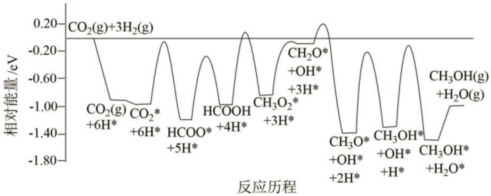
下列說法不正確的是。
A.該反應的ΔH1<0,能低溫自發
B.該歷程中最小能壘(活化能)步驟的化學方程式為:CH2O*+OH*+3H*→CH3O*+OH*+2H*
C.催化劑可以降低反應活化能和反應熱,但對反應物的轉化率無影響
D.最后一步是CH3OH(g)、H2O(g)從催化劑表面的解吸過程,△S<0
(2)若反應Ⅱ的正、逆反應速率分別表示為v正=k正c(CO2)?c(H2),v逆=kc(CO)?c(H2O),k正、k逆分別為正、逆反應速率常數,c為物質的量濃度。pk=-lgk,如圖中有表示反應Ⅱ的正、逆反應速率常數隨溫度T變化的圖象,若A、B、C、D點的縱坐標分別為a+3、a+1、a-1、a-3,則溫度T1時反應Ⅱ的化學平衡常數K=。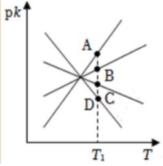
(3)在恒壓條件下,CO2和H2發生反應Ⅰ、反應Ⅱ,反應相同時間,測得不同溫度下CO2的轉化率和CH3OH的選擇性如圖中實驗值所示。圖中平衡值表示相同條件下平衡狀態CO2的轉化率和CH3OH的選擇性隨溫度的變化[CH3OH的選擇性=×100%]:n(CH3OH)生成n(CO2)消耗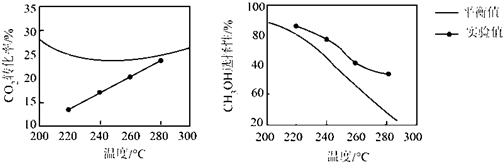
①220℃時,測得反應器出口氣體中全部含碳物質的物質的量之比n(CH3OH):n(CO2):n(CO)=1:7.2:0.11,則該溫度下CO2轉化率=(結果保留1位小數)。
②220℃~260℃甲醇的平衡選擇性隨溫度升高而降低的原因可能是。
③260℃時,甲醇產率的實驗值是。
(4)若只考慮反應Ⅰ,在有分子篩膜時甲醇的產率隨溫度的變化如圖所示,其中分子篩膜能選擇性分離出H2O,甲醇產率先增大后減小的原因是;請在圖中畫出無分子篩膜時甲醇的平衡產率隨溫度的變化曲線。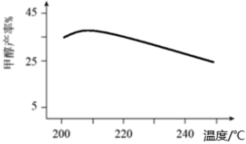 組卷:47引用:1難度:0.5
組卷:47引用:1難度:0.5 -
19.物質G是能阻斷血栓形成的藥物的中間體,它的一種合成路線如圖所示。
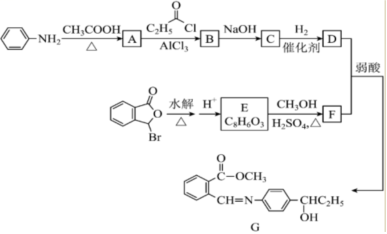
已知:i.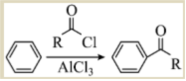 ;
;
ii.R′CHOR′CH=NR″;R″NH2弱酸
iii.同一個碳原子上連有兩個羥基不穩定,會失水形成羰基。
回答下列問題:
(1)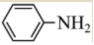 的名稱是 ,
的名稱是 ,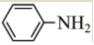 →A的反應類型是 。
→A的反應類型是 。
(2)B的分子式為C11H13NO2,則C的結構簡式為。
(3)1molE分子與新制氫氧化銅完全反應,理論上可以生成Cu2Omol。寫出E生成F的化學方程式。
(4)W分子比E分子組成多一個CH2,寫出滿足下列條件的W的一種結構簡式:。
i.包含2個六元環,不含甲基
ii.W可水解,W與NaOH溶液共熱時,1molW最多消耗3molNaOH
(5)已知Bamberger重排反應為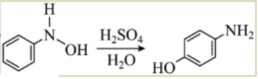 ,參考圖中合成路線,以
,參考圖中合成路線,以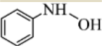 為原料,用最簡路線合成
為原料,用最簡路線合成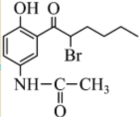 ,試劑任選 。組卷:27引用:1難度:0.3
,試劑任選 。組卷:27引用:1難度:0.3


