2022年上海市楊浦高級中學高考化學質檢試卷(5月份)
發布:2024/4/20 14:35:0
一、選擇題(本題共40分,每小題2分,每小題只有一個正確答案)
-
1.目前工業上獲得汽油主要通過( )
A.石油裂化 B.石油裂解 C.煤干餾 D.乙烯水化 組卷:23引用:2難度:0.9 -
2.萃取振蕩時,需排放氣體。放氣時分液漏斗的狀態是( )
A. 
B. 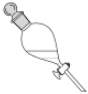
C. 
D. 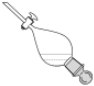 組卷:75引用:2難度:0.8
組卷:75引用:2難度:0.8 -
3.環己烯(
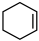 )常用于有機合成。對環己烯的說法正確的是( )
)常用于有機合成。對環己烯的說法正確的是( )A.存在于石油中 B.難溶于水 C.密度比水大 D.平面結構 組卷:40引用:2難度:0.8 -
4.不能說明碳的非金屬性比硅強的是( )
A.同濃度溶液堿性:Na2SiO3>Na2CO3 B.鍵的極性:C-H>Si-H C.高溫下C和SiO2反應生成Si和CO D.SiC中Si是+4價,C是-4價 組卷:27引用:2難度:0.7 -
5.對純堿工業的下列分析,錯誤的是( )
A.氨堿法利用復分解反應制NaHCO3 B.氨堿法利用強堿制弱堿處理母液 C.聯合制堿法利用氧化還原反應處理母液 D.聯合制堿法母液處理后循環利用 組卷:41引用:2難度:0.7 -
6.實驗室制取SO2時,下列裝置能達到實驗目的的是( )
A. 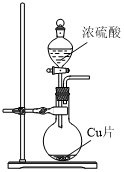
生成SO2B. 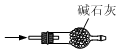
干燥SO2C. 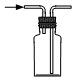
收集SO2D. 
吸收SO2組卷:58引用:4難度:0.5 -
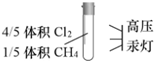 7.如圖所示,試管中裝有用排飽和食鹽水法收集的體積Cl2和45體積CH4,強光照射,充分反應后,試管中不會出現( )15
7.如圖所示,試管中裝有用排飽和食鹽水法收集的體積Cl2和45體積CH4,強光照射,充分反應后,試管中不會出現( )15A.氣體壓強變大 B.氣體顏色變淺 C.白霧 D.液滴 組卷:103引用:2難度:0.7 -
8.下列儀器的有關說法,錯誤的是( )
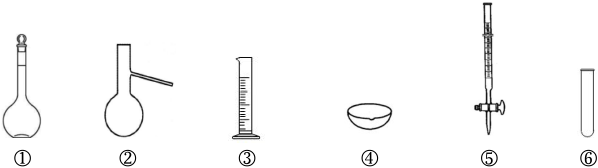
A.①和⑤實驗前需檢漏 B.②④⑥可直接用酒精燈加熱 C.②和④可用于物質提純 D.③和⑤可用于量取液體的體積 組卷:51引用:2難度:0.8
二、綜合題(共60分)
-
23.芳香族化合物F的一種合成路線如圖:
已知:

完成下列填空:
(1)A中官能團的名稱是:。A→B的反應類型是:反應。
(2)W是C的同分異構體,W同時滿足下列條件,任寫一種W結構簡式。。
①含苯環,能發生銀鏡反應;
②分子中不同化學環境的氫原子數目比為3:1:1。
(3)條件X是:(選填選項)
a.H2SO4
b.NaOH
c.Na2CO3
d.(NH4)2SO4
理由是:。
(4)1molE最多能和molH2發生反應。E→F的反應類型是:反應。
(5)利用題中條件,寫出以(CH3)2CHCH2Cl和 為原料制備高分子化合物
為原料制備高分子化合物 的合成路線 (其他無機試劑任選)(合成路線的表示方式為:甲乙…反應條件反應試劑目標產物)。反應條件反應試劑組卷:21引用:3難度:0.3
的合成路線 (其他無機試劑任選)(合成路線的表示方式為:甲乙…反應條件反應試劑目標產物)。反應條件反應試劑組卷:21引用:3難度:0.3 -
24.工業上可用軟錳礦制備硫酸錳。某生產硫酸錳的工藝流程如圖:
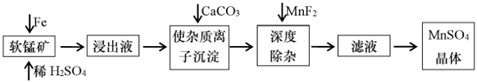
已知:①軟錳礦的主要成分是MnO2,還含有SiO2、CaO、Al2O3、Fe2O3等。
②MnO2在酸性條件下氧化性較強。
③不同金屬離子沉淀的pH
④MnSO4在不同溫度下的溶解度物質 Fe(OH)3 Fe(OH)2 Al(OH)3 Mn(OH)2 開始沉淀 1.9 6.5 3.3 7.7 沉淀完全 3.7 9.7 5.2 9.8
完成下列填空:溫度/℃ 50 80 90 100 溶解度/(g/100g水) 58 48 42 34
(1)軟錳礦與鐵、稀硫酸可能發生的氧化還原反應有:Fe+2H+→Fe2++H2、、。(再寫兩個離子反應方程式)
(2)浸出液中含Fe2+和Fe3+。寫出檢驗浸出液中含Fe2+的方法。。
(3)加入CaCO3之前需加入H2O2,選H2O2的理由是:。
(4)加入MnF2的目的可能是:。
(5)從濾液中獲得MnSO4晶體的方法是:。
(6)在m(H2SO4):n(MnO2)=2.1:1、反應溫度為50℃條件下,探究n(Fe):n(MnO2)對錳浸出率的影響,實驗數據如圖所示。工業上宜選擇n(Fe):n(MnO2)=0.78:1,請結合圖象說明原因。。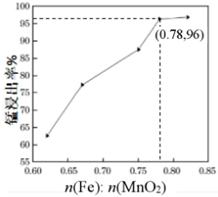 組卷:55引用:2難度:0.5
組卷:55引用:2難度:0.5


