2021-2022學年江蘇省揚州市江都三中九年級(上)期中化學試卷
發布:2024/4/20 14:35:0
一、單項選擇題(每小題2分,每題只有一個選項符合題意,共40分)
-
1.2021年世界環境日的主題是“人人參與,創建有機家園”。下列做法不符合這一主題的是( )
A.大量使用化肥農藥,提高糧食產量 B.生活垃圾分類回收,垃圾資源化 C.低碳生活,綠色出行 D.開展污水共治,保護水資源 組卷:32引用:4難度:0.7 -
2.下列物質由分子構成的是( )
A.氯化鈉 B.氨氣 C.金剛石 D.水銀 組卷:15引用:4難度:0.6 -
 3.全硼富勒烯團簇(B40)的分子結構像中國紅燈籠(如圖)。B40屬于( )
3.全硼富勒烯團簇(B40)的分子結構像中國紅燈籠(如圖)。B40屬于( )A.單質 B.氧化物 C.混合物 D.化合物 組卷:307引用:12難度:0.8 -
4.下列有關實驗現象的描述中,正確的是( )
A.電解水實驗中正極與負極產生的氣體體積之比為2:1 B.木炭在氧氣中燃燒發白光,放出熱量,生成二氧化碳 C.鐵絲在空氣中劇烈燃燒,火星四射,放出熱量,生成黑色固體 D.硫粉在氧氣中燃燒發出藍紫色火焰,放出熱量,生成有刺激性氣味的氣體 組卷:19引用:2難度:0.5 -
5.地殼中含量最多的金屬元素是( )
A.氧 B.硅 C.鋁 D.鐵 組卷:2157引用:386難度:0.9 -
6.氮化鍶(Sr3N2)是生產高端熒光粉的主要原料。已知Sr3N2中N的化合價為-3,則Sr的化合價為( )
A.-3 B.+3 C.+2 D.-2 組卷:589引用:23難度:0.5 -
7.下列安全圖標中,表示“禁止燃放鞭炮”的是( )
A. 
B. 
C. 
D.  組卷:63引用:16難度:0.8
組卷:63引用:16難度:0.8 -
8.下列化學用語正確的是( )
A.2個氫原子:H2 B.兩個硝酸根離子:2NO3 C.3個二氧化硫分子:3SO2 D.鐵離子:Fe2+ 組卷:8引用:1難度:0.5
二、填空題(共5題,滿分60分)
-
 24.閱讀下列科普短文,回答問題。
24.閱讀下列科普短文,回答問題。
碳捕捉與封存技術
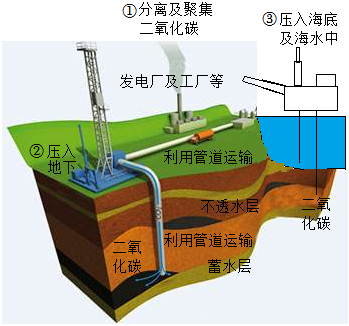
“碳捕捉與封存”是我國的一項先進技術(如圖所示)。
我國能源消耗的70%來自于煤炭。每秒有100噸煤在燃燒,年消耗量超過30億噸。
如果任由煤炭資源在諸多領域利用,將對大氣、河流、土地產生污染,溫室效應增強。實現節能減排、綠色環保,我國政府舉全國之力,積極倡導并大力發展新的綠色經濟。比如:電廠中的煤在極高的溫度下充分燃燒,會產生大量的CO2,每年的排放量大約1600萬噸,運用“碳捕捉與封存”技術,這些CO2將不會進入大氣。被封存的CO2有許多用途,如用于食品保鮮、氣體肥料、冷藏食物、物品滅火等,以此來消除資源的巨大浪費。我國正以超世界一流的目光發展經濟,完善環保體制。
(1)二氧化碳由(填微粒的名稱)構成。檢驗二氧化碳的試劑是,反應的化學方程式。
(2)“碳捕捉與封存”技術有利于控制的增強。“碳捕捉與封存”技術的先進之處是。
(3)將分離聚集的CO2壓入地下的過程中,分子間空隙會(填“變大”或“變小”),將CO2封入蓄水層中發生反應的化學方程式為。
(4)對CO2氣體加壓、降溫可獲得固態二氧化碳,俗名,常用于冷藏食物,用于冷藏食物的原理是。
(5)二氧化碳常用于滅火,但活潑金屬鎂著火不能用二氧化碳滅火,原因是鎂在二氧化碳中能燃燒生成黑色固體碳和白色固體氧化鎂,寫出該反應的化學方程式。組卷:33引用:2難度:0.7 -
25.“富氧空氣”是指氧氣含量高于普通空氣的氣體,可用于航天、醫療、煉鋼等。在“新型肺炎”重癥患者的治療上有一個重要環節為“高流氧呼吸”,其本質和“富氧空氣”差不多,化學興趣小組欲混制“富氧空氣”并開展相關探究,進行以下實驗。
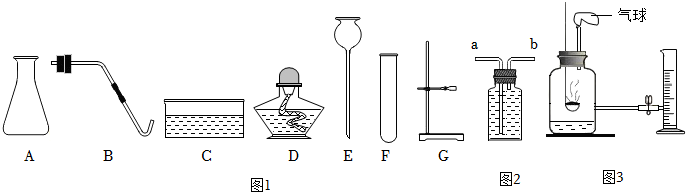
實驗一:混制“富氧空氣”。
(1)寫出圖1中相關儀器的名稱:A;E。
(2)實驗室用高錳酸鉀制取氧氣,反應的化學方程式為,該反應的基本反應類型是,組裝發生裝置所需的儀器(選填字母)。
(3)如圖2,用純氮氣及上述實驗制取的氧氣,混制一瓶(集氣瓶容積為250mL)氧氣體積分數為40%的“富氧空氣”,氣體應從裝置中的管(選“a”或“b”)通入,先通入氮氣排出120mL水,再通入氧氣排出mL水。
實驗二:測定“富氧空氣”中氧氣的含量
用圖3裝置測定“富氧空氣”中氧氣的含量(集氣瓶中“富氧空氣”體積為100mL,底部殘留少量水,燃燒匙內有足量紅磷),操作如下。
①往量筒內加入適量水,讀出量筒內水的體積為V1mL;
②用電點火裝置點燃紅磷,充分反應;
③打開止水夾,待右側量筒內液面不再變化時,排出氣球中的氣體,調節兩邊液面在同一水平面上,讀出量筒內水的體積為V2mL。
回答以下問題:
(1)實驗前,先檢查裝置氣密性:關閉彈簧夾,兩手緊握集氣瓶。過一會兒,若觀察到,證明裝置不漏氣。
(2)用化學方程式表示出操作Ⅱ中紅磷燃燒發生的化學反應:。
(3)本次實驗測得“富氧空氣”中氧氣的含量為。(用含V1、V2的式子表示)。
(4)若讀取V1時仰視,讀取V2時俯視,則測得實驗結果。(選填“偏大”、“偏小”或“無影響”)。
實驗三:研究“富氧空氣”的應用
通過重油、褐煤在氧氣含量不同的空氣中燃燒的實驗,得到有關數據如圖:
(1)結合圖4,說明空氣中氧氣含量與燃燒產生的溫度的關系:。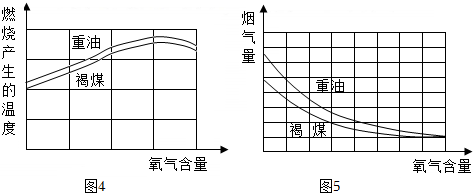
(2)結合圖5,簡述減少燃料燃燒尾氣污染的措施:。
實驗四:空氣中氧氣含量的再探究
化學興趣小組想探究用不同物質在空氣中燃燒測定氧氣含量方法的優劣。他們用足量的蠟燭、紅磷和白磷分別在相同體積與狀態的空氣中燃燒,用氧氣探測器測定密閉容器中剩余氧氣與時間的關系如圖。下列說法正確的是。(填字母)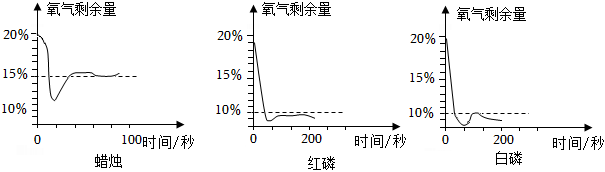
A.測定空氣中氧氣含量效果最好的是蠟燭,因為它反應速率快
B.該實驗證明氧氣的濃度較低時,紅磷與白磷還能與之發生反應
C.三個實驗中均為氧氣過量
D.若用這三種物質做實驗,測得空氣中氧氣含量偏高組卷:55引用:3難度:0.6


