2020-2021學年江西省南昌市南昌縣蓮塘二中高三(上)月考化學試卷(1月份)
發布:2024/12/18 12:30:2
一、單項選擇題(18個小題,每題3分,共54分)
-
1.2019年江西南昌“海昏侯墓”出土了一件青銅白酒蒸餾器。下列說法不正確的是( )
A.古代常用明礬水除去銅器表面的銅綠 B.青銅文物和鐵質文物在潮濕的土壤環境中容易發生電化學腐蝕 C.與火法冶銅(以Cu2S為原料)相比,采用濕法冶銅(以CuSO4為原料)的優點是減少環境污染和能源的消耗 D.在實驗室進行蒸餾時,必須使用圓底燒瓶、直形冷凝管、酒精燈、錐形瓶等儀器 組卷:2引用:1難度:0.7 -
2.化學用語是學習化學的重要工具,下列化學用語不正確的是( )
A.二氧化硅的結構式:O=Si=O B.二氧化碳的電子式: 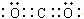
C.過氧化鈉的電子式: 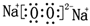
D.Mg2+的結構示意圖: 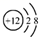 組卷:8引用:1難度:0.7
組卷:8引用:1難度:0.7 -
3.如圖是分離乙酸乙酯、乙酸和乙醇混合物的實驗操作流程圖:
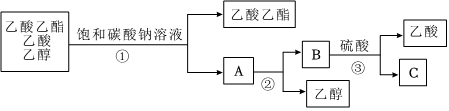
在如圖所示實驗過程中,所涉及的三次分離操作分別是( )A.①蒸餾 ②過濾 ③分液 B.①分液 ②蒸餾 ③蒸餾 C.①蒸餾 ②分液 ③分液 D.①分液 ②蒸餾 ③結晶、過濾 組卷:96引用:20難度:0.7 -
4.下列關于化學平衡的敘述,正確的是( )
A.2NO2(g)?N2O4(g)△H<0,反應達平衡后,壓縮體系體積,平衡正向移動,體系顏色變淺 B.H2(g)+I2(g)?2HI(g)△H<0,反應達平衡后,增大體系體積,平衡不移動,體系顏色不變 C.FeCl3(aq)+3KSCN(aq)?Fe(SCN)3(aq)+3KCl(aq),反應達平衡后,向體系中加入少量KCl固體,平衡逆向移動,體系顏色變淺 D.N2(g)+3H2(g)?2NH3(g),反應達平衡后,保持體系壓強不變,充入He,平衡逆向移動,體系中NH3的百分含量降低 組卷:86引用:8難度:0.5 -
5.在下列各溶液中,一定能大量共存的離子組是( )
A.有色透明溶液中:Fe2+、Ba2+、[Fe(CN)6]3-、NO3- B.強酸性溶液中:Cu2+、K+、ClO-、SO42- C.含有大量AlO2-的溶液中:K+、Na+、HCO3-、I- D.常溫下水電離的c(H+)為1×10-12mol/L的溶液中:K+、Na+、Cl-、NO3- 組卷:40引用:4難度:0.8 -
6.環扁桃酯具有松弛血管平滑肌,擴張血管的功能,其一種同系物(X)可以發生如圖轉化,下列說法中錯誤的是( )
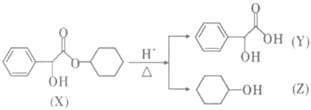
A.X的分子式為C14H18O3 B.Y可以發生氧化反應、加成反應、酯化反應、縮聚反應 C.Y中最多可以有15個原子共平面 D.Z的同分異構體含有醛基有8種 組卷:2引用:1難度:0.5 -
7.主族元素W、X、Y、Z的原子序數依次增加,且均不超過20.W、X、Y最外層電子數之和為15,化合物Z+[Y-W≡X]-是實驗室用于檢驗某常見金屬離子的一種化學試劑。下列說法錯誤的是( )
A.離子半徑大小:Y>Z B.元素X、Z的氫化物遇水均能形成堿性溶液 C.簡單氫化物的沸點:W<X D.[Y-W≡X]-中并不是所有原子最外層均滿足8電子穩定結構 組卷:101引用:3難度:0.5
二、填空題(4小題,共46分)
-
 21.氰化鈉(NaCN)是一種基本化工原料,同時也是一種毒物質。一旦泄漏需要及時處理,一般可以通過噴灑雙氧水或過硫酸鈉(Na2S2O8)溶液來處理,以減少對環境的污染。
21.氰化鈉(NaCN)是一種基本化工原料,同時也是一種毒物質。一旦泄漏需要及時處理,一般可以通過噴灑雙氧水或過硫酸鈉(Na2S2O8)溶液來處理,以減少對環境的污染。
Ⅰ.(1)NaCN溶液呈(填“酸性”、“堿性”或“中性”),NaCN用雙氧水處理后,產生一種酸式鹽和一種能使濕潤的紅色石蕊試紙變藍的氣體,該反應的化學方程式是。
Ⅱ.工業制備過硫酸鈉的反應原理如下所示:
主反應:(NH4)2S2O8+2NaOHNa2S2O8+2NH3↑+2H2O55℃
副反應:2NH3+3Na2S2O8+6NaOH6Na2SO4+N2+6H2O90℃
某化學小組利用上述原理在實驗室制備過硫酸鈉,并用過硫酸鈉溶液處理含氰化鈉的廢水。
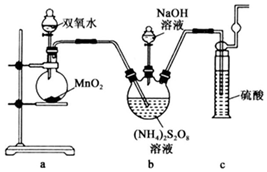
實驗一:實驗室通過如圖所示裝置制備Na2S2O8。
(2)裝置中盛放(NH4)2S2O8溶液的儀器的名稱是。
(3)裝置a中反應產生的氣體需要持續通入裝置c的原因是。
(4)上述裝置中還需補充的實驗儀器或裝置有(填字母代號)。
A.溫度計 B.水浴加熱裝置 C.洗氣瓶 D.環形玻璃攪拌棒
實驗二:測定用過硫酸鈉溶液處理后的廢水中氰化鈉的含量。已知:
①廢水中氰化鈉的最高排放標準為0.50mg/L。
②Ag++2CN-=[Ag(CN)2]-,Ag++I-=AgI↓,AgI呈黃色,CN-優先與Ag+發生反應。實驗如下:取IL處理后的NaCN廢水,濃縮為10.00mL置于錐形瓶中,并滴加幾滴KI溶液作指示劑,用1.0×10-3mol/L的標準AgNO3溶液滴定,消耗AgNO3溶液的體積為5.00mL。
(5)滴定終點的現象是。
(6)處理后的廢水中氰化鈉的濃度為mg/L。
Ⅲ.(7)利用電化學原理,用惰性電極電解飽和NaHSO4溶液也可以制備過硫酸鈉。已知在陽極放電的離子主要為HSO4-,則陽極主要的反應式為。組卷:5引用:2難度:0.5 -
22.化合物Ⅰ是合成含六元環甾類化合物的一種中間體。利用Robinson成環反應合成Ⅰ的路線如圖,回答下列問題:
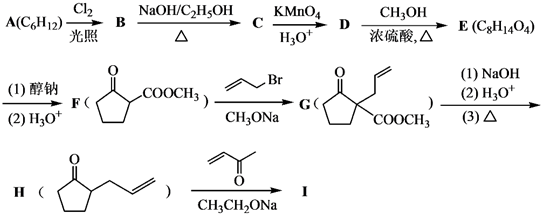
已知:①A是一種環烴,其核磁共振氫譜顯示為單峰:
②R3CH=CHR2R3COOH+R2COOH(R1、R2為烴基)KMnO4H3O+
③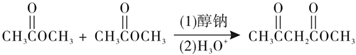
④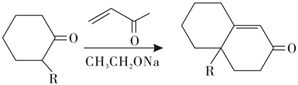
(1)H分子中所含官能團的名稱為。
(2)B→C和F→G的反應類型分別是、。
(3)D→E的反應方程式為。
(4)化合物Ⅰ的結構簡式為。
(5)符合下列條件的G的同分異構體有種。
①苯環上有4個取代基;
②1mol該有機物最多消耗3mol氫氧化鈉。組卷:7引用:1難度:0.5


