蘇教版(2019)必修第二冊《 6.3.1 化學能與電能的轉化》2021年同步練習卷(2)
發布:2024/11/29 7:0:2
一、選擇題
-
1.美國化學家諾塞拉研制出一種可以將水分解成氫氣和氧氣的催化劑,這將使氫氣生產成為可能,并使太陽能使用步入新的時代,被稱為“水發電技術”。下列有關說法正確的是( )
A.“水發電技術”是指水分解生成氫氣和氧氣,同時放出能量來發電 B.“水發電技術”可實現發電過程中的零污染物排放 C.若水分解產生的H2、O2分別通入燃料電池的兩極,通H2的電極上發生還原反應 D.“水發電技術”的能量轉換形式為:化學能→電能→熱能 組卷:8引用:1難度:0.8 -
2.下列裝置能形成原電池的是( )
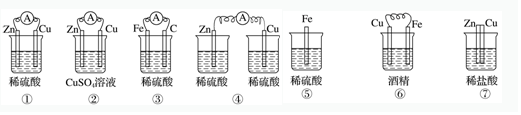
A.①②③⑦ B.①②⑤⑥ C.①②③④ D.①②③⑥⑦ 組卷:106引用:6難度:0.6 -
 3.如圖為一原電池裝置,下列說法錯誤的是( )
3.如圖為一原電池裝置,下列說法錯誤的是( )A.若電解質溶液為稀硫酸,Fe電極上發生反應:Fe-2e-=Fe2+ B.若電解質溶液為濃硝酸,溶液由無色逐漸變為藍色 C.若電解質溶液為飽和食鹽水,Cu電極上有氣體逸出 D.若電解質溶液更換為酒精,電流表指針不偏轉 組卷:8引用:1難度:0.5 -
 4.如圖所示裝置中,觀察到電流計指針偏轉;M棒變粗;N棒變細,由此判斷表中所列M、N、P物質,其中與實驗現象相符的是( )
4.如圖所示裝置中,觀察到電流計指針偏轉;M棒變粗;N棒變細,由此判斷表中所列M、N、P物質,其中與實驗現象相符的是( )
M N P A Zn Cu NaOH溶液 B Cu Fe 稀鹽酸 C Ag Zn AgNO3溶液 D Al Fe CuSO4溶液 A.A B.B C.C D.D 組卷:21引用:3難度:0.7 -
5.某原電池工作時總的反應為Zn+Cu2+=Zn2++Cu,該原電池的組成可能是( )
選項 正極 負極 電解質溶液 A Zn Cu CuCl2溶液 B Cu Zn 稀H2SO4 C Cu Zn CuSO4溶液 D Fe Zn ZnSO4溶液 A.A B.B C.C D.D 組卷:17引用:1難度:0.6 -
6.一種微生物電池可用于污水凈化、海水淡化,其工作原理如圖。下列說法正確的是( )

A.a電極作原電池的正極 B.處理后的硝酸根廢水pH降低 C.電池工作時,中間室的Cl-移向右室,Na+移向左室,實現海水淡化 D.左室發生反應的電極反應式:C6H12O6-24e-+6H2O═6CO2↑+24H+ 組卷:113引用:4難度:0.7
二、實驗題
-
17.某化學興趣小組為了探究鋁電極在原電池中的作用,設計并進行了以下一系列實驗,實驗結果記錄如下.
試根據上表中的實驗現象回答下列問題:編號 電極材料 電解質溶液 電流表指針偏轉方向 1 Al、Mg 稀鹽酸 偏向Al 2 Al、Cu 稀鹽酸 偏向Cu 3 Al、C(石墨) 稀鹽酸 偏向石墨 4 Al、Mg 氫氧化鈉溶液 偏向Mg 5 Al、Zn 濃硝酸 偏向Al
(1)實驗1、2中Al所作的電極(正極或負極)是否相同(填“是”或“否”)?.
(2)對實驗3完成下列填空:
①鋁為極,電極反應式:.
②石墨為極,電極反應式:.
③電池總反應式:.
(3)實驗4中鋁作負極還是正極,理由是.寫出鋁電極的電極反應式:.
(4)解釋實驗5中鋁作正極的原因:.
(5)根據實驗結果總結出影響鋁在原電池中作正極或負極的因素:.組卷:84引用:5難度:0.3
四、原理綜合題
-
18.(1)從能量的變化和反應的快慢等角度研究反應:2H2(g)+O2(g)=2H2O(g)。已知該反應為放熱反應,如圖能正確表示該反應中能量變化的是
。
從斷鍵和成鍵的角度分析上述反應中能量的變化,化學鍵的鍵能如下表所示:
則生成1molH2O(g)可以放出熱量化學鍵 H-H O=O H-O 鍵能(kJ?mol-1) 436 496 463 kJ。
(2)下列反應中,屬于放熱反應的是,屬于吸熱反應的是。
a.鹽酸與燒堿溶液反應
b.Ba(OH)2?8H2O+2NH4Cl=BaCl2+10H2O+2NH3↑
c.氫氣在氧氣中燃燒生成水
d.高溫煅燒石灰石使其分解
e.鋁和鹽酸反應
f.葡萄糖在人體內氧化分解
(3)A、B、C、D四種金屬按下表中裝置進行實驗。
根據實驗現象回答下列問題:裝置 


現象 二價金屬A不斷溶解 C的質量增加 A上有氣體產生
①裝置甲中溶液中的陰離子移向極(填“A”或“B”)。
②裝置乙中正極的電極反應式為。
③四種金屬活動性由強到弱的順序是。組卷:98引用:5難度:0.6


