2021-2022學(xué)年安徽省亳州二中高二(下)期末化學(xué)試卷
發(fā)布:2024/4/20 14:35:0
一、選擇題(16小題,每題3分)每題只有一個選項(xiàng)是正確的。
-
1.做好垃圾分類,推動城市綠色發(fā)展。如表有關(guān)生活垃圾分類不合理的是( )
選項(xiàng) A B C D 生活垃圾 牛奶盒 眼藥水 干電池 西瓜皮 垃圾分類標(biāo)識 



A.A B.B C.C D.D 組卷:41引用:5難度:0.6 -
2.現(xiàn)有四種元素的基態(tài)原子的電子排布式如下:①1s22s22p63s23p4②1s22s22p63s23p3③1s22s22p3④1s22s22p5。則下列有關(guān)比較中正確的是( )
A.第一電離能:④>③>②>① B.原子半徑:④>③>②>① C.電負(fù)性:④>③>②>① D.最高正化合價:④>③=②>① 組卷:559引用:184難度:0.7 -
3.中國宣布了到2030年單位國內(nèi)生產(chǎn)總值CO2排放量比2005年下降60%~65%的減排目標(biāo)。下列措施與這一目標(biāo)無關(guān)的是( )
A.給汽車安裝尾氣處理器 B.自備購物布袋,不用塑料袋 C.使用節(jié)能電器,及時關(guān)閉電器設(shè)備,節(jié)約用電 D.開發(fā)新能源,如太陽能、風(fēng)能等,減少對化石能源的依賴 組卷:34引用:1難度:0.7 -
4.下列敘述正確的是 ( )
A.NH3是極性分子,分子中N原子處在3個H原子所組成的三角形的中心 B.CCl4是非極性分子,分子中C原子處在4個Cl原子所組成的正方形的中心 C.H2O是極性分子,分子中O原子處在2個H原子所連成的直線的中點(diǎn) D.CO2是非極性分子,分子中C原子處在2個O原子所連成的直線的中點(diǎn) 組卷:146引用:7難度:0.5 -
5.防曬霜之所以能有效減輕紫外光對人體的傷害,是因?yàn)樗挠行С煞值姆肿又泻笑墟I,π鍵的電子可在吸收紫外光后被激發(fā),從而阻擋部分紫外光對皮膚的傷害。下列物質(zhì)中沒有防曬效果的是( )
A.氨基苯甲酸(H2N-C6H4-COOH) B.羥基丙酮(HO-CH2-CO-CH3) C.肉桂酸(C6H5CH═CH-COOH) D.乙醇(CH3-CH2-OH) 組卷:46引用:3難度:0.7 -
6.設(shè)NA代表阿伏加德羅常數(shù)的值,下列說法正確的是( )
A.標(biāo)準(zhǔn)狀況下,22.4LCCl4中所含的原子數(shù)目為5NA B.28gN60(分子結(jié)構(gòu)如圖 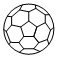 )中含有的N-N鍵數(shù)目為1.5NA
)中含有的N-N鍵數(shù)目為1.5NAC.常溫下,2LpH=12的Na2CO3溶液中含有OH-數(shù)目為0.02NA D.常溫下,將5.6g鐵投入足量的稀硫酸中,充分反應(yīng),轉(zhuǎn)移的電子數(shù)目為0.3NA 組卷:20引用:2難度:0.6
二、非選擇題
-
19.(1)一種銅金合金晶體具有面心立方最密堆積結(jié)構(gòu),在晶胞中Cu原子處于面心,Au原子處于頂點(diǎn),則該合金中Cu原子與Au原子數(shù)量之比為
;該晶體中原子之間的作用力是。
(2)上述晶體具有儲氫功能,氫原子可進(jìn)入由Cu原子與Au原子構(gòu)成的四面體空隙中。若將Cu原子與Au原子等同看待,該晶體儲氫后的晶胞結(jié)構(gòu)與CaF2(如圖1)的結(jié)構(gòu)相似,該晶體儲氫后的化學(xué)式應(yīng)為。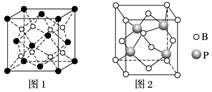
(3)立方BP(磷化硼)的晶胞結(jié)構(gòu)如圖2所示,晶胞中含B原子數(shù)目為。
(4)鐵有δ、γ、α三種同素異形體,γ晶體晶胞中所含有的鐵原子數(shù)為,δ、α兩種晶胞中鐵原子的配位數(shù)之比為。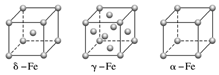
(5)奧氏體是碳溶解在γ-Fe中形成的一種間隙固溶體,無磁性,其晶胞如圖所示,則該物質(zhì)的化學(xué)式為,若晶體密度為ρg/cm3,則晶胞中最近的兩個碳原子的距離為pm(阿伏加德羅常數(shù)的值用NA表示,寫出計(jì)算式即可)。(相對原子質(zhì)量鐵56、碳12)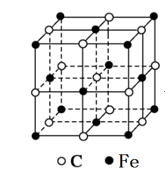 組卷:15引用:2難度:0.5
組卷:15引用:2難度:0.5 -
 20.早期發(fā)現(xiàn)的一種天然二十面體準(zhǔn)晶顆粒由Al、Cu.Fe三種金屬元素組成,回答下列問題:
20.早期發(fā)現(xiàn)的一種天然二十面體準(zhǔn)晶顆粒由Al、Cu.Fe三種金屬元素組成,回答下列問題:
(1)①銅元素位于周期表中區(qū)。Cu2+離子的價層軌道表示式為。
②錳、鐵、鈷三種元素的逐級電離能如表:
鐵元素的第三電離能明顯低于錳元素和鈷元素,其原因是電離能/KJ/mol I1 I2 I 3 I4 Mn 717.3 1509.0 3248 4940 Fe 762.5 1561.9 2957 5290 Co 760.4 1648 3232 4950 。
③實(shí)驗(yàn)室可用赤血鹽K3[Fe(CN)6]檢驗(yàn)Fe2+離子,在赤血鹽中鐵元素的化合價為,中心離子的配位數(shù)為。
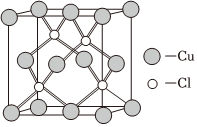
(2)利用反應(yīng):X+C2H2+NH3→Cu2C2+NH4Cl(未配平)可檢驗(yàn)乙炔。
①化合物X晶胞結(jié)構(gòu)如圖,據(jù)此可知X的化學(xué)式為。
②乙炔分子中σ鍵與π鍵數(shù)目之比為,碳原子的雜化方式為;空間構(gòu)型為NH+4(用文字描述)。
(3)①下列三種化合物a。AlCl3 b.NaCl c.Al2O3沸點(diǎn)由高到低依次是(填編號),其原因是。
②Al單質(zhì)中原子采取面心立方最密堆積,其晶胞邊長為0.405nm,列式表示Al單質(zhì)的密度g/cm3(不必計(jì)算出結(jié)果)。組卷:13引用:3難度:0.5


