2022年陜西省安康市漢濱區江北高級中學高考化學第一次模擬試卷
發布:2024/12/2 8:0:28
一、選擇題(本題共10小題,每小題2分,共20分。每小題給出的四個選項中只有一個選項符合要求).
-
1.化學與生活、社會發展息息相關,下列有關說法正確的是( )
A.向牛奶中加入果汁會產生沉淀,這是因為發生了酸堿中和反應 B.將香蕉和青蘋果放在一起,青蘋果更容易成熟,是因為香蕉釋放的乙烯有催熟作用 C.“火神山”醫院地面上鋪的HDPE也稱高密度聚乙烯膜,是一種天然有機高分子化合物 D.二氧化硅是太陽能電池板的主要材料,太陽能替代化石燃料有利于環保 組卷:50引用:4難度:0.6 -
2.反應CO2+2NH3
CO(NH2)2+H2O可應用于工業合成尿素。下列表示反應中相關微粒的化學用語正確的是( )高壓△A.中子數為8的碳原子: C86B.NH3的電子式: 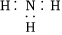
C.氧原子的結構示意圖: 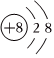
D.CO(NH2)2的結構簡式: 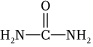 組卷:82引用:6難度:0.7
組卷:82引用:6難度:0.7 -
3.科學家從化肥廠生產的(NH4)2SO4中檢出化學式為N4H4(SO4)2的物質,該物質的晶體中含有SO42-和N4H44+兩種離子,當N4H44+遇到堿性溶液時,會生成N4分子.下列說法正確的是( )
A.14N、N4與N2互為同位素 B.N4H4(SO4)2的電離方程式為N4H4(SO4)2?N4H44++2SO42- C.N4H4(SO4)2不能與草木灰、K3PO4等化肥混合施用 D.N4H4(SO4)2中只含有共價鍵,不含離子鍵 組卷:30引用:10難度:0.9 -
4.化學反應可用微觀示意圖形象化地表示。圖為處理汽車尾氣中的有毒氣體的微觀示意圖(未配平),其中不同符號的球代表不同種原子。下列說法正確的是( )

A.甲和丙中同種元素化合價不可能相等 B.該反應屬于置換反應 C.丁物質一定是非金屬單質 D.乙物質被還原 組卷:16引用:2難度:0.9 -
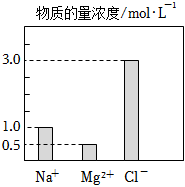 5.在0.1L由NaCl、MgCl2、BaCl2組成的混合溶液中,部分離子濃度大小如圖所示,下列對該溶液成分說法不正確的是( )
5.在0.1L由NaCl、MgCl2、BaCl2組成的混合溶液中,部分離子濃度大小如圖所示,下列對該溶液成分說法不正確的是( )A.NaCl的物質的量為0.1mol B.該混合液中BaCl2的物質的量為0.05mol C.溶質MgCl2的質量為9.5 g D.將該混合液加水稀釋至體積為1 L,稀釋后溶液中的Na+物質的量的濃度為0.1mol/L 組卷:6引用:7難度:0.7 -
6.某澄清透明溶液中,可能大量存在下列離子中的若干種:H+、NH4+、K+、Mg2+、Cu2+、Br-、AlO2-、Cl-、SO42-、CO32-,現進行如下實驗:
①用試管取少量溶液,逐滴加入稀鹽酸至過量,溶液先渾濁后又變澄清,有無色氣體放出。將溶液分為3份。
②在第1份溶液中逐滴加入NaOH溶液至過量,溶液先渾濁后又變澄清。加熱,將濕潤的紅色石蕊試紙置于試管口,未見明顯現象。
③在第2份溶液中加入新制的氯水和CCl4,振蕩后靜置,下層溶液顯橙紅色。
則下列推斷正確的是( )A.溶液中一定有K+、Br-、AlO2-、CO32- B.溶液中一定沒有NH4+、Mg2+、Cu2+、Cl- C.不能確定溶液中是否有K+、Cl-、SO42- D.往第3份溶液中滴加硝酸酸化的硝酸銀溶液可確認是否有Cl- 組卷:143引用:8難度:0.6
三.非選擇題(本題共4小題,共60分)
-
18.某強酸性溶液X,可能含有Al3+、Ba2+、
、Fe2+、Fe3+、NH+4、CO2-3、SO2-4、SiO2-3中的一種或幾種離子,取該溶液進行實驗,其現象及轉化如圖。反應過程中有一種氣體是紅棕色。NO-3
請回答下列問題: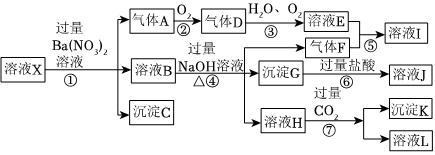
(1)由強酸性條件即可判斷溶液X中一定不存在的離子有。
(2)溶液X中,關于的判斷一定正確的是NO-3。
a.一定有 b.一定沒有 c.可能有
(3)產生氣體A的離子方程式為。
(4)轉化⑥發生反應的現象為。
(5)轉化④中產生H的離子方程式為。
(6)若轉化③中,D、H2O、O2三種物質恰好發生化合反應生成E,則反應中D與O2的物質的量之比為
(7)對不能確定是否存在的離子,可以另取X溶液,加入下列溶液中的一種,根據現象即可判斷,該試劑最好是。
①NaOH溶液,②KSCN溶液,③石蕊試劑,④pH試紙,⑤KMnO4溶液,⑥氯水和KSCN的混合溶液。組卷:98引用:7難度:0.1 -
19.某實驗小組研究KI和酸性KMnO4溶液的反應。
資料:實驗序號 Ⅰ Ⅱ 實驗操作 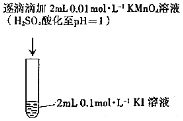

實驗現象 KMnO4溶液的紫色褪去,溶液變為棕黃色 KMnO4紫色溶液迅速變為棕褐色懸濁液,然后沉淀消失,溶液變為棕黃色
ⅰ.MnO4-在酸性條件下最終被還原為Mn2+。
ⅱ.酸性條件下氧化性:KMnO4>KIO3>I2。
(1)實驗Ⅰ中溶液呈棕黃色,推測生成了。
(2)實驗小組繼續對實驗Ⅱ反應中初始階段的產物成分進行探究: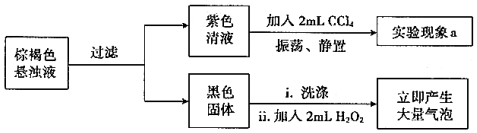
①經檢驗,實驗Ⅱ初始階段I-的氧化產物不是I2,則“實驗現象a”為。
②黑色固體是。
③經檢驗,在“紫色清液”中存在IO3-.下列實驗方案中,可用于檢驗“紫色清液”中IO3-的是(填寫編號)。
A.用潔凈的玻璃棒蘸取“紫色清液”滴在淀粉-碘化鉀試紙上,觀察試紙是否變藍色。
B.取少量“紫色清液”于試管中,向其中加入幾滴淀粉溶液,溶液不變藍,再加入NaHSO3溶液,若試管中溶液變藍色,則“紫色清液”中存在IO3-。
C.取少量“紫色清液”于試管中,向其中加入稀硝酸酸化,再加入幾滴硝酸銀溶液,觀察是否生成黃色沉淀。
④寫出在“紫色清液“中生成IO3-的離子方程式為。
(3)探究實驗Ⅱ中棕褐色沉淀消失的原因。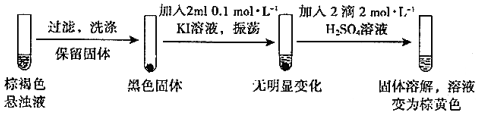
用離子方程式解釋實驗Ⅱ中棕褐色沉淀消失的原因:。
(4)實驗后的反思:導致實驗Ⅰ和實驗Ⅱ中KI和酸性KMnO4溶液反應產物變化的因素是(寫出兩點):、。組卷:34引用:2難度:0.6


