2014-2015學年四川省樂山外國語學校高二(上)周練化學試卷(2)
發布:2024/4/20 14:35:0
一、選擇題:(每題只有一個正確答案,每題3分,共48分)
-
1.1869年,俄國化學家門捷列夫制作出了第一張元素周期表,揭示了化學元素間的內在聯系,成為化學發展史上的重要里程碑之一.下列有關我們常用的元素周期表的說法正確的是( )
A.元素周期表有七個橫行,也是七個周期 B.元素周期表有18個縱行,即有18個族 C.短周期是指第一、二、三、四周期 D.ⅠA族的元素全部是金屬元素 組卷:62引用:15難度:0.7 -
2.近幾年,我國的航天事業成就斐然,“神舟六號”載人飛船已發射成功,“嫦娥”探月工程也在穩步進行中.據科學家預測,月球的土壤中吸附著數百萬噸的3He,每百噸3He核聚變所釋放出的能量相當于目前人類一年消耗的能量.在地球上,該元素主要以4He的形式存在.下列說法正確的是( )
A.4He原子核內含有4個質子 B.3He和4He互為同位素 C.3He原子核內含有3個中子 D.4He的最外層電子數為2,所以4He具有較強的金屬性 組卷:32引用:11難度:0.9 -
3.元素周期表和元素周期律是學習化學的重要工具,可以幫助我們推測元素及其化合物的結構和性質.某元素的原子序數為7,下列有關該元素的推斷不正確的是( )
A.它處于元素周期表中第二周期VA族 B.它的最高正價為+5,負價為-3 C.它的最高價氧化物對應水化物是一種強酸 D.它的非金屬性比磷弱比氧強 組卷:26引用:5難度:0.9 -
4.化學反應進行的快慢可以用“化學反應速率”來衡量.在某一化學反應中,反應物B的濃度在20s內從1.0
mol?L-1變成0.2mol?L-1,則在這20s內以B物質表示的化學反應速率為( )A.0.08mol?L-1?s-1 B.0.04mol?L-1?s-1 C.0.8mol?L-1?s-1 D.0.04mol?L-1 組卷:14引用:4難度:0.9 -
5.某同學在探究原電池形成的條件時,設計了如下實驗裝置,其中燒杯中盛放的都是稀H2SO4,你認為能形成原電池的是( )
A. 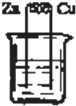
B. 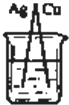
C. 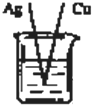
D. 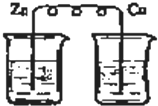 組卷:3引用:3難度:0.9
組卷:3引用:3難度:0.9 -
6.我國的東部經濟發達,但能源緊缺,已經啟動的“西氣東輸”,就是改善東部地區能源緊缺狀況、開發大西北的一項重大工程.這里的“西氣”是指( )
A.煤氣 B.天然氣 C.液化氣 D.乙烯氣 組卷:14引用:4難度:0.9 -
7.在“西氣東輸”工程全線貫通的同時,珠江三角洲,特別是佛山、深圳等地的LNG管道工程也如火如荼,通過該工程,大佛山將在2010年全面采用與“西氣”成分相同的燃料作為居民用氣.如果通過改造現有以液化石油氣(主要成分為C3H8)為燃料的爐具,使其改燒“西氣”并與燃燒液化石油氣達到同樣的效果,若在“燃料氣”進氣口不變的前提下,則需要把空氣的進氣量( )
A.減小 B.增大 C.維持不變 D.不能確定 組卷:53引用:1難度:0.7
二、非選擇題:(共52分)
-
21.各大媒體紛紛報道:根據美國最新研究,數十種牙膏、洗手液、洗潔精等抗菌清潔用品,當中包括高露潔等牌子的產品,含有三氯生(triclosan)的化學物質,該物質與經氯消毒的自來水接觸后會產生“哥羅芳”,長期使用可致癌.已知三氯生中含碳的質量分數為49.75%,含氫的質量分數為2.42%,此外1個三氯生分子里含有2個氧原子和3個氯原子,且0.5mol三氯生的質量為144.75g,則
(1)三氯生的相對分子質量為;
(2)三氯生的分子式為.組卷:31引用:2難度:0.5 -
22.化學在自然資源開發和利用中具有十分重要的意義和作用,如對于金屬礦物的冶煉就是其中一個重要方面.某研究性學習小組在實驗室利用磁鐵礦石(主要成分為Fe3O4)研究金屬的冶煉.請你幫助計算或分析實驗中存在的有關問題.
(1)計算:磁鐵礦石中Fe3O4的質量分數為76.0%,SiO2的質量分數為11.0%,其余均為不含鐵的易溶于水的雜質,若要冶煉出5g鐵,需要這種礦石多少克?
(2)同學們稱好所需質量的礦石后,老師建議他們在冶煉前,先除去礦石中的雜質,以提高礦石中有用成分的含量.請你幫他們設計一個簡單的實驗方案除去礦石中存在的雜質.
(3)實驗室常用CO、H2等作還原劑來煉鐵,同學們經過討論后,決定采用H2作還原劑來煉鐵,你認為他們不采用CO作還原劑的原因可能是什么?
(4)做好準備工作后,同學們開始用H2還原磁鐵礦石.實驗中發現反應速率比較慢.請你寫出反應的化學方程式,并提出兩項能加快該反應速率的措施.組卷:14引用:1難度:0.1


