2023-2024學年福建省福州市延安中學高三(上)期中化學試卷
發布:2024/10/23 12:0:1
一、選擇題(本題共13小題,每小題3分,共39分。每小題只有一個選項符合題意)。
-
1.神舟十四號順利發射、“天宮課堂”如期開講及“華龍一號”核電海外投產等,均展示了我國科技發展的巨大成就。下列相關敘述正確的是( )
A.“泡騰片實驗”中,檸檬酸與小蘇打反應時,有電子的轉移 B.“五環實驗”中,向1.0mol?L-1乙酸中滴甲基橙后變成紅色 C.飛船返回艙表層材料中的玻璃纖維屬于天然有機高分子 D.核電站反應堆所用鈾棒中含有的 U和23597U互為同系物23892組卷:8引用:5難度:0.7 -
2.在指定條件下,下列各組離子一定能大量共存的是( )
A.滴加甲基橙試劑顯紅色的溶液中:Na+、Fe2+、Cl-、NO3- B.滴入KSCN溶液顯血紅色的溶液中:NH4+、Mg2+、SO42-、Cl- C. =1012的溶液中:NH4+、Al3+、NO3-、CO32-c(OH-)c(H+)D.由水電離的c(H+)=1.0×10-13mol?L-1的溶液中:K+、NH4+、AlO2-、HCO3- 組卷:15引用:2難度:0.6 -
3.NA為阿伏加德羅常數的值。下列說法正確的是( )
A.2molNO與1molO2在密閉容器中充分反應后的分子數小于2NA B.0.1mol?L-1AlCl3溶液中,含有Al3+的數目小于0.1NA C.標準狀況下,11.2LSO3所含的分子數為0.5NA D.1molCl2與足量KOH溶液反應生成KClO3轉移的電子數為NA 組卷:13引用:3難度:0.7 -
4.能正確表示下列反應的離子方程式為( )
A.硫化亞鐵和過量硝酸混合:FeS+2H+=Fe2++H2S↑ B.向FeI2溶液中通入等物質的量的Cl2:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl- C.Na2CO3溶液中通入少量SO2; +2SO2+H2O=2CO2-3+CO2HSO-3D.等物質的量濃度的Ba(OH)2和NH4HSO4溶液以體積比1:2混合:Ba2++2OH-+2H++ =BaSO4↓+2H2OSO2-4組卷:99引用:3難度:0.5 -
5.染料木黃酮的結構如圖,下列說法正確的是( )
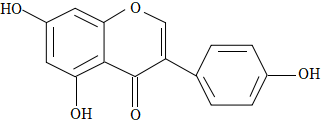
A.分子中存在3種官能團 B.可與HBr反應 C.1mol該物質與足量溴水反應,最多可消耗4molBr2 D.1mol該物質與足量NaOH溶液反應,最多可消耗2molNaOH 組卷:594引用:8難度:0.7
二、非選擇題(本題共4小題,共61分)。
-
16.某小組欲探究反應2Fe2++I2?2Fe3++2I-,完成如下實驗:
資料:如圖1,AgI是黃色固體,不溶于稀硝酸。新制的AgI見光會少量分解。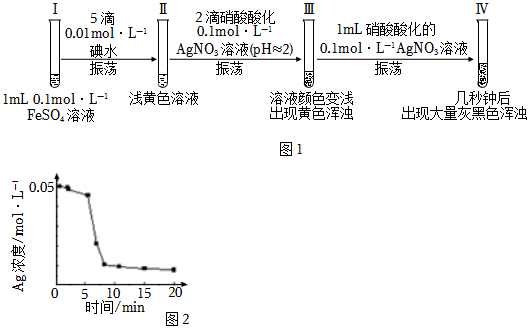
(1)Ⅰ、Ⅱ均未檢出Fe3+,檢驗Ⅱ中有無Fe3+的實驗操作及現象是:取少量Ⅱ中溶液,。
(2)Ⅲ中的黃色渾濁是。
(3)經檢驗,Ⅱ→Ⅲ的過程中產生了Fe3+。
①對Fe3+產生的原因做出如下假設:
假設a:空氣中存在O2,由于(用離子方程式表示),可產生Fe3+;
假設b:溶液中Ag+具有氧化性,可產生Fe3+;
假設c:;
假設d:該條件下,I2溶液可將Fe2+氧化為Fe3+。
②通過實驗進一步證實a、b、c不是產生Fe3+的主要原因,假設d成立。Ⅱ→Ⅲ的過程中I2溶液氧化Fe2+的原因是。
(4)經檢驗,Ⅳ中灰黑色渾濁中含有AgI和Ag。
①驗證灰黑色渾濁含有Ag的實驗操作及現象是:取洗凈后的灰黑色固體,。
②為探究Ⅲ→Ⅳ出現灰黑色渾濁的原因,完成了實驗1和實驗2。
實驗1:向1mL0.1mol?L-1FeSO4溶液中加入1mL0.1mol?L-1AgNO3溶液,開始時,溶液無明顯變化。幾分鐘后,出現大量灰黑色渾濁。反應過程中溫度幾乎無變化。測定溶液中Ag+濃度隨反應時間的變化如圖2。
實驗2:實驗開始時,先向試管中加入幾滴Fe2(SO4)3溶液,重復實驗1,實驗結果與實驗1相同。
ⅰ.實驗1中發生反應的離子方程式是。
ⅱ.Ⅳ中迅速出現灰黑色渾濁的可能的原因是。組卷:99引用:9難度:0.6 -
17.?吸入氧氣、排出二氧化碳,這看似再簡單不過的新陳代謝,在遙遠的太空中卻并不容易,因為在航天服、航天器、空間站等密閉系統中,CO2濃度會高得多,而超過一定濃度會導致呼吸急促、頭暈頭痛、昏迷甚至死亡,因此必須通過一定方法將CO2清除。
Ⅰ.非再生式氫氧化鋰(LiOH)除碳技術
(1)我國“飛天”艙外航天服采用非再生式氫氧化鋰(LiOH)吸附CO2生成碳酸鋰,該技術設備操作簡單,功能可靠,適用于短期出艙任務。吸附時發生反應的化學方程式為。采用LiOH而不用NaOH的原因是。
Ⅱ.再生式快速循環胺技術
(2)以固態胺作為吸附劑,吸附CO2與水蒸氣。當固態胺吸附飽和后,將其暴露于真空中,破壞碳酸氫鹽的化學鍵,釋放出CO2,從而完成吸附劑的再生。該技術大大提升了艙外航天服的續航時間。固態胺的吸附是變化(填“物理”或“化學”)。
Ⅲ.薩巴蒂爾(Sabatier)除碳生氧技術
(3)利用薩巴蒂爾(Sabatier)反應清除二氧化碳并再生氧氣的大體流程如圖所示。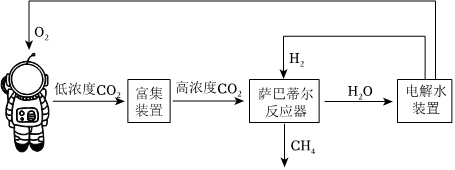
下列說法錯誤的是。
A.CO2的最終產物為CH4和O2
B.電解水裝置中,反應物的能量低于生成物的能量
C.薩巴蒂爾反應器中反應的氧化劑與還原劑質量之比為11:1
D.物質轉化中O、H原子的利用率均為100%
Ⅳ.富集CO2的原電池模擬裝置如圖: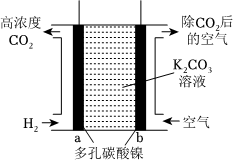
(4)b極為極,a電極上發生的電極反應為。
(5)上述電極材料采用多孔碳載鎳,“多孔”的優點是。
(6)該裝置若消耗2molH2,則理論上在b極除去CO2的質量為。
Ⅴ.能量存儲與循環技術
(7)將電解水裝置與燃料電池配合使用,可實現充放電的循環過程,應用于長壽命的航天器中,工作原理如圖: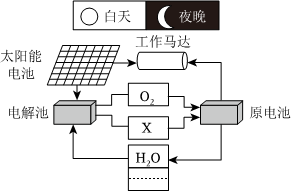
關于該循環系統下列說法正確的是。
A.該系統中存在著太陽能、電能、化學能和機械能之間的相互轉化
B.電解池中可選用CuSO4來增強水的導電性
C.太陽能電池帆板的主要成分為SiO2
D.利用太陽能代替化石能源符合“低碳經濟”組卷:16引用:1難度:0.5


