2021-2022學年湖南省長沙市岳麓區湖南大學附中九年級(上)期中化學試卷
發布:2024/4/20 14:35:0
一、單選題(本大題共12小題,每小題3分,共36分,每小題只有一個選項符合題意)
-
1.下列說法屬于物理變化的是( )
A.破釜沉舟 B.緩慢氧化 C.死灰復燃 D.鉆木取火 組卷:17引用:1難度:0.8 -
2.下列選項中不屬于化學研究范圍的是( )
A.研發氫能源 B.合成新材料 C.用石油生產化工原料 D.編寫電腦程序 組卷:17引用:2難度:0.8 -
3.下列實驗操作或裝置不正確的是( )
A. 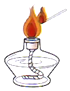
點燃酒精燈B. 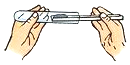
送入固體粉末C. 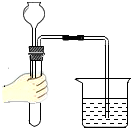
檢查裝置的氣密性D. 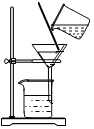
過濾組卷:19引用:4難度:0.7 -
4.下列有關空氣的說法中,正確的是( )
A.空氣中氮氣所占的質量分數為78% B.空氣中二氧化碳能造成溫室效應,對人類是無益的 C.空氣中分離出的氮氣,可作食品保護氣 D.空氣質量報告中所列的空氣質量級別數值越大,說明空氣質量越好 組卷:60引用:4難度:0.8 -
5.下列物質在空氣中燃燒,實驗現象描述正確的是( )
A.木炭:產生紅色火焰 B.紅磷:產生黃色火焰和大量白霧 C.硫粉:產生明亮的藍紫色火焰 D.硫粉:產生微弱的淡藍色火焰 組卷:9引用:1難度:0.5 -
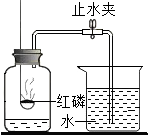 6.某同學用如圖所示裝置測定空氣中氧氣的含量。實驗時,連接好裝置并檢查裝置氣密性后再進行后續操作。下列說法不正確的是( )
6.某同學用如圖所示裝置測定空氣中氧氣的含量。實驗時,連接好裝置并檢查裝置氣密性后再進行后續操作。下列說法不正確的是( )A.紅磷要過量,以保證集氣瓶內空氣中的氧氣能充分反應 B.點燃紅磷后,應迅速地把燃燒匙伸入瓶內并塞緊橡皮塞 C.紅磷熄滅后,要等到裝置冷卻到室溫后再打開止水夾 D.把紅磷換成燃燒的木炭,能夠更精確地測定空氣中氧氣的含量 組卷:184引用:6難度:0.5 -
7.下列各物質的變化中,不屬于化合反應的是( )
A.生石灰+水→熟石灰 B.乙炔+氧氣 水+二氧化碳點燃C.汞+氧氣 氧化汞加熱D.銅+氧氣 氧化銅加熱組卷:10引用:2難度:0.7 -
8.宏觀辨識與微觀探析是化學學科核心素養之一,下表中對宏觀事實的微觀解釋,不合理的是( )
選項 事實 解釋 A 濕衣服在陽光下比在陰涼處干得快 溫度越高,分子運動速率越快 B 氧氣和液氧都能支持燃燒 同種分子化學性質相同 C 熱脹冷縮 分子的大小隨溫度而改變 D 水在通電條件下,可分解為氧氣和氫氣 化學反應中分子是可分的 A.A B.B C.C D.D 組卷:82引用:3難度:0.6
五、(本題共2小題,每空2分,共20分)
-
23.實驗室用高錳酸鉀制取氧氣,并驗證氧氣的化學性質。
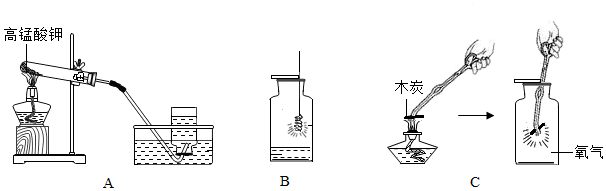
(1)圖A裝置用于高錳酸鉀制取氧氣,發生反應的文字表達式為,用排水法收集氣體,利用的氧氣性質是。
(2)圖A實驗結束,停止加熱前要先把導管移出水面;反之,則會導致水倒吸入試管中。引起倒吸的原因是。
(3)如圖B所示,可觀察到鐵絲在氧氣中劇烈燃燒、,放出大量熱,。該反應的文字表達式為。
(4)圖C可觀察到木炭在氧氣中燃燒,,放熱。木炭在氧氣中燃燒比在空氣中更劇烈的原因是。組卷:479引用:3難度:0.6 -
 24.化學反應速率是衡量化學反應進行快慢的物理量,為了探究影響化學反應速率的因素,以過氧化氫分解為研究對象進行實驗。三個小組均可采用如圖裝置進行實驗,記錄收集10mL氧氣的時間,實驗室可供選擇的試劑有:2%、5%、10%三種濃度的H2O2溶液、MnO2、CuO、紅磚粉末。
24.化學反應速率是衡量化學反應進行快慢的物理量,為了探究影響化學反應速率的因素,以過氧化氫分解為研究對象進行實驗。三個小組均可采用如圖裝置進行實驗,記錄收集10mL氧氣的時間,實驗室可供選擇的試劑有:2%、5%、10%三種濃度的H2O2溶液、MnO2、CuO、紅磚粉末。
A組:探究催化劑對化學反應速率的影響取5mL10%H2O2溶液,三次實驗分別加入1gMnO2、紅磚粉末、CuO進行實驗,記錄數據如下:
由此可出結論:MnO2、CuO對H2O2分解有催化作用,紅磚粉末無催化作用,某同學對該結論提出疑問。補充對比實驗,操作為試 劑 ①MnO2 ②紅磚粉末 ③CuO t/s 10 60 20 。
結果:長時間(大于100s),收集到很少量氣體。
更正結論:紅磚粉末(選填“有”、“無”)催化作用,三者中催化效率最高,寫出用試劑③催化分解過氧化氫的符號表達式:。
B組:探究反應物濃度對化學反應速率的影響
甲同學:取10mL5% H2O2溶液,加入1gMnO2為催化劑,進行實驗,記錄時間t1。
乙同學:取10mL2% H2O2溶液,加入1gCuO為催化劑,進行實驗,記錄時間t2。
實驗結果:t1t2。
結論:濃度越大,反應速率越快。
丙同學:對實驗設計提出疑問,并補充實驗:,記錄時間t3,且t1<t3<t2。
更正結論為:當時,反應物濃度越大,反應速率越快。
C組:探究對化學反應速率的影響。
均取10mL5% H2O2溶液和1gCuO為催化劑進行兩次實驗,分別將試管置于冰水浴和50℃熱水浴記錄時間t4、t5,且t4>t5。
結論:當反應物濃度和催化劑相同時,。
綜上所述:為了研究某一因素對化學反應速率的影響,必須。組卷:70引用:3難度:0.5


