2020年北京市東城區高考化學二模試卷
發布:2024/11/16 20:0:1
一、第一部分(選擇題共42分)本部分共14小題,每小題3分,共42分.在每小題列出的4個選項中,選出最符合題目要求的一項.
-
1.下列自然現象發生或形成的過程中,指定元素既沒有被氧化又沒有被還原的是( )




A.溶洞--鈣 B.閃電--氮 C.火山噴發--硫 D.光合作用--碳 A.A B.B C.C D.D 組卷:40引用:2難度:0.8 -
2.下列說法不正確的是( )
A.乙二醇的沸點比乙醇的沸點高 B.淀粉和蔗糖水解的最終產物中均含有葡萄糖 C.植物油通過催化加氫可轉變為半固態的脂肪 D.硫酸銨或氯化鈉溶液都能使蛋白質發生變性 組卷:142引用:3難度:0.6 -
3.下列離子方程式正確的是( )
A.溴化亞鐵溶液中通入過量氯氣:2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl- B.硫酸中加入少量氫氧化鋇溶液:H++SO42-+Ba2++OH-═BaSO4↓+H2O C.苯酚鈉溶液中通入少量二氧化碳:2C6H5O-+CO2+H2O→2C6H5OH+CO32- D.硝酸銀溶液中加入過量氨水:Ag++NH3?H2O═AgOH↓+NH4+ 組卷:95引用:4難度:0.7 -
4.除去下列物質中含有的少量雜質(括號內為雜質),所選試劑不正確的是( )
A.Cl2(HCl):飽和食鹽水、濃硫酸 B.AlCl3溶液(Fe3+):氨水、鹽酸 C.C2H2(H2S):CuSO4溶液、堿石灰 D.NaCl溶液(SO42-):BaCO3、鹽酸 組卷:56引用:2難度:0.5 -
5.關于下列消毒劑的有效成分的分析錯誤的是 ( )
A.雙氧水 B.漂白粉 C.滴露 D.強氯精 有效成分 H2O2 Ca(ClO)2 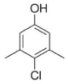
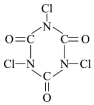
分析 可與NaClO發生反應 可用Cl2與Ca(OH)2制備 分子式為C8H9OCl 分子中有2種環境的碳原子 A.A B.B C.C D.D 組卷:62引用:4難度:0.9 -
6.短周期中8種元素a~h,其原子半徑、最高正化合價或最低負化合價隨原子序數遞增的變化如圖所示。下列判斷不正確的是( )
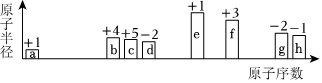
A.a、d、f組成的化合物能溶于強堿溶液 B.a可分別與b或c組成含10個電子的分子 C.e的陽離子與g的陰離子具有相同的電子層結構 D.最高價氧化物對應水化物的酸性:h>g>b 組卷:74引用:4難度:0.5
二、第二部分(綜合題共58分)本部分共5小題,共58分.
-
18.聚酰亞胺是一類非常有前景的可降解膜材料,其中一種膜材料Q的合成路線如圖。
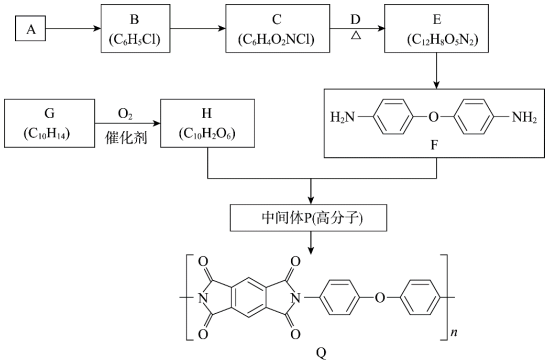
已知:
ⅰ.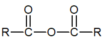 +R′-NH2→
+R′-NH2→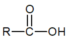 +
+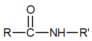
ⅱ.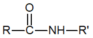 +NaOH→
+NaOH→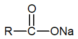 +R′-NH2
+R′-NH2
(1)A是芳香烴,A→B的化學方程式是。
(2)B轉化為C的試劑和條件是。
(3)C中所含的官能團的名稱是。
(4)D可由C與KOH溶液共熱來制備,C與D反應生成E的化學方程式是。
(5)E→F的反應類型是。
(6)G與A互為同系物,核磁共振氫譜有2組峰,G→H的化學方程式是。
(7)H與F生成中間體P的原子利用率為100%,P的結構簡式是(寫一種)。
(8)廢棄的膜材料Q用NaOH溶液處理降解后可回收得到F和(填結構簡式)。組卷:76引用:1難度:0.3 -
19.某小組通過分析鎂與酸反應時pH的變化,探究鎂與醋酸溶液反應的實質。
【實驗】在常溫水浴條件下,進行實驗Ⅰ~Ⅲ,記錄生成氣體體積和溶液pH的變化:
Ⅰ.取0.1g光亮的鎂屑(過量)放入10mL 0.10mol?L-1HCl溶液中。
Ⅱ.取0.1g光亮的鎂屑放入10mL 0.10mol?L-1CH3COOH溶液(pH=2.9)中。
Ⅲ.取0.1g光亮的鎂屑放入10mL pH=2.9 HCl溶液中。
【數據】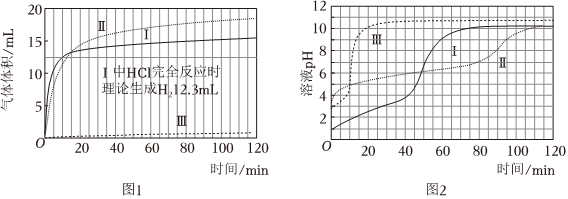
(1)起始階段,Ⅰ中主要反應的離子方程式是。
(2)Ⅱ起始溶液中約為c(CH3COOH)c(H+)。(選填“1”、“10”或“102”)。
(3)起始階段,導致Ⅱ、Ⅲ氣體產生速率差異的主要因素不是c(H+),實驗證據是。
(4)探究Ⅱ的反應速率大于Ⅲ的原因。
提出假設:CH3COOH能直接與Mg反應。
進行實驗Ⅳ:。
得出結論:該假設成立。
(5)探究醋酸溶液中與Mg反應的主要微粒,進行實驗Ⅴ。
與Ⅱ相同的條件和試劑用量,將溶液換成含0.10mol?L-1的CH3COOH與0.10mol?L-1CH3COONa的混合溶液(pH=4.8),氣體產生速率與Ⅱ對比如表。
對比a~c中的微粒濃度,解釋其a與b、a與c氣體產生速率差異的原因:a.實驗Ⅴ起始速率 b.實驗Ⅱ起始速率 c.實驗ⅡpH=4.8時速率 2.1mL?min-1 2.3mL?min-1 0.8mL?min-1 。
(6)綜合以上實驗得出結論:
①鎂與醋酸溶液反應時,CH3COOH、H+、H2O均能與鎂反應產生氫氣。
②。
(7)實驗反思:120min附近,Ⅰ~ⅢpH均基本不變,pH(Ⅰ)≈pH(Ⅱ)<pH(Ⅲ),解釋其原因:。組卷:142引用:3難度:0.5


