2021-2022學年黑龍江省綏化市部分學校高一(上)期末化學試卷
發布:2024/10/28 5:0:2
一、選擇題(本大題共18小題,每小題3分,共計54分。在每小題列出的四個選項中,只有一項是符合題目要求的)
-
1.按照不同的分類標準,H2SO4應屬于( )
①酸
②硫酸鹽
③含氧酸
④混合物
⑤化合物
⑥二元酸A.①②③④ B.①③⑤⑥ C.①②③⑤ D.②③⑤⑥ 組卷:35引用:3難度:0.8 -
2.下列有關膠體的說法錯誤的是( )
A.根據丁達爾效應將分散系分為溶液、濁液和膠體 B.一束平行光線射入蛋白質溶液里,從側面可以看到一條光亮的通路 C.分散質的顆粒介于1~100nm之間的分散系稱為膠體 D.不管是分散質還是分散劑,都可以是固態、液態、氣態中任一狀態 組卷:27引用:2難度:0.8 -
3.下列說法正確的是( )
A.CO2的水溶液能導電,所以CO2是電解質 B.NaHCO3的電離方程式為NaHCO3═Na++H++CO32- C.CaCO3在水中的溶解度很小,所以在離子方程式里不能拆成離子形式 D.中和反應的實質是H+與OH-結合生成水,故中和反應的離子方程式均為H++OH-═H2O 組卷:17引用:3難度:0.6 -
4.下列關于鈉及其化合物的說法正確的是( )
A.將Na2O2投入水中,反應后生成可燃性氣體 B.將Na投入CuSO4溶液中,能得到藍色沉淀 C.Na常溫下在空氣中被氧化為Na2O2 D.將Na久置在空氣中,最終得到一種淡黃色粉末 組卷:45引用:2難度:0.6 -
5.煉鐵的反應原理為:Fe2O3+3CO
3CO2+2Fe,當有2mol Fe生成時,下列說法中,錯誤的是( )高溫A.還原產物為Fe B.該條件下,生成CO2氣體的體積大于67.2L C.轉移的電子數約為7.224×1024個 D.參加反應的Fe2O3和CO物質的量分別為1mol、3mol 組卷:59引用:2難度:0.7 -
6.下列反應的離子方程式正確的是( )
A.向稀鹽酸溶液中加鐵:2Fe+6H+═2Fe3++3H2↑ B.CuSO4溶液與Ba(OH)2溶液反應:Ba2++SO42-═BaSO4↓ C.澄清石灰水中通入過量CO2:2OH-+CO2═CO32-+H2O D.碳酸鈉溶液與足量稀鹽酸的反應:CO32-+2H+═CO2↑+H2O 組卷:8引用:2難度:0.6 -
7.下列各組離子在指定溶液中一定能大量共存的是( )
A.pH=12的無色溶液中:Na+、Al3+、MnO4-、SO42- B.飽和氯水中:Ag+、Fe2+、Br-、NO3- C.0.1mol?L-1NaHSO4溶液中:Na+、Mg2+、Cl-、NO3- D.能溶解氧化鋁的溶液中:K+、Ca2+、Cl-、HCO3- 組卷:6引用:1難度:0.7
二、非選擇題(本題共4小題,共46分)
-
21.組裝如圖所示裝置可用于制備Cl2并驗證其性質(部分夾持儀器已省略)。已知:苯的密度比水的小且難溶于水。回答下列問題:
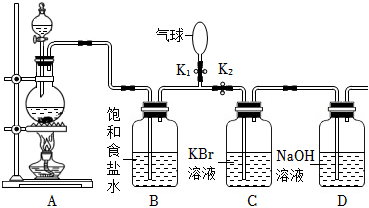
Ⅰ.Cl2的制備
(1)制備氯氣選用的藥品為固體二氧化錳和濃鹽酸,則相關的化學反應方程式為:;裝置B中飽和食鹽水的作用是。
Ⅱ.Cl2的性質
(2)將氯水滴在藍色石蕊試紙上,試紙先變紅后褪色,說明氯水具有(填性質)。
(3)實驗室常用氫氧化鈉溶液吸收多余的Cl2,寫出該反應的離子方程式:。
(4)比較氯、溴、碘單質的氧化性強弱。打開K2,關閉K1,向C中緩緩通入少量氯氣時,離子反應方程式為;當裝置C中溶液剛變為黃色時,(寫出開關操作)。用玻璃棒蘸取少量C中溶液滴在淀粉KI試紙上,觀察到的現象是;說明氯、溴、碘單質的氧化性由強到弱的順序為。組卷:6引用:1難度:0.6 -
22.剛玉在工業上有廣泛的用途,其主要成分為α-氧化鋁。利用鋁灰(主要成分為Al2O3,含少量雜質SO2、FeO、Fe2O3)制備剛的工藝流程如圖:
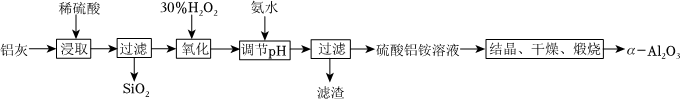
回答下列問題:
(1)鋁灰的所有成分中屬于兩性氧化物的是(填化學式)。
(2)“浸取”時Fe2O3發生反應的化學方程式為。
(3)“氧化”操作中發生的離子反應方程式為。
(4)已知:生成氫氧化物沉淀的pH如下表所示。
用氨水“調節pH”,pH的范圍是氫氧化物 Al(OH)3 Fe(OH)2 Fe(OH)3 開始沉淀時 3.4 6.3 1.5 完全沉淀時 4.7 8.3 2.8 。
(5)寫出濾渣成分的化學式:。組卷:83引用:4難度:0.5


