2020-2021學年云南省昆明市官渡區九年級(上)期末化學試卷
發布:2024/4/20 14:35:0
一、選擇題(本題共20小題,其中第1~15小題每小題2分,第16~20小題每小題2分,滿分45分。每小題只有1個選項符合題意)
-
1.中醫藥文化博大精深,是中華民族智慧的象征。下列中藥傳統制作技藝中主要涉及化學變化的是( )
A.白芍切片 B.研磨珍珠粉 C.厚樸去皮 D.燒制血余炭 組卷:139引用:3難度:0.8 -
2.空氣的成分按體積分數計算,含量最多的是( )
A.氧氣 B.稀有氣體 C.氮氣 D.其他成分 組卷:79引用:1難度:0.9 -
3.玉龍雪山海拔5596米,是國家5A級風景名勝區。為避免出現高原反應,游客進入景區可攜帶便攜式氧氣瓶。氧氣可被壓縮在便攜式氧氣瓶中的原因是( )
A.分子間有間隔 B.分子的質量很小 C.分子在不斷運動 D.分子的體積很小 組卷:16引用:1難度:0.7 -
4.具備基本的實驗技能是進行科學探究的保證。 下列實驗操作正確的是( )
A. 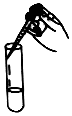
滴加液體B. 
傾倒液體C. 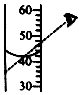
量取液體D. 
加熱液體組卷:29引用:1難度:0.8 -
5.2020年日11月24日,長征五號遙五運載火箭成功發射“嫦娥五號”月球探測器。此次航天任務中用到了我國研制的大尺寸二氧化碲晶體等關鍵材料。二氧化碲(TeO2)中Te的化合價為( )
A.-2 B.+1 C.+2 D.+4 組卷:36引用:2難度:0.6 -
6.下列化學用語中數字“2”表示分子個數的是( )
A.H2 B.2N C.2SO3 D.Cu2+ 組卷:19引用:2難度:0.6 -
7.用化學知識對下列成語進行解釋,不正確的是( )
A.“釜底抽薪”的滅火原理是移除可燃物 B.“煽風點火”的原理是加速空氣的流動補充氧氣 C.“火上澆油”的原理是為燃燒提供了更多的可燃物 D.“鉆木取火”的原理是通過摩擦生熱提高木材的著火點 組卷:29引用:1難度:0.6 -
8.對下列物質燃燒現象的描述正確的是( )
A.紅磷在氧氣中燃燒生成大量的白霧 B.鐵絲在空氣中劇烈燃燒,火星四射 C.硫在空氣中燃燒發出淡藍色火焰 D.木炭在空氣中燃燒生成二氧化碳 組卷:21引用:3難度:0.6 -
9.明代詩人于謙在其詩中寫道“鑿開混沌得烏金,藏蓄陽和意最深。爝火燃回春浩浩,烘爐照破夜沉沉”,詩中所寫的“烏金”主要成分是( )
A.金 B.二氧化錳 C.炭 D.氧化銅 組卷:69引用:3難度:0.6
三、實驗與探究(本題共2小題,化學方程式每空2分,其余每空1分,滿分16分)
-
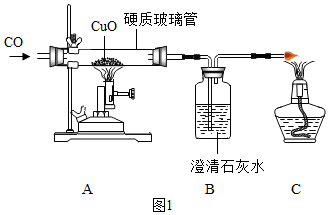
27.某化學興趣小組同學模仿工業冶煉金屬的原理,設計如圖1實驗用CO還原CuO制取金屬銅。加熱一段時間后發現硬質玻璃管內固體不完全是光亮紫紅色,還有部分是鮮紅色。興趣小組同學對此現象進行了分析和探究。
【查閱資料】①Cu2O是鮮紅色固體,Cu是紫紅色固體。
②銅的氧化物有氧化亞銅(Cu2O)和氧化銅兩種。
【實驗分析】上述實驗過程中,還觀察到B裝置中澄清石灰水變渾濁,則A裝置硬質玻璃管中發生反應的化學方程式為,C處酒精燈的作用是。
【提出問題】實驗過程中有Cu2O生成與什么因素有關?
【作出猜想]猜想一:與反應物CuO的堆放方式有關;猜想二:與反應的溫度有關。
【實驗探究】序號 實驗操作 實驗現象 實驗結論 1 取等量的CuO粉末,其中一份堆積在硬質玻璃管內,另一份平鋪在硬質玻璃管內,進行對照實驗 堆積在硬質玻璃管內的固體為鮮紅色,平鋪在硬質玻璃管內的固體為紫紅色 猜想 成立2 另取適量的CuO粉末進行實驗,過程中利用原位X射線粉末進行衍射儀測定不同溫度下反應4小時后的固體物質成分,實驗結果如圖2所示 / 300℃時,固體產物中含有Cu2O和 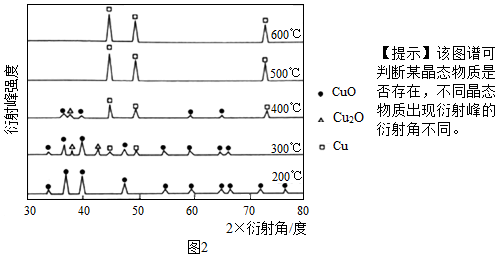
【得出結論】生成Cu2O的因素是多方面的。由圖譜可知,用CO還原CuO欲制取純凈的Cu,反應的溫度應要控制在℃以上。
【反思評價】規范操作和嚴格控制反應條件是保障實驗成功的關鍵。若實驗剛結束就直接將純凈的銅倒在紙上,會觀察到銅表面變黑,生成黑色物質的原因是。組卷:30引用:1難度:0.4
四、分析與計算(本題共1小題,滿分6分)
-
28.硼及其化合物在現代工農業、醫學、國防中有著重要的應用價值。工業上可用鎂與三氧化二硼(B2O3)固體生產硼,反應原理為B2O3+3Mg
2B+3MgO,要生產4.4t的硼。請計算:高溫
(1)理論上需要B2O3的質量是多少?
(2)理論上可以得到MgO的質量是多少?組卷:39引用:2難度:0.6


