人教版(2019)必修第二冊《第六章 化工反應與能量》2020年單元測試卷(1)
發布:2024/4/20 14:35:0
一、單選題
-
1.下列反應中,生成物的總能量大于反應物的總能量的是( )
A.氫氣在氧氣中燃燒 B.焦炭在高溫下與水蒸氣反應 C.硫在氧氣中燃燒 D.鐵絲在氧氣中燃燒 組卷:442引用:24難度:0.9 -
2.反應2SO2+O2?2SO3達到平衡后,再向反應容器中充入含氧的同位素
O的氧氣經過一段時間后,188O原子存在于( )188A.O2 B.SO2 C.O2和SO2 D.O2、SO2和SO3 組卷:146引用:7難度:0.9 -
3.某原電池總反應的離子方程式為:2Fe3++Fe═3Fe2+能實現該反應的原電池是( )
A.正極為Cu,負極為Fe,電解質溶液為FeCl3 B.正極為C,負極是Fe,電解質溶液為FeCl2 C.正極為Fe,負極為Zn,電解質溶液為Fe2(SO4)3 D.正極為Ag,負極為Fe,電解質溶液為CuSO4 組卷:97引用:5難度:0.7 -
4.100℃時,將0.1molN2O4置于1L密閉的燒瓶中,然后將燒瓶放入 100℃的恒溫槽中,燒瓶內的氣體逐漸變為紅棕色:N2O4(g)═2NO2(g)。 下列選項不能說明上述反應在該條件下已經達到平衡狀態的是( )
A.燒瓶內氣體的密度不再變化 B.燒瓶內氣體的顏色不再變化 C.燒瓶內氣體的壓強不再變化 D.燒瓶內氣體的平均相對分子質量不再變化 組卷:33引用:2難度:0.7 -
5.恒容容器內的可逆反應N2+3H2?2NH3,達到限度后,再充入一定量的氮氣,下列敘述不正確的是( )
A.該化學反應的限度發生改變 B.氮氣和氫氣的轉化率都提高 C.氫氣的轉化率提高 D.氮氣的轉化率減低 組卷:13引用:1難度:0.7 -
6.下列說法正確的是( )
A.化學電池的放電過程就是電能轉換為化學能的過程 B.化學電池中電子由正極流出,經外電路流向負極 C.物質燃燒總是放熱的,燃料電池兩極板均發生氧化還原反應 D.燃料電池工作時,通常是將空氣通向正極 組卷:36引用:1難度:0.5 -
7.在一定溫度下,反應A2(g)+B2(g)?2AB(g)達到反應限度的標志是( )
A.容器內的總壓強不隨時間變化 B.單位時間內生成2nmol AB的同時生成nmol B2 C.c(A2):(B2):c(AB)=1:1:2 D.A2和B2的物質的量之和與AB的物質的量相等 組卷:23引用:1難度:0.7
二、填空題
-
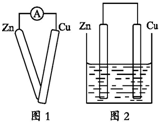 20.某同學在做原電池原理的實驗時,有如下實驗步驟:
20.某同學在做原電池原理的實驗時,有如下實驗步驟:
①用導線將靈敏電流計的兩端分別與純凈的鋅片和銅片相連接(如圖1);
②把一塊純凈的鋅片插入盛有稀硫酸的燒杯中;
③把一塊純凈的銅片插入盛有稀硫酸的燒杯中;
④用導線把鋅片和銅片連接起來后,再平行地插入盛有稀硫酸的燒杯中(如圖2).
回答下列問題:
(1)實驗步驟①中應觀察到的現象是.
(2)實驗步驟②中應觀察到的現象是.
(3)實驗步驟③中應觀察到的現象是.
(4)實驗步驟④中應觀察到的現象是.
(5)通過實驗步驟④該同學頭腦中有了一個猜想(或假設),該猜想是.
(6)為了證實該猜想,該同學又設計了第⑤步實驗,請簡要敘述該同學的實驗原理并畫出第⑤步實驗的裝置示意圖.組卷:27引用:2難度:0.5 -
21.在下列事實中,什么因素影響了化學反應的速率?
(1)集氣瓶中有H2和Cl2的混合氣體,在瓶外點燃鎂條時發生爆炸;
(2)黃鐵礦煅燒時要粉碎成細小的礦粒;
(3)KI晶體和HgCl2晶體混合后無明顯現象,若一起投入水中,很快生成紅色HgI2;
(4)熔化的KClO3放出氣泡很慢,撒入少量MnO2后很快產生氣體;
(5)同濃度、同體積的鹽酸中放入同樣大小的鋅粒和鎂塊,產生氣體的速率有快有慢;
(6)同樣大小的石灰石分別在0.1mol?L-1的鹽酸和1mol?L-1的鹽酸中反應速率不同;
(7)夏天的食品易變霉,冬天就不易發生該現象;
(8)葡萄糖在空氣中燃燒時需要較高的溫度,可是在人體里,在正常體溫(37℃)時,就可以被氧化,這是因為。組卷:28引用:2難度:0.7


