2013-2014學(xué)年北京市高三(上)開學(xué)摸底化學(xué)試卷
發(fā)布:2024/11/17 14:0:2
一、選擇題
-
1.在下列變化過程中,只發(fā)生物理變化的是( )
A.荔枝釀酒 B.酸雨侵蝕建筑物 C.空氣液化制取氮?dú)?/label> D.生石灰遇水成為熟石灰 組卷:33引用:10難度:0.9 -
2.化學(xué)科學(xué)需要借助化學(xué)專用語言描述,下列有關(guān)化學(xué)用語書寫正確的是( )
A.CO2的電子式 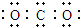
B.Cl-的結(jié)構(gòu)示意圖 
C.HCl的電子式 
D.質(zhì)量數(shù)為37的氯原子 3717Cl組卷:16引用:3難度:0.9 -
3.下列是純凈物的是( )
A.鋁熱劑 B.酒精 C.植物油 D.淀粉 組卷:26引用:3難度:0.9 -
4.將下列各組物質(zhì)按單質(zhì)、氧化物、酸、堿、鹽分類順序排列,其中正確的是( )
A.水銀、干冰、硫酸、燒堿、食鹽 B.碘酒、冰、鹽酸、燒堿、食鹽 C.氫氣、二氧化硫、硝酸、純堿、硫酸銅 D.銅、氧化銅、醋酸、石灰石、氯化銅 組卷:90引用:12難度:0.9 -
5.月球上的主要礦物有輝石[CaMgSi2O6]、斜長石[KAlSi3O8]和橄欖石[(Mg,Fe)2SiO4]等,下列說法或分析錯(cuò)誤的是( )
A.輝石、斜長石及橄欖石均屬于硅酸鹽礦 B.輝石成分中非金屬元素的原子數(shù)是金屬原子數(shù)的4倍 C.斜長石的氧化物形式可表示為K2O?Al2O3?6SiO2 D.橄欖石中鎂、鐵元素的化合價(jià)均為+1 組卷:16引用:2難度:0.9 -
6.科學(xué)家最近研究出一種環(huán)保、安全的儲(chǔ)氫方法,其原理可表示為:儲(chǔ)氫釋氫NaHCO3+H2
HCOONa+H2O下列有關(guān)說法正確的是( )儲(chǔ)氫釋氫A.儲(chǔ)氫、釋氫過程均無能量變化 B.NaHCO3、HCOONa均含有離子鍵和共價(jià)鍵 C.儲(chǔ)氫過程中,NaHCO3被氧化 D.釋氫過程中,每消耗0.1molH2O放出2.24L的H2 組卷:774引用:20難度:0.9 -
7.NA代表阿伏加德羅常數(shù).下列有關(guān)敘述正確的是( )
A.標(biāo)準(zhǔn)狀況下,22.4LH2O含有的分子數(shù)等于0.1NA B.常溫下.100mL 1mol/L Na2CO3溶液中陰離子總數(shù)大于0.1NA C.分子數(shù)為NA的CO、C2H4混合氣體體積約為22.4L,質(zhì)量為28g D.3.4g NH3中含N-H鍵數(shù)目為0.2NA 組卷:331引用:7難度:0.7 -
8.下列說法正確的是( )
A.H、D、T屬于同位素,H2、D2、T2屬于同素異形體 B.氯水、氨水、王水是混合物,鐵粉、漂白粉是純凈物 C.HCl、NH3、BaSO4是電解質(zhì),CO2、Cl2、C2H5OH是非電解質(zhì) D.風(fēng)能、生物質(zhì)能是可再生能源,煤、石油、天然氣是不可再生能源 組卷:554引用:6難度:0.9
三、解答題(共1小題,滿分0分)
-
24.今有一澄清溶液,只可能含有下表中的若干種離子(存在的離子均大量):
現(xiàn)取三份上述澄清溶液各100mL,分別進(jìn)行以下實(shí)驗(yàn):陽離子 K+、NH 、H+、Ba2++4陰離子 Cl-、CO 、SO2-3、OH-2-4
①第一份加入AgNO3溶液有沉淀產(chǎn)生
②第二份加入足量NaOH溶液加熱后,收集到氣體0.04mol
③第三份加入足量BaCl2溶液后,得干燥沉淀6.27g,經(jīng)足量鹽酸洗滌,干燥后,沉淀質(zhì)量為2.33g.
請(qǐng)回答下列問題:
(1)100mL溶液中c(SO)=2-4.
(2)第二份加入NaOH溶液產(chǎn)生氣體的離子方程式
(3)6.27g沉淀的成分是(用化學(xué)式表示)
(4)上述澄清溶液中除SO以外,一定大量存在的離子是2-4.組卷:65引用:3難度:0.5
四、解答題(共1小題,滿分0分)
-
25.臭氧層是地球生命的保護(hù)神,臭氧比氧氣具有更強(qiáng)的氧化性.實(shí)驗(yàn)室可將氧氣通過高壓放電管來制取臭氧:3O2
2O3通電
(1)若在上述反應(yīng)中有30%的氧氣轉(zhuǎn)化為臭氧,所得混合氣的平均摩爾質(zhì)量為g/mol (保留一位小數(shù)).
(2)將8L氧氣通過放電管后,恢復(fù)到原狀況,得到氣體6.5L,其中臭氧為L.
(3)實(shí)驗(yàn)室將氧氣和臭氧的混合氣體0.896L(標(biāo)準(zhǔn)狀況)通入盛有20.0g銅粉的反應(yīng)器中,充分加熱后,粉末的質(zhì)量變?yōu)?1.6g.則原混合氣中臭氧的體積分?jǐn)?shù)為.組卷:478引用:17難度:0.1


