2022年山東省百師聯盟高考化學聯考試卷
發布:2025/1/7 23:0:2
一、選擇題:本題共10小題,每小題2分,共20分。每小題只有一個選項符合題目要求。
-
1.化學與生產生活密切相關。下列說法錯誤的是( )
A.誤食重金屬鹽引起人體中毒,急救時可以喝大量的牛奶解毒 B.醫學上常用BaSO4作為內服造影劑檢查消化系統 C.油脂的皂化反應是高分子化合物降解過程 D.以鐵粉為主要成分制成雙吸劑放入食品包裝袋,可以延長食物的保質期 組卷:21引用:3難度:0.6 -
2.下列物質的性質或用途的敘述錯誤的是( )
A.鹽酸可用于除去水垢中的CaSO4 B.“84”消毒液消毒原理是利用了NaClO的強氧化性 C.Fe2O3常用作油漆、涂料、油墨的紅色顏料 D.過氧化鈉可用作呼吸面具中的供氧劑 組卷:16引用:3難度:0.7 -
3.實驗室進行海帶提碘實驗,萃取后繼續分離得到單質碘的主要操作:用濃氫氧化鈉溶液進行反萃取、分液、酸化、過濾及干燥等。下列對應各實驗步驟的裝置錯誤的是( )
A. 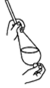
B. 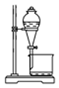
C. 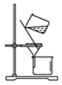
D.  組卷:26引用:1難度:0.7
組卷:26引用:1難度:0.7 -
4.下列反應的離子方程式錯誤的是( )
A.FeI2溶液中通入少量Cl2:Cl2+2Fe2+═2Fe3++2Cl- B.NaClO溶液中通入少量SO2:H2O+3ClO-+SO2═SO42-+Cl-+2HClO C.硝酸銀溶液中加入足量濃氨水:Ag++2NH3?H2O═[Ag(NH3)2]++2H2O D.氫氧化鎂固體溶解于氯化銨溶液:Mg(OH)2+2NH4+═Mg2++2NH3?H2O 組卷:16引用:1難度:0.7 -
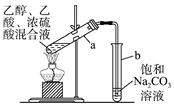 5.某同學進行乙酸乙酯的制備實驗:向試管中加入無水乙醇、濃硫酸、乙酸的混合物,按圖所示連接裝置,用酒精燈小心均勻地加熱試管,觀察到飽和Na2CO3溶液上方形成酯層,將試管中乙酸乙酯的粗產品用分液漏斗進行分液得乙酸乙酯。實驗操作及裝置圖中存在的錯誤有幾處?( )
5.某同學進行乙酸乙酯的制備實驗:向試管中加入無水乙醇、濃硫酸、乙酸的混合物,按圖所示連接裝置,用酒精燈小心均勻地加熱試管,觀察到飽和Na2CO3溶液上方形成酯層,將試管中乙酸乙酯的粗產品用分液漏斗進行分液得乙酸乙酯。實驗操作及裝置圖中存在的錯誤有幾處?( )A.4 B.3 C.2 D.1 組卷:59引用:1難度:0.7 -
6.四種常見元素的性質或結構信息如下表,下列說法正確的是( )
元素 甲 乙 丙 丁 性質或結構信息 原子核外有兩個電子層,最外層有3個未成對電子 原子的M層有1對成對的p電子 原子核外價電子排布為3dx4s2,有+2、+3兩種常見化合價 有兩種常見氧化物,其中一種是冶煉金屬工業的常用還原劑 A.甲元素氫化物的沸點一定比丁元素氫化物的沸點高 B.乙元素與丁元素的原子可構成直線形分子 C.將丙的+3價硝酸鹽溶解在稀硝酸中,溶液顯黃色 D.丁元素最高價氧化物的熔點比同主族相鄰元素最高價氧化物的熔點高 組卷:34引用:1難度:0.6
三、非選擇題:本題共5小題,共60分。
-
19.物質G是一種新型除草劑,可以經過如圖流程制得。
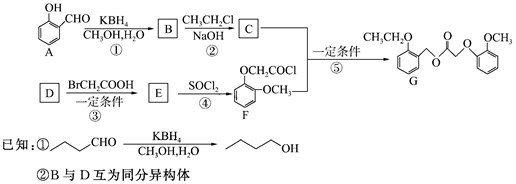
回答下列問題:
(1)物質A的化學名稱為。
(2)寫出同時符合下列條件的C的同分異構體的結構簡式。
①屬于芳香族化合物
②核磁共振氫譜有4組峰,峰面積之比為6:3:2:1
③遇FeCl3溶液無顏色變化,不能與單質鈉反應產生氫氣
(3)物質D的結構簡式為,物質E中含氧官能團名稱為。
(4)生成G的反應類型為。
(5)反應②的化學方程式為,反應③的無機產物為。
(6)結合題目信息,設計以A為原料合成物質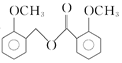 的路線 (其他試劑任選)。組卷:20引用:2難度:0.3
的路線 (其他試劑任選)。組卷:20引用:2難度:0.3 -
20.研究CO2加氫制CH4對資源綜合利用有重要意義。相關的主要化學反應如下:
I.CO2(g)+4H2(g)?CH4(g)+2H2O(g)ΔH1<0
II.CO2(g)+H2(g)?CO(g)+H2O(g)ΔH2
III.2CO(g)+2H2(g)?CO2(g)+CH4(g)ΔH3=-247.1kJ?mol-1
回答下列問題:
(1)在一定溫度下,由最穩定單質生成1mol某物質的焓變叫做該物質的標準摩爾生成焓,下表為298K時幾種物質的標準摩爾生成焓。則反應Ⅱ的焓變ΔH2=kJ?mol-1。
(2)在一定條件下,向體積為VL的恒容密閉容器中通入1molCO2和4molH2發生上述反應,反應20min容器內反應達到平衡時,容器中CH4(g)為amol,CO為bmol,以H2表示的0~20min內平均反應速率v(H2)=物質 H2 O2 CO CO2 H2O ΔfHmθ 0 0 -110.5 -393.5 -241.8 mol?L-1?min-1(用含a、b、V的代數式表示,下同),此時H2O(g)的濃度為mol?L-1,反應Ⅱ的平衡常數為(列出計算式)。
(3)在恒壓、CO2和H2的起始量一定的條件下,平衡時CH4、CO、CO2的物質的量隨溫度的變化如圖所示。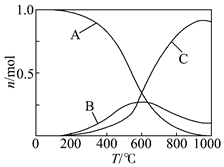
圖中曲線B表示的物質為;其物質的量在溫度高于600℃時隨溫度升高而下降的原因是。
(4)一定溫度和壓強條件下,為了提高反應速率和CH4選擇性,應當采取的措施是。組卷:26引用:2難度:0.5


