2020-2021學年湖南省岳陽市岳陽縣一中高一(下)期末化學試卷
發布:2025/1/7 13:30:2
一、單選題(每小題只一個選項符合題意)10個小題,每小題3分,共30分。
-
1.下列說法正確的是( )
A.C60和C70互為同位素 B.C2H6和C6H14互為同系物 C.CO和CO2互為同素異形體 D.CH3COOH和CH3OOCH是同一種物質 組卷:363引用:10難度:0.6 -
2.關于油脂,下列說法不正確的是( )
A.硬脂酸甘油酯可表示為 
B.花生油能使酸性高錳酸鉀溶液褪色 C.液態植物油通過催化加氫可轉變為固態氫化植物油 D.油脂是一種重要的工業原料,可用于制造肥皂 組卷:23引用:1難度:0.8 -
3.某金屬單質跟一定濃度的硝酸反應,假定只產生單一的還原產物,當參加反應的單質與被還原HNO3的物質的量之比為2:1時,還原產物可能是( )
A.N2O B.NO C.NO2 D.N2 組卷:364引用:9難度:0.9 -
4.在一定溫度下的密閉容器中發生反應:xA(g)+yB(g)?zC(g),平衡時測得A的濃度為0.80mol/L。保持溫度不變,將容器的容積擴大到原來的兩倍,再達平衡時,測得A的濃度為0.50mol/L。下列有關判斷正確的是( )
A.x+y<z B.平衡向正反應方向移動 C.B的轉化率增大 D.C的體積分數減小 組卷:28引用:4難度:0.6 -
5.下列有關物質的性質與用途對應關系錯誤的是( )
A.硅膠有吸水性,可作袋裝食品的干燥劑 B.小蘇打可溶于水,可作糕點的膨松劑 C.臭氧具有強氧化性,可作食品的殺菌劑 D.維生素C具有還原性,可作食品的抗氧化劑 組卷:11引用:3難度:0.6 -
6.化學與人類生產、生活、社會可持續發展密切相關,下列說法不正確的是( )
A.“天宮一號”中使用的碳纖維,是一種新型無機非金屬材料 B.為防止富脂食品氧化變質,常在包裝袋中放入生石灰 C.開發新能源,減少對化石燃料的依賴,可以促進低碳經濟 D.“靜電除塵”、“燃燒固硫”、“汽車尾氣催化凈化”都能提高空氣質量 組卷:37引用:4難度:0.9
三、非選擇題(4道小題,共50分)
-
18.(15分)能源開發和利用是科學研究的熱點課題。
(1)幾個有關CO的熱化學方程式如下:
I.CO(g)+2H2(g)?CH3OH(g)△H1
II.2CH3OH(g)?CH3OCH3(g)+H2O(g)△H2
III.CO(g)+H2O(g)?CO2(g)+H2(g)△H3
則3CO(g)+3H2(g)?CH3OCH3(g)+CO2(g)△H=(用含△H1、△H2、△H3的代數式表示)。
(2)在1L恒容密閉容器中充入一定量CH3OH發生反應:2CH3OH(g)?CH3OCH3(g)+H2O(g)△H,測得CH3OH的濃度與溫度的關系如圖所示: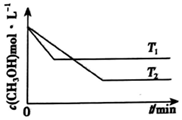
①△H(填“>”“<”或“=”)0,說明理由。
②在T1時達到平衡后,再向容器中充入少量甲醇蒸氣,CH3OH的平衡轉化率(填“增大”“減小”或“不變”)。
(3)工業上,利用水煤氣合成CH3OH的反應表示如下:2H2(g)+CO(g)?CH3OH(g)△H=-91.0kJ?mol-1,向1 L的恒容密閉容器中加入0.1mol H2和0.05mol CO在一定溫度下發生上述反應,10 min后反應達到平衡狀態,測得放出的熱量為3.64 kJ。
①從反應開始恰好平衡狀態時,H2的平均反應速率v(H2)為。
②在溫度不變條件下,上述反應達到平衡后再向容器中充入0.01 mol H2和0.05 mol CH3OH(g)時,平衡(填“向左移動”、“向右移動”或“不移動”)。
(4)探究CH3OH合成反應化學平衡的影響因素,有利于提高CH3OH的產率。以CO2、H2為原料合成CH3OH涉及的主要反應如下:
I.CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.5 kJ?mol-1
II.CO(g)+2H2(g)?CH3OH(g)△H2=-90.4 kJ?mol-1
III.CO2(g)+H2(g)?CO(g)+H2O(g)△H3
一定條件下,向體積為VL的恒容密閉容器中通入1mol CO2和3mol H2發生上述反應,達到平衡時,容器中CH3OH(g)為a mol,CO為b mol,此時H2O(g)的濃度為mol?L-1(用含a、b、V的代數式表示,下同),反應III的平衡常數為。組卷:41引用:4難度:0.3 -
19.用含鉻不銹鋼廢渣(含SiO2、Cr2O3、Fe2O3、Al2O3等)制取Cr2O3(鉻綠)的工藝流程如圖所示:

回答下列問題:
(1)“堿熔”時,為使廢渣充分氧化可采取的措施是(答一條即可)。
(2)Cr2O3、KOH、O2反應生成K2CrO4的化學方程式為。
(3)“水浸”時,堿熔渣中的KFeO2強烈與水反應生成的難溶物為(填化學式,下同);為檢驗“水浸”后的濾液中是否含有Fe3+,可選用的化學試劑是溶液。
(4)常溫下,“酸化”時pH不宜過低(pH低即酸性強)的原因是防止(填元素名稱)元素進入溶液;
(5)“還原”時發生反應的離子方程式為。組卷:4引用:1難度:0.5


