2021-2022學(xué)年云南省玉溪市通海三中高一(上)期末化學(xué)試卷
發(fā)布:2024/4/20 14:35:0
一、單選題(共30小題,每題2分,共60分)
-
1.人體正常的血紅蛋白中應(yīng)含F(xiàn)e2+.若誤食亞硝酸鈉,則導(dǎo)致血紅蛋白中的Fe2+轉(zhuǎn)化為高鐵血紅蛋白而中毒.服用維生素C可解除亞硝酸鈉中毒.下列敘述中正確的是( )
A.亞硝酸鈉表現(xiàn)了還原性 B.維生素C表現(xiàn)了還原性 C.維生素C將Fe3+氧化成Fe2+ D.亞硝酸鈉被氧化 組卷:60引用:9難度:0.7 -
2.在3NO2+H2O═2HNO3+NO的反應(yīng)中,發(fā)生還原反應(yīng)和氧化反應(yīng)的物質(zhì)的分子個(gè)數(shù)比是( )
A.3:1 B.1:3 C.1:2 D.2:1 組卷:11引用:2難度:0.5 -
3.將10mLNO和NO2的混合氣體通入裝滿水的倒立在水槽中的量筒,充分反應(yīng)后,最后剩余4mL氣體,(已知一氧化氮與水不反應(yīng),二氧化氮與水反應(yīng):3NO2+H2O═2HNO3+NO)則原混合氣體中NO的體積為( )
A.1mL B.3mL C.5mL D.7mL 組卷:21引用:1難度:0.5 -
4.用硫酸渣制備鐵黃(一種鐵基顏料)的過程中存在如下反應(yīng):4FeSO4+8NH3?H2O+O2═4FeOOH+4(NH4)2SO4+2H2O,下列說法正確的是( )
A.O2發(fā)生氧化反應(yīng) B.FeSO4作氧化劑 C.反應(yīng)中轉(zhuǎn)移電子數(shù)目為2e- D.FeOOH既是氧化產(chǎn)物又是還原產(chǎn)物 組卷:37引用:4難度:0.7 -
5.下列說法正確的是( )
A.非極性鍵只能存在單質(zhì)中,不可能存在化合物中 B.陰、陽離子間通過靜電引力所形成的化學(xué)鍵是離子鍵 C.冰中H2O分子間存在氫鍵,H2O分子內(nèi)存在極性共價(jià)鍵 D.HBr比HCl的熱穩(wěn)定性差,說明HBr的分子間作用力比HCl弱 組卷:375引用:4難度:0.4 -
6.已知原子序數(shù),可以推斷原子的( )
①質(zhì)子數(shù) ②中子數(shù) ③質(zhì)量數(shù) ④核電荷數(shù) ⑤核外電子數(shù) ⑥原子結(jié)構(gòu)示意圖A.①②③④ B.①④⑤⑥ C.②③④⑤ D.③④⑤⑥ 組卷:26引用:3難度:0.7 -
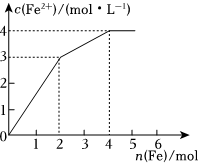 7.在Fe2(SO4)3和CuSO4的混合液中逐漸加入鐵粉,溶液中Fe2+的物質(zhì)的量濃度和加入鐵粉的物質(zhì)的量之間關(guān)系如圖所示。則該溶液中Fe2(SO4)3與CuSO4的物質(zhì)的量濃度之比為( )
7.在Fe2(SO4)3和CuSO4的混合液中逐漸加入鐵粉,溶液中Fe2+的物質(zhì)的量濃度和加入鐵粉的物質(zhì)的量之間關(guān)系如圖所示。則該溶液中Fe2(SO4)3與CuSO4的物質(zhì)的量濃度之比為( )A.3:1 B.1:2 C.2:1 D.1:1 組卷:22引用:1難度:0.7 -
8.某工業(yè)廢氣所含氮氧化物(NOx)的氮氧質(zhì)量比為7:4,該NOx可表示為( )
A.N2O B.NO C.N2O3 D.NO2 組卷:1067引用:6難度:0.9 -
9.已知有如下反應(yīng):①2
+Cl2═Br2+2BrO-3ClO-3
②+5Cl-+6H+═3Cl2+3H2OClO-3
③2FeCl2+Cl2═2FeCl3。
根據(jù)上述反應(yīng),判斷下列結(jié)論中錯(cuò)誤的是( )A.Cl2在反應(yīng)②中既是氧化產(chǎn)物又是還原產(chǎn)物 B.Cl2 在①、③反應(yīng)中均作氧化劑 C.氧化性強(qiáng)弱的順序?yàn)椋?div dealflag="1" class="MathJye" mathtag="math"> >BrO-3>Cl2>Fe3+ClO-3D.溶液中可發(fā)生: +6Fe2++6H+═Cl-+6Fe3++3H2OClO-3組卷:128引用:19難度:0.5 -
10.下列對于過氧化鈉的敘述中正確的是( )
A.是一種易溶于水的白色固體粉末 B.與酸反應(yīng)生成鹽和水,所以它是堿性氧化物 C.與水反應(yīng)時(shí),過氧化鈉是氧化劑,水是還原劑 D.與CO2反應(yīng)時(shí),1mol Na2O2轉(zhuǎn)移1mol電子 組卷:20引用:3難度:0.6 -
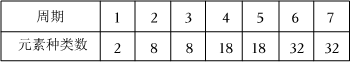 11.元素周期表中前七個(gè)周期的元素種類數(shù)如圖,請你從中尋找規(guī)律,并預(yù)言第八周期最多可能包含的元素種類數(shù)為( )
11.元素周期表中前七個(gè)周期的元素種類數(shù)如圖,請你從中尋找規(guī)律,并預(yù)言第八周期最多可能包含的元素種類數(shù)為( )A.18 B.32 C.50 D.64 組卷:9引用:2難度:0.5
二、非選擇題(共5小題,共40分)
-
34.A、B、C、D、E五種物質(zhì)的焰色反應(yīng)都顯黃色,A、B與水反應(yīng)都有氣體放出,A與水的反應(yīng)放出的氣體只具有氧化性,同時(shí)都生成溶液C,C與少量的CO2反應(yīng)生成D,D溶液與過量的CO2反應(yīng)生成E,E加熱能變成D。
(1)寫出下列物質(zhì)的化學(xué)式:A、C、E。
(2)B與水反應(yīng)的離子方程式是。
(3)D溶液中通入CO2的離子方程式:。
(4)7.8 g的A加入到足量的硫酸銅溶液中,標(biāo)況下,產(chǎn)生氣體的質(zhì)量為g,生成沉淀的質(zhì)量為g。組卷:1引用:1難度:0.4 -
35.以下是有關(guān)金屬與酸的反應(yīng),請?zhí)顚懴铝锌瞻祝?br />(1)分別取Wg鈉、鐵、鋁與足量的鹽酸反應(yīng),在相同條件下產(chǎn)生氫氣的體積比是
。
(2)分別取0.1mol鈉、鐵、鋁與足量的鹽酸反應(yīng),在相同條件下產(chǎn)生氫氣的體積比是。
(3)若產(chǎn)生相同物質(zhì)的量的氫氣,所需鈉、鐵、鋁的質(zhì)量比是。
(4)若產(chǎn)生相同體積(同溫同壓)的氫氣,所需鈉、鐵、鋁的物質(zhì)的量之比是。
(5)取0.2mol的金屬鈉、鐵、鋁,分別投入10mL1mol?L-1的鹽酸中,標(biāo)況下產(chǎn)生氫氣的體積由大到小的順序是。(鈉、鐵、鋁產(chǎn)生氫氣的體積分別用V1、V2、V3表示)組卷:16引用:2難度:0.5


