2021-2022學年湖南省長沙市長郡中學高一(上)期中化學試卷
發布:2025/1/3 13:30:2
一、選擇題(本題包括21小題,每小題2分,共42分,在每小題給出的四個選項中,只有一項是符合題目要求的)
-
1.分類是認識和研究物質及其變化的一種常用的科學方法.下列分類不合理的是( )
A.H2SO4屬于酸 B.Ca(OH)2屬于堿 C.NaHCO3屬于鹽 D.Cu屬于電解質 組卷:26引用:6難度:0.8 -
2.磁流體是電子材料的新秀,它既具有固體的磁性,又具有液體的流動性,其分散質粒子直徑在36~55nm之間。下列說法正確的是( )
A.該磁流體是一種純凈物 B.該磁流體比較穩定 C.該磁流體為懸濁液 D.該磁流體不能產生丁達爾效應 組卷:8引用:2難度:0.7 -
3.下列各組澄清透明液中,能大量共存的離子組是( )
A.Na+、Cu2+、Cl-、SO42- B.Na+、MnO4-、SO42-、I- C.Na+、OH-、HCO3-、SO42- D.Ba2+、Fe2+、Cl-、SO42- 組卷:39引用:6難度:0.7 -
4.下列反應中,劃線物質是還原劑的是( )
A.Zn+H2SO4═ZnSO4+H2↑ B.Cl2+2NaBr═2 NaCl+Br2 C.C+CO2 2CO高溫D.Fe2O3+2 Al 2Fe+Al2 O3高溫組卷:120引用:9難度:0.8 -
5.下列物質在指定條件下電離方程式正確的是( )
A.NaHCO3溶于水:NaHCO3═Na++H++CO32- B.Al2O3加熱熔化:Al2O3═2Al3++3O2- C.H2S在水中的電離:H2S?S2-+2H+ D.Cu(OH)2在水溶液中電離:Cu(OH)2═Cu2++2OH- 組卷:71引用:4難度:0.6 -
6.在下列反應中,H2O的作用與反應Br2+SO2+2H2O═H2SO4+2HBr中H2O的作用不同的是( )
A.Cl2+H2O═HClO+HCl B.4Fe(OH)2+O2+2H2O═4Fe(OH)3 C.CaO+H2O═Ca(OH)2 D.2H2O 2H2↑+O2↑通電組卷:15引用:2難度:0.7 -
7.下列離子能大量共存的是( )
A.使無色酚酞試液呈紅色的溶液中:Na+、K+、 、SO2-4CO2-3B.無色透明的溶液中:Cu2+、K+、 、SO2-4NO-3C.含有大量Ba(NO3)2的溶液中:Mg2+、 、NH+4、Cl-SO2-4D.使紫色石蕊試液呈紅色的溶液中:Na+、K+、 、CO2-3NO-3組卷:295引用:65難度:0.7 -
8.在某體系內有反應物和生成物5種物質:H2S、S、FeCl3、FeCl2、HCl.已知H2S為反應物,則另一反應物是( )
A.FeCl3 B.FeCl2 C.S D.HCl 組卷:113引用:25難度:0.7 -
9.為除去括號內的雜質,所選用的試劑或方法錯誤的是( )
A.CO2氣體(HCl),飽和NaHCO3溶液 B.Na2CO3固體(NaHCO3),加熱至不再產生氣體 C.Na2O2粉末(Na2O),將混合物在氧氣中加熱 D.Na2CO3溶液(Na2SO4),加入適量Ba(OH)2溶液,過濾 組卷:77引用:19難度:0.5
二、非選擇題(本題共6小題,共58分)
-
26.氯可形成多種含氧酸鹽,廣泛應用于殺菌、消毒及化工領域,實驗室中利用如圖裝置(部分裝置省略)制備KClO3和NaClO,探究其氧化還原性質。
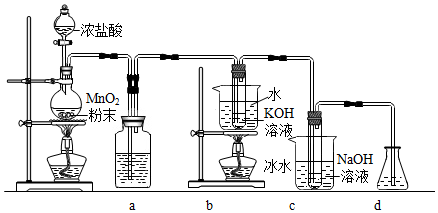
回答下列問題:
(1)a中的試劑為。
(2)b中采用的加熱方式是,c中化學反應的離子方程式是,采用冰水浴冷卻的目的是。
(3)反應結束后,取出b中試管,經冷卻結晶,,干燥,得到KClO3晶體。
(4)高鐵酸鈉(Na2FeO4)(其中氧元素是-2價)是一種新型的凈水劑,可以通過下述反應制取:2Fe(OH)3+4NaOH+3NaClO═2Na2FeO4+3NaCl+5H2O。
①用雙線橋法在化學方程式中標出電子轉移的情況:
2Fe(OH)3+4NaOH+3NaClO═2Na2FeO4+3NaCl+5H2O
②當反應中有5個FeO42-生成時,轉移的電子數是個。組卷:19引用:1難度:0.5 -
27.(1)X、Y、Z三種物質存在如圖1所示轉化關系。
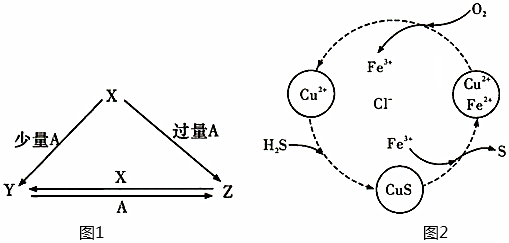
回答下列問題:
①若X為黑色固體單質,A為O2,寫出Z→Y的化學方程式:。
②若X為NaOH溶液,則寫出Y→Z的離子方程式:。
(2)已知常溫下在溶液中可發生如下兩個反應:
Ce4++Fe2+═Fe3++Ce3+
Sn2++2Fe3+═2Fe2++Sn4+
由此可以確定Ce4+、Sn4+、Fe3+三種離子的氧化性由強到弱的順序是。
(3)Mn2+、Bi3+、BiO3-、MnO4-、H+、H2O組成的一個氧化還原反應體系中,發生BiO3-→Bi3+的反應過程.
①該反應中,被氧化的元素是(填元素符號),氧化劑是(填化學式)。
②將以上物質分別填入下面對應的橫線上,組成一個未配平的化學方程式:++→++H2O。
(4)將H2S和空氣的混合氣體通入FeCl3、FeCl2、CuCl2的混合溶液中反應回收S,其物質轉化如圖2所示。
①寫出CuCl2與H2S反應的離子方程式:。
②通過流程圖的分析,整個流程的總反應為。組卷:36引用:1難度:0.5


