2021-2022學年安徽省滁州市定遠縣育才學校高二(下)第二次月考化學試卷(二)
發布:2024/4/20 14:35:0
一、選擇題(本大題共16小題每小題3分,滿分48分)
-
1.已知Zn2+的4s軌道和4p軌道可以形成sp3型雜化軌道,那么[ZnCl4]2-的空間構型為( )
A.直線形 B.平面正方形 C.正四面體形 D.正八面體型 組卷:243引用:20難度:0.7 -
2.在
離子中存在4個N-H共價鍵,則下列說法正確的是( )NH+4A.四個共價鍵的鍵長完全相同 B.四個共價鍵的鍵長完全不同 C.原來的三個N-H的鍵長完全相同,但與由配位鍵形成的N-H鍵不同 D.四個N-H鍵鍵長相同,但鍵能不同 組卷:27引用:7難度:0.9 -
 3.鐵鎂合金是目前已發現的儲氫密度較高的儲氫材料之一,其晶胞結構如圖所示(黑球代表Fe,白球代表Mg)。則下列說法錯誤的是( )
3.鐵鎂合金是目前已發現的儲氫密度較高的儲氫材料之一,其晶胞結構如圖所示(黑球代表Fe,白球代表Mg)。則下列說法錯誤的是( )A.鐵鎂合金的化學式可表示為Mg2Fe B.晶胞中有14個鐵原子 C.晶體中存在的化學鍵類型為金屬鍵 D.該晶胞的質量是 g(NA表示阿伏加德羅常數的值)416NA組卷:22引用:5難度:0.6 -
4.下列有關晶體的敘述中,錯誤的是( )
A.干冰晶體中,每個CO2周圍緊鄰12個CO2 B.氯化鈉晶體中,每個Na+周圍緊鄰且距離相等的Na+共有6個 C.氯化銫晶體中,每個Cs+周圍緊鄰8個Cl- D.金剛石為三維骨架結構,由共價鍵形成的碳原子環中,最小的環上有6個碳原子 組卷:107引用:7難度:0.7 -
5.如圖是元素周期表的一部分,圖中的字母分別代表某種化學元素。下列說法正確的是( )

A.沸點:A2D<A2X B.CA3分子是非極性分子 C.單質C2中δ鍵與π鍵的數目之比為1:2 D.酸性:HCl>H2S,可說明非金屬性:Cl>S 組卷:25引用:2難度:0.7 -
6.利用分子間作用力形成超分子進行“分子識別”,實現分子分離,是超分子化學的重要研究和應用領域。如圖表示用“杯酚”對C60和C70進行分離的過程,下列對該過程的說法錯誤的是( )

A.C70能溶于甲苯,C60不溶于甲苯 B.C60能與“杯酚”形成超分子 C.C70不能與“杯酚”形成超分子 D.“杯酚”能夠循環使用 組卷:20引用:2難度:0.5
二、綜合題(本大題共4小題,滿分52分)
-
19.根據原子結構、元素周期表和元素周期律的知識回答下列問題:
(1)A元素次外層電子數是最外層電子數的1/4,外圍電子的電子排布圖是.
(2)B是1~36號元素原子核外未成對電子數最多的元素,B元素的名稱是,該元素在元素周期表中的位置是.
(3)C元素基態原子的電子排布圖是如圖1中的(填序號),另一電子排布圖不能作為基態原子的電子排布圖是因為它不符合(填編號“A”、“B”、“C”).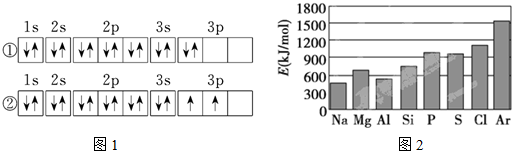
A.能量最低原理 B.泡利原理 C.洪特規則
(4)第三周期元素的氣態電中性基態原子失去最外層一個電子轉化為氣態基態正離子所需的最低能量叫做第一電離能(設為E).如圖2所示:
①同周期內,隨著原子序數的增大,E值變化的總趨勢是;
②根據圖中提供的信息,試推斷E氧E氟(填“>”、“<”或“=”,下同);
③根據第一電離能的含義和元素周期律,試推斷E鎂E鈣.組卷:91引用:5難度:0.3 -
20.四種元素A、B、C、D,其中A元素原子的原子核內只有一個質子;B的基態原子s能級的總電子數比p能級的總電子數多1;C元素的原子最外層電子數是次外層的3倍;D是形成化合物種類最多的元素.
(1)A、D形成的某種化合物甲是一種重要的化工產品,可用作水果和蔬菜的催熟劑,甲分子中σ鍵和π鍵數目之比為;寫出由甲制高聚物的反應方程式.
(2)A、C形成的某種化合物乙分子中含非極性共價鍵,乙分子屬于(“極性分子”或“非極性分子”);其電子式;將乙加入淺綠色酸性溶液中,溶液變為棕黃色,寫出該反應的離子方程式.
(3)寫出B的基態原子電子排布圖為.與PH3相比,DC2易液化的主要原因是;
(4)笑氣(B2C)是一種麻醉劑,有關理論認為B2C與CO2分子具有相似的結構.故B2C的空間構型是,其為(填“極性”或“非極性”)分子.組卷:37引用:6難度:0.5


