2021-2022學(xué)年重慶市育才中學(xué)高三(上)月考化學(xué)試卷(五)
發(fā)布:2025/1/4 6:0:2
一、選擇題:本題共14個小題,每小題3分,共42分。在每小題給出的四個選項中,只有一項是符合題目要求的。
-
1.中國文化中蘊藏著豐富的化學(xué)知識,下列對古代研究成果的說明不合理的是( )
A.聞名世界的秦兵馬俑是陶制品,由黏土經(jīng)高溫?zé)Y(jié)而成,主要化學(xué)成分為硅酸鹽 B.《本草綱目》“用濃酒和糟入甑,蒸令氣上,用器承滴露”,利用到蒸餾 C.“素紗單衣”所用的蠶絲的主要成分是纖維素 D.商代后期鑄造出工藝精湛的青銅器司母戊鼎,其材質(zhì)屬于合金 組卷:6引用:1難度:0.8 -
2.下列關(guān)于物質(zhì)應(yīng)用錯誤的是( )
A.熱的純堿溶液清洗鐵器表面油脂類油污 B.硅具有電學(xué)特性,可用作光導(dǎo)纖維 C.明礬、硫酸鐵易水解形成膠體,可用于凈水 D.液氨氣化吸熱,液氨可用作制冷劑 組卷:2引用:1難度:0.7 -
3.阿伏加德羅常數(shù)的值為NA,下列說法正確的是( )
A.標(biāo)準(zhǔn)狀況下,5.6L甲烷和乙烯的混合氣體中所含氫原子數(shù)為NA B.1molFe與1molCl2充分反應(yīng)轉(zhuǎn)移電子數(shù)為3NA C.標(biāo)準(zhǔn)狀況下,22.4L己烷中所含共價鍵數(shù)目為19NA D.標(biāo)準(zhǔn)狀況下,11.2LCl2溶于水,溶液中Cl-、ClO-和HClO的微粒數(shù)之和為NA 組卷:0引用:1難度:0.7 -
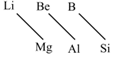 4.元素周期表中,某些主族元素與右下方的主族元素(如圖)的性質(zhì)具有相似性,這種規(guī)律被稱為“對角線規(guī)則”。則下列敘述正確的是( )
4.元素周期表中,某些主族元素與右下方的主族元素(如圖)的性質(zhì)具有相似性,這種規(guī)律被稱為“對角線規(guī)則”。則下列敘述正確的是( )A.Li在空氣中燃燒生成Li2O2 B.BF3各原子均滿足最外層8電子結(jié)構(gòu) C.Be(OH)2既能溶于強酸又能溶于強堿溶液 D.硼酸鈉水溶液顯中性 組卷:3引用:1難度:0.8 -
5.向密閉容器中充入1molHI,發(fā)生反應(yīng):2HI(g)?H2(g)+I2(g)△H>0,達(dá)到平衡狀態(tài)。該反應(yīng)經(jīng)過以下兩步基元反應(yīng)完成:i.2HI→H2+2IΔH1,ii.2I→I2ΔH2。下列分析正確的是( )
A.升高容器內(nèi)溫度,正反應(yīng)速率升高,逆反應(yīng)速率降低 B.n(HI)+n(I2)=1mol C.恒溫時,壓縮容器,平衡不移動導(dǎo)致氣體顏色不變 D.ΔH1+ΔH2>0 組卷:5引用:1難度:0.7 -
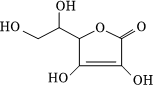 6.維生素C(VC)具有緩解重金屬中毒、預(yù)防癌癥、強抗氧化性等功能,它主要存在于新鮮的蔬菜、水果中,其結(jié)構(gòu)簡式如圖所示。下列有關(guān)維生素C的敘述正確的是( )
6.維生素C(VC)具有緩解重金屬中毒、預(yù)防癌癥、強抗氧化性等功能,它主要存在于新鮮的蔬菜、水果中,其結(jié)構(gòu)簡式如圖所示。下列有關(guān)維生素C的敘述正確的是( )A.VC的分子式為C6H10O6 B.VC易溶于水 C.VC分子中有羥基、碳碳雙鍵、羰基、醚鍵四種官能團 D.VC在空氣中易被還原而變質(zhì),需密封保存 組卷:3引用:1難度:0.7
(二)選考題:請考生從18、19題中任選一題作答。【化學(xué)——選修3:物質(zhì)結(jié)構(gòu)與性質(zhì)】(15分)
-
18.鐵在生活中分布較廣,占地殼含量的4.75%,僅次于氧、硅、鋁,位居地殼含量第四位,鐵及其化合物在人們生成、生活中有著廣泛的應(yīng)用,請按要求回答下列問題:
(1)請寫出Fe原子的價層電子排布圖:。
(2)早在西漢時期的《淮南萬畢術(shù)》中就記載“曾青得鐵則化為銅”,這是有關(guān)“濕法煉銅”的最早文獻(xiàn)記錄。若向盛裝有硫酸銅水溶液的試管里加入氨水,首先生成藍(lán)色沉淀,繼續(xù)滴加氨水,得到深藍(lán)色的透明溶液。
①請寫出藍(lán)色沉淀溶解的離子反應(yīng)方程式:。
②若向該深藍(lán)色的透明溶液中加入極性較小的溶劑(如乙醇),將有深藍(lán)的晶體析出,請寫出該晶體的化學(xué)式:。
(3)二茂鐵又稱二環(huán)戊二烯合鐵,分子式為(C5H5)2Fe,是一種具有芳香族性質(zhì)的有機過渡金屬化合物。其結(jié)構(gòu)為 ,其制備原理可簡單表示為2KOH+FeCl2+2C5H5→(C5H5)2Fe+2KCl+2H2O。
,其制備原理可簡單表示為2KOH+FeCl2+2C5H5→(C5H5)2Fe+2KCl+2H2O。
①環(huán)戊二烯( )分子中的碳原子的雜化方式為 。結(jié)合所學(xué)知識分析上述反應(yīng)中除Cl元素之外,其他非金屬元素的電負(fù)性由大到小的順序為。
)分子中的碳原子的雜化方式為 。結(jié)合所學(xué)知識分析上述反應(yīng)中除Cl元素之外,其他非金屬元素的電負(fù)性由大到小的順序為。
②當(dāng)環(huán)戊二烯(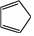 )失去一個氫離子之后,形成環(huán)戊二烯負(fù)離子(
)失去一個氫離子之后,形成環(huán)戊二烯負(fù)離子(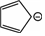 ),研究發(fā)現(xiàn)在該結(jié)構(gòu)中形成了類似于苯環(huán)中的大π鍵,則該大π鍵可表示為 。(已知
),研究發(fā)現(xiàn)在該結(jié)構(gòu)中形成了類似于苯環(huán)中的大π鍵,則該大π鍵可表示為 。(已知 分子中的大π鍵可表示為π66)。
分子中的大π鍵可表示為π66)。
(4)如圖是一種鐵、鋁金屬間化合物的晶胞結(jié)構(gòu),因該物質(zhì)資源豐富,具有優(yōu)良抗腐蝕性和抗氧化性,價格低廉,有取代不銹鋼的巨大潛力。說明:Fe原子位于頂點、面心、棱心、大立方體的體心,以及四個互不相鄰的小立方體的體心;Al原子位于四個互不相鄰的小立方體體心。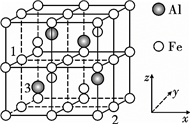
①鐵、鋁金屬間化合物的化學(xué)式為;若晶胞中1,2號原子的坐標(biāo)分別為(0,,12)、(0,12,0),則晶胞中3號原子的坐標(biāo)12。
②則該立方晶胞的密度為ρg/cm3,NA表示阿伏加德羅常數(shù),試計算晶胞中距離最近的兩個Fe原子核間的距離為pm。組卷:15引用:1難度:0.3
【化學(xué)——選修5:基礎(chǔ)有機化學(xué)】(15分)
-
19.以鏈烴 A 為原料合成兩種高分子材料的路線如圖:
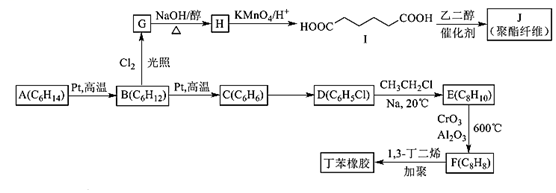
已知以下信息:
①B 的核磁共振氫譜中只有一組峰;G 為一氯代烴。
②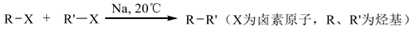
③烷烴可在Pt高溫催化作用下脫氫環(huán)化,逐步轉(zhuǎn)化為芳香烴。
回答下列問題:
(1)B的化學(xué)名稱為。
(2)G生成H的化學(xué)方程式為。
(3)由C生成D的反應(yīng)條件是,由E生成F的反應(yīng)類型為。
(4)J結(jié)構(gòu)簡式為。
(5)I的同分異構(gòu)體中能同時滿足下列條件的共有種(不含立體異構(gòu))。
①能與飽和NaHCO3溶液反應(yīng)產(chǎn)生氣體;
②既能發(fā)生銀鏡反應(yīng),又能發(fā)生水解反應(yīng)。
其中核磁共振氫譜為4組峰,且面積比為 6:2:1:1 的是(寫出一種結(jié)構(gòu)簡式)。
(6)參照上述合成路線,以2-甲基己烷和一氯甲烷為原料(無機試劑任選),設(shè)計制備化合物E的合成路線:。組卷:1引用:1難度:0.5


