2021-2022學年四川省成都二十中高一(上)期中化學試卷
發布:2024/11/23 2:30:1
一、選擇題(共20小題,每小題3分,滿分60分)
-
1.下列儀器不能用于加熱的是( )
A. 
B. 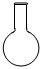
C. 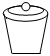
D. 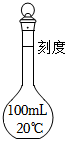 組卷:117引用:14難度:0.7
組卷:117引用:14難度:0.7 -
2.蘋果汁是人們喜愛飲料,由于此飲料中含有Fe2+,現榨的蘋果汁在空氣中會由淡綠色變為棕黃色,若榨汁時加入維生素C,可有效防止這種現象發生.這說明維生素C具有( )
A.氧化性 B.還原性 C.堿性 D.酸性 組卷:408引用:172難度:0.7 -
3.從水和食用油的混合物中分離出食用油,該步驟應選的實驗裝置是( )
A. 
B. 
C. 
D.  組卷:0引用:1難度:0.5
組卷:0引用:1難度:0.5 -
4.下列關于分散系的說法不正確的是( )
A.制備氫氧化鐵膠體時,可以將飽和FeCl3溶液滴入沸水,然后煮沸至溶液呈紅褐色 B.根據是否具有丁達爾效應,將分散系分為溶液、濁液和膠體 C.氯化鐵溶液可用于傷口止血。這種“傷口上撒鹽”的做法的化學原理是膠體的聚沉 D.膠體區別于其他分散系的本質特征是分散質的微粒直徑在1~100nm之間 組卷:28引用:1難度:0.8 -
5.下列關于物質的分類正確的是( )
選項 金屬氧化物 含氧酸 鹽 混合物 電解質 A SiO2 HClO 燒堿 KAl(SO4)2?12H2O C2H5OH B Na2O HNO3 NaHSO4 鹽酸 AgCl C MgO H2SiO3 Cu2(OH)2CO3 食鹽 NH3 D Al2O3 NH3?H2O BaCO3 自來水 Mg A.A B.B C.C D.D 組卷:8引用:1難度:0.6 -
6.下列操作不能達到目的的是( )
選項 目的 操作 A 配制100mL 1mol/LCuSO4溶液 將16g CuSO4溶于100mL蒸餾水中 B 除去汽油中的水 將混合物靜置,再分液 C 除去NaCl溶液中的泥沙 將混合物過濾 D 制備氫氧化鐵膠體 將氯化鐵飽和溶液滴入沸水中,加熱到紅褐色 A.A B.B C.C D.D 組卷:1引用:2難度:0.7 -
7.用NA表示阿伏加德羅常數的值,下列敘述正確的是( )
A.常溫常壓下,2NA個CO2分子占有的體積為44.8L B.標準狀況下22.4LCCl4含有的分子數為NA C.2L0.5mol?L-1FeCl3溶液中Cl-濃度為3mol?L-1 D.2.3gNa與O2完全反應生成Na2O,失去的電子總數為0.1NA 組卷:3引用:1難度:0.7 -
8.下列兩種氣體的分子數一定相等的是( )
A.質量相同,體積不同的N2和C2H4 B.相同密度、不同體積的CO2和C2H4 C.同溫同體積的O2和N2 D.標準狀況下1molO2和22.4LH2O 組卷:5引用:1難度:0.7
二、解答題(共4小題,滿分60分)
-
23.為了除去KCl溶液中少量的MgCl2、MgSO4,可選用Ba(OH)2、HCl和K2CO3三種試劑,按如下步驟操作:

(1)寫出上述三種試劑的化學式:A,B,C。
(2)上述操作Ⅰ所用玻璃儀器的名稱是;操作Ⅱ的名稱是。
(3)加過量A時發生有關反應的化學方程式為、。
(4)檢驗B是否過量的方法是。組卷:80引用:4難度:0.3 -
24.現有五種物質A、B、C、D、E,其中有一種是堿,四種是鹽,溶于水后電離可以產生下表中的離子:
為鑒別它們,分別完成以下實驗,其結果如下:陽離子 Na+ H+ Ba2+ 陰離子 OH- CO2-3SO2-4
①A溶液與B溶液反應生成無色氣體X,氣體X可以和C溶液反應生成沉淀E,沉淀E可與B溶液反應,但反應很快停止;
②B溶液與 C溶液反應生成白色沉淀D,沉淀D不溶于稀硝酸.
請根據上述實驗結果,填空:
(1)寫出下列物質的名稱:X.
(2)鑒別B在溶液中產生的陰離子的實驗操作方法是.
(3)完成以下水溶液中的反應的離子方程式:
A溶液與B溶液反應:
B與C反應至溶液呈中性:
(4)D 與E的混合物ag,加入足量鹽酸,反應完畢生成標準狀況時的氣體 bL,則D在混合物中的質量分數為.組卷:16引用:2難度:0.3


