2020-2021學年內蒙古巴彥淖爾市杭錦后旗奮斗中學高一(上)期中化學試卷
發布:2024/4/20 14:35:0
一、單項選擇題(共25題,每題2分,共50分)
-
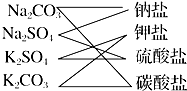 1.如圖所示是對Na2CO3、Na2SO4、K2CO3、K2SO4四種物質進行的分類,這種分類方法的名稱是( )
1.如圖所示是對Na2CO3、Na2SO4、K2CO3、K2SO4四種物質進行的分類,這種分類方法的名稱是( )A.交叉分類法 B.樹狀分類法 C.圈圖法 D.鏈狀箭頭法 組卷:39引用:3難度:0.9 -
2.如圖分別表示四種操作,其中有兩處錯誤的是( )
A. 
讀數B. 
稀釋C. 
稱量D. 
溶解組卷:51引用:4難度:0.9 -
3.如果你家里的食用花生油不小心混入了大量的水,利用你所學的知識,最簡便的分離方法是( )
A. 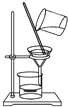
B. 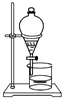
C. 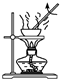
D. 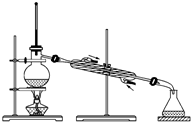 組卷:341引用:102難度:0.7
組卷:341引用:102難度:0.7 -
4.對于易燃、易爆、有毒的化學物質,往往會在其包裝上貼上危險警告標簽。下面所列物質貼錯了標簽的是( )
A B C D 物質 氫氧化鈉 金屬汞 碳酸鈉 硝酸銨 危險警告標簽 



A.A B.B C.C D.D 組卷:21引用:2難度:0.8 -
5.水的摩爾質量是( )
A.18 B.18g C.18g/mol D.18mol 組卷:125引用:28難度:0.9 -
6.下列對實驗操作的敘述錯誤的是( )
A.萃取碘時,倒轉分液漏斗,用力振蕩,并不時旋開活塞放氣 B.蒸餾盛在燒瓶中含水的酒精,需在瓶內放一些碎瓷片 C.蒸餾實驗中,溫度計插入液體中測量混合液的溫度 D.用分液漏斗分離兩種互不相溶的液體時,從分液漏斗上口倒出上層水溶液 組卷:2引用:2難度:0.5 -
7.下列常用實驗儀器中,能直接加熱的是( )
A.分液漏斗 B.普通漏斗 C.蒸餾燒瓶 D.試管 組卷:96引用:28難度:0.9 -
8.鑒別硫酸銅溶液與氫氧化鐵膠體最簡便的方法是( )
A.萃取 B.蒸餾 C.過濾 D.丁達爾效應 組卷:68引用:28難度:0.9 -
9.溶液、膠體和濁液這三種分散系的本質區別是( )
A.是否有丁達爾現象 B.是否能通過濾紙 C.分散質粒子的大小 D.是否均一、透明、穩定 組卷:952引用:94難度:0.9 -
10.下列物質屬于電解質且能導電的是( )
A.銅 B.熔融狀態燒堿 C.食鹽水 D.蔗糖 組卷:9引用:2難度:0.5
二、解答題(共5小題,滿分50分)
-
29.要配制480mL 0.2mol?L-1的FeSO4溶液,配制過程中有如下操作步驟:
①把稱量好的綠礬(FeSO4?7H2O)放入小燒杯中,加適量蒸餾水溶解;
②把①所得溶液小心轉入中;
③繼續向容量瓶中加蒸餾水至液面距離刻度l~2cm處,改用滴加蒸餾水至液面與刻度線相切;
④用少量蒸餾水洗滌燒杯和玻璃棒2~3次,每次洗滌的液體都小心轉入容量瓶,并輕輕搖勻;
⑤將容量瓶塞緊,反復上下顛倒,搖勻;
⑥待溶液恢復到室溫。
請填寫下列空白:
(1)實驗操作步驟的正確順序為(填序號),完成此配制實驗,除了量筒、燒杯、玻璃棒外還需要的常見的玻璃儀器有。
(2)實驗室用綠礬(FeSO4?7H2O)來配制該溶液,用托盤天平稱量綠礬g。
(3)由于錯誤操作,使得實際濃度比所要求的偏小的是(填寫編號)。
A.稱量綠礬時,左碼右物
B.使用容量瓶配制溶液時,俯視液面定容
C.沒有用蒸餾水洗燒杯2~3次,并將洗液移入容量瓶中
D.容量瓶剛用蒸餾水洗凈,沒有干燥
E.定容時,滴加蒸餾水,先使液面略高于刻度線,再吸出少量水使液面凹面與刻度線相切
F.把配好的溶液倒入剛用蒸餾水洗凈的試劑瓶中備用
(4)定容時,若加蒸餾水時不慎超過刻度線,處理方法是。組卷:14引用:3難度:0.7 -
30.現將31.8gNa2CO3固體溶于水配成體積為1L的溶液,回答下列問題:
(1)該溶液中含有CO32-的數目是,Na+的濃度是mol/L
(2)現有某濃度的濃鹽酸,該鹽酸的密度d=1.2g/cm3,質量分數w=36.5%,計算該鹽酸的物質的量濃度
是mol/L。
(3)欲將題干中的Na2CO3完全反應生成CO2氣體,則至少需要(2)中的鹽酸mL,生成的CO2氣體的體積是mL (標況下)。組卷:12引用:2難度:0.5


