2020-2021學年北京市首師大二附中高一(上)期中化學試卷
發布:2024/11/18 1:30:2
一、選擇題
-
1.下列有關我國古代技術應用中,其工作原理不涉及化學反應的是( )
A.火藥使用 B.糧食釀酒 C.轉輪排字 D.鐵的冶煉 



A.A B.B C.C D.D 組卷:49引用:16難度:0.9 -
2.下列貢獻與中國科學家無關的是( )
A.創立侯氏制堿法 B.發現青蒿素 C.合成結晶牛胰島素 D.發明元素周期表 組卷:68引用:3難度:0.9 -
3.下列物質中,屬于純凈物的是( )
A.漂白粉 B.濃硫酸 C.液氯 D.氯水 組卷:12引用:2難度:0.8 -
4.在①MgO、CuO、CaO、SO2;②C、Fe、S、P;③ZnCl2、BaCO3、HNO3、NaNO3三組物質中,每組各有一種物質在分類上與組內其他物質不同,這三種物質分別是( )
A.CuO、Fe、ZnCl2 B.SO2、Fe、HNO3 C.CaO、C、BaCO3 D.SO2、S、NaNO3 組卷:81引用:6難度:0.9 -
5.下列敘述正確的是( )
A.直徑介于1nm~100nm之間的微粒稱為膠體 B.Fe(OH)3難溶于水,因此不可能均勻地分散在水里形成穩定的紅褐色膠體 C.根據丁達爾效應,利用一束強光可以區別淀粉膠體和食鹽溶液 D.膠體粒子是很多分子的集合體,因此不能透過濾紙,但可以通過半透膜 組卷:49引用:7難度:0.8 -
6.等質量的下列物質中,所含分子數最少的是( )
A.Cl2 B.HCl C.NH3 D.H2SO4 組卷:88引用:24難度:0.7 -
7.下列物質不能用氯氣與單質直接化合制取的是( )
A.AlCl3 B.FeCl2 C.HCl D.CuCl2 組卷:22引用:6難度:0.7 -
8.下列說法中,正確的是( )
A.Mg的摩爾質量是24g/mol B.22gCO2物質的量為2.2mol C.1molCl2中含有的氯原子數約為6.02×1023 D.常溫常壓下,1molN2的體積是22.4L 組卷:73引用:4難度:0.7 -
9.配制體積為100mL、溶質物質的量為0.2mol的NaOH溶液時,不需要用到的儀器是( )
A. 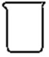
燒杯B. 
玻璃棒C. 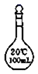
容量瓶D. 
集氣瓶組卷:11引用:2難度:0.6 -
10.下列過程中,沒有氣體產生的是( )
A. 
B. 
C. 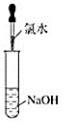
D. 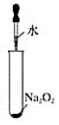 組卷:7引用:1難度:0.5
組卷:7引用:1難度:0.5 -
11.在標準狀況下,下列物質體積最大的是( )
A.3 g氫氣 B.6.02×1023個氫分子 C.44.8 L氫氣 D.0.5 mol氫氣 組卷:61引用:4難度:0.7
二、填空題
-
32.某實驗需要500mL 0.10mol/L的Na2CO3溶液,現通過如下步驟配制:
①把稱量好的固體Na2CO3放入小燒杯中,加適量蒸餾水攪拌溶解;
②用少量蒸餾水洗滌燒杯和玻璃棒2~3次,每次洗滌的液體都小心轉入容量瓶,并輕輕搖勻;
③蓋好瓶塞,反復上下顛倒,搖勻;
④把溶解固體后所得溶液冷卻至室溫,轉入儀器A中;
⑤繼續加蒸餾水至液面距刻度線1~2cm處,改用膠頭滴管滴加蒸餾水至溶液的凹液面與刻度線相切;
(1)操作步驟的正確順序為。(填序號)
(2)稱量的Na2CO3固體質量應為g。
(3)儀器A的名稱是。
(4)取出100mL配制好的溶液,加蒸餾水稀釋至c(Na2CO3)=0.02mol/L.則稀釋后溶液的體積為。
(5)下列關于容量瓶的使用方法中,正確的是。(填字母序號)
A.使用前要檢驗是否漏水
B.在容量瓶中直接溶解固體或稀釋液體
C.在燒杯中溶解固體后,迅速將溶液轉移到容量瓶中
D.向容量瓶中轉移溶液用玻璃棒引流
E.加水時水量超過了刻度線,迅速用膠頭滴管將過量的水吸出
(6)下列操作會使所配溶液的物質的量濃度偏低的是。(填字母序號)
A.將燒杯中的溶液轉移到容量瓶時不慎灑到容量瓶外
B.定容讀數時,俯視容量瓶上的刻度線
C.加水定容時,水量超過了刻度線
D.洗滌步驟中,洗滌液沒有轉入容量瓶組卷:223引用:3難度:0.5 -
33.我國著名的制堿專家侯德榜,在純堿制造方面做出了重大貢獻。用“侯氏制堿法”制得的純堿中常含有氯化鈉等雜質,化學興趣小組欲對某品牌純堿樣品中碳酸鈉的質量分數進行實驗探究。
資料摘要:
①濃硫酸具有很強的吸水性。
②堿石灰常用于吸收水蒸氣和二氧化碳。
利用如圖所示實驗裝置(鐵架臺略去)和試劑,通過測定樣品和稀鹽酸反應產生的CO2氣體的質量,計算Na2CO3的質量分數(裝置氣密性良好,忽略鹽酸的揮發性且每步反應或作用都是完全的)。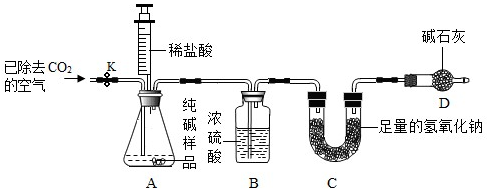
(1)打開止水夾K,先對裝置A和B(已連接)通入已除去CO2的空氣一會兒,以排盡裝置A和B中含有,再接上裝置C和D。
(2)關閉止水夾K,加入足量的稀鹽酸(雜質不與鹽酸反應),裝置A中樣品產生氣體的化學方程式。
(3)待裝置A中的反應結束后,再一次打開止水夾K,繼續往裝置通入已除去CO2的空氣一會兒。此操作的目的是。若沒有裝置B,將會使測定結果(選填“偏大”或“偏小”)。裝置D的作用。組卷:7引用:1難度:0.6


