2015-2016學(xué)年河南省三門峽市陜州中學(xué)高三(上)入學(xué)化學(xué)試卷
發(fā)布:2024/10/30 22:0:2
一、選擇題(共48分,每題3分)
-
1.分類是科學(xué)研究的重要方法,下列物質(zhì)分類不正確的是( )
A.化合物:干冰,冰水混合物,燒堿,小蘇打 B.非電解質(zhì):乙醇,四氯化碳,氯氣,葡萄糖 C.同素異形體:活性炭,C60,C80,金剛石 D.混合物:漂白粉,純凈礦泉水,分析純鹽酸,石灰石 組卷:26引用:3難度:0.9 -
2.X、Y、Z為三種單質(zhì).已知:Y能將Z從其化合物的水溶液中置換出來,而Z又能將X從其化合物的水溶液中置換出來.由此可以推斷下列說法中可能正確的是( )
①單質(zhì)的氧化性:Y>Z>X; ②單質(zhì)的還原性:Y>Z>X;
③對應(yīng)離子的氧化性:X>Z>Y; ④對應(yīng)離子的還原性:X>Z>Y.A.只有① B.只有②③ C.只有①④ D.①②③④ 組卷:77引用:12難度:0.7 -
3.物質(zhì)的量濃度相同的硝酸鉀、硫酸鉀、磷酸鉀(K3PO4)三種溶液中,若使鉀離子的物質(zhì)的量相同,則這三種溶液的體積比為( )
A.3:2:1 B.6:3:2 C.2:3:6. D.1:2:3 組卷:107引用:14難度:0.9 -
4.有BaCl2和NaCl的混合溶液a L,將它均分成兩份。一份滴加稀硫酸,使Ba2+離子完全沉淀;另一份滴加AgNO3溶液,使Cl-離子完全沉淀。反應(yīng)中消耗xmolH2SO4、y mol AgNO3.據(jù)此得知原混合溶液中的c(Na+)/mol?L-1為( )
A. y-2xaB. y-xaC. 2y-2xaD. 2y-4xa組卷:194引用:104難度:0.9 -
5.下列溶液中Cl-濃度與50mL 1mol?L-1 AlCl3溶液中Cl-濃度相等的是( )
A.150 mL 1 mol?L-1的NaCl溶液 B.75 mL 2 mol?L-1NH4Cl溶液 C.75 mL 1 mol?L-1的FeCl3溶液 D.150 mL 2 mol?L-1的KCl溶液 組卷:60引用:22難度:0.7 -
6.下列物質(zhì)按照純凈物、混合物、電解質(zhì)和非電解質(zhì)順序排列的是( )
A.鹽酸、水煤氣、醋酸、干冰 B.天然氣、空氣、苛性鉀、石灰石 C.液氨、氯水、硫酸鈉、乙醇 D.膽礬、漂白粉、氯化鉀、氯氣 組卷:47引用:10難度:0.9 -
7.能在水溶液中大量共存的一組離子是( )
A.K+、H+、 、NO-3SiO2-3B.H+、 、Al3+、NH+4SO2-4C.Fe2+、H+、ClO-、 SO2-4D. 、Mg2+、AlO-2、HCO-3NO-3組卷:5引用:2難度:0.7
二、(非選擇題共52分)
-
21.通常狀況下,CO是一種無色、無味、有毒的氣體,難溶于水,與酸、堿、鹽溶液均不反應(yīng).已知乙二酸晶體加熱分解的方程式為:H2C2O4?2H2O
3H2O+CO2↑+CO↑,不考慮其他因素干擾,如何利用如圖所示裝置驗證反應(yīng)產(chǎn)物中含有CO2和CO(裝置不能重復(fù)使用).酒精噴燈可作高溫?zé)嵩矗埢卮鹣铝袉栴}:175℃△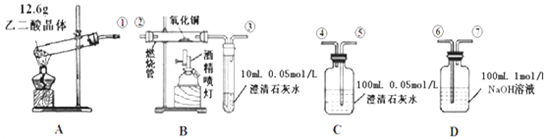
(1)檢驗裝置A氣密性的方法是.
(2)按氣流方向連接各儀器,用數(shù)字表示接口的連接順序:①→;
(3)證明CO存在的實驗現(xiàn)象是;
(4)本實驗尾氣處理的方法是;
(5)根據(jù)題給的數(shù)據(jù),假設(shè)反應(yīng)產(chǎn)生的氣體全部排出,并與吸收液充分反應(yīng)(提示:B、C中澄清石灰水均先變渾濁,后又變澄清),D中溶質(zhì)及對應(yīng)的物質(zhì)的量是.組卷:35引用:4難度:0.1 -
22.將一定質(zhì)量由Cu和CuO組成的固體粉末加入到100mL 11mol/L的濃HNO3中,充分反應(yīng)后,固體溶解完全,收集到NO、NO2混合氣體6.72L(標(biāo)準(zhǔn)狀況).若將該混合氣體與2.24L O2(標(biāo)準(zhǔn)狀況)混合并通入到足量水中,恰好生成HNO3.
(1)NO的體積是L,NO2的體積是L(標(biāo)準(zhǔn)狀況).
(2)固體粉末中Cu單質(zhì)的質(zhì)量是g.
(3)向濃HNO3反應(yīng)后的溶液中加入4mol/L的NaOH溶液,當(dāng)Cu2+恰好沉淀完時,需要NaOH溶液的體積是L.組卷:31引用:3難度:0.5


