2014-2015學年河北省保定市高陽中學高三(上)第六次周練化學試卷
發布:2024/12/17 4:0:2
一、選擇題(共10小題,每小題3分,滿分30分)
-
1.下列說法不正確的是( )
①將BaSO4放入水中不能導電,所以BaSO4是非電解質
②氨溶于水得到的氨水能導電,所以氨水是電解質
③固態共價化合物不導電,熔融態的共價化合物可以導電
④固態的離子化合物不導電,熔融態的離子化合物也不導電
⑤強電解質溶液的導電能力一定比弱電解質溶液的導電能力強.A.①④ B.①④⑤ C.①②③④ D.①②③④⑤ 組卷:425引用:52難度:0.9 -
2.下列反應所得溶液中一定只含一種溶質的是( )
A.向NaOH溶液中通入CO2 B.向Ca(OH)2溶液中通入Cl2 C.向蒸餾水中加入少量金屬Na D.向Al2(SO4)3溶液中滴入Ba(OH)2溶液 組卷:28引用:7難度:0.7 -
3.常溫下,某未知溶液中
=1×1012,且含有大量Al3+和c(H+)c(OH-),檢驗此溶液中是否大量存在以下6種離子:①NO-3、②SiO2-3、③Fe2+、④Na+、⑤NH+4、⑥Cl-,其中不必檢 驗就能加以否定的離子是( )HCO-3A.①③⑤ B.②③④ C.①②⑥ D.④⑤⑥ 組卷:93引用:22難度:0.7 -
4.類推是化學研究中常用的一種思維方式,下列有關離子反應方程式推理正確的是( )
已 知 推 理 A 向次氯酸鈣溶液中通CO2氣體:
Ca2++2ClO-+CO2+H2O═CaCO3↓+2HClO向次氯酸鈣溶液中通SO2氣體:
Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClOB 用惰性電極電解酸銅溶液:
2Cu2++2H2O2Cu+O2↑+4H+電解用銅電極電解硫酸銅溶液:
2Cu2++2H2O2Cu+O2↑+4H+電解C 稀硫酸與Ba(OH)2溶液反應,pH=7時,
2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O硫酸氫鈉溶液與Ba(OH)2溶液反應,pH=7時,
2H++SO42-+Ba2++2OH-═BaSO4↓+2H2OD Ba(OH)2溶液逐滴滴入硫酸鋁鉀溶液至沉淀質量達到最大值:
2Ba2++4OH-+Al3++2SO42-═2BaSO4↓+AlO2-+2H2OBa(OH)2溶液逐滴滴入硫酸鋁銨溶液至沉淀質量達到最大值:
2Ba2++4OH-+Al3++2SO42-═2BaSO4↓+AlO2-+2H2OA.A B.B C.C D.D 組卷:31引用:3難度:0.5
二、填空題(共4小題,每小題3分,滿分12分)
-
 13.1L某混合溶液,可能含有的離子如下表:
13.1L某混合溶液,可能含有的離子如下表:
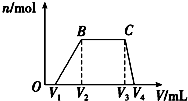
(1)往該溶液中逐滴加入NaOH產生沉淀的物質的量(n)與加入NaOH溶液的體積(V)的關系如圖所示.則該溶液中一定不含有的離子是可能大量含有的陽離子 H+、K+、Mg2+、Al3+、 、Fe2+、Fe3+NH+4可能大量含有的陰離子 Cl-、Br-、I-、 、CO2-3AlO-2.
(2)BC段離子方程式為.
(3)V1、V2、V3、V4之間的關系為.
(4)經檢測,該溶液中還含有大量的Cl-、Br-、I-,若向1L該混合溶液中通入一定量的Cl2,溶液中Cl-、Br-、I-的物質的量與通入Cl2的體積(標準狀況)的關系如下表所示,分析后回答下列問題
①當通入Cl2的體積為2.8L,溶液中發生反應的離子方程式為Cl2的體積(標準狀況) 2.8L 5.6L 11.2L n(Cl-) 1.25mol 1.5mol 2mol n(Br-) 1.5mol 1.4mol 0.9mol n(I-) a mol 0 0 .
②原溶液中Cl-、Br-、I-的物質的量濃度之比為.組卷:97引用:7難度:0.5 -
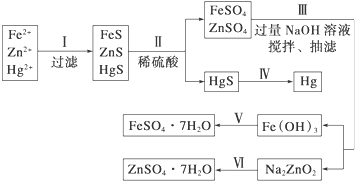 14.某工廠排出的污水中含有大量的Fe3+、Zn2+、Hg2+三種金屬離子.以下是某化學研究性學習小組的同學設計除去污水中的金屬離子,并回收綠礬、皓礬(ZnSO4?7H2O)和汞的方案.
14.某工廠排出的污水中含有大量的Fe3+、Zn2+、Hg2+三種金屬離子.以下是某化學研究性學習小組的同學設計除去污水中的金屬離子,并回收綠礬、皓礬(ZnSO4?7H2O)和汞的方案.
[藥品]NaOH溶液、硫化鈉溶液、硫化亞鐵、稀硫酸、鐵粉
[實驗方案]如圖
[問題探究]
(1)步驟Ⅱ所發生反應的離子方程.
(2)步驟Ⅲ中抽濾的目的是,該步驟產生Fe(OH)3的反應的離子方程式為.
(3)步驟Ⅵ中得到硫酸鋅溶液的離子方程式為.
(4)欲實現步驟Ⅴ,需加入的試劑有、,所涉及的主要操作依次為.
(5)步驟Ⅳ常用的方法是,該步驟是否對環境有影響?(填“是”或“否”),如有影響,請你設計一個綠色環保方案來實現步驟Ⅳ的反應:.
(6)該研究小組的同學在強堿溶液中,用次氯酸鈉與Fe(OH)3反應獲得了高效凈水劑Na2FeO4,該反應的離子方程式為.組卷:260引用:5難度:0.1


