2012年第二十二屆“天原杯”全國初中學(xué)生化學(xué)素質(zhì)和實(shí)驗(yàn)?zāi)芰Ω傎悘?fù)賽試卷
發(fā)布:2024/4/20 14:35:0
一、選擇題(本題包括15個(gè)小題,每小題2分,共30分.每小題有1個(gè)或2個(gè)選項(xiàng)符合題意.若有兩個(gè)答案的錯(cuò)1個(gè)不得分,漏選1各扣1分.請將答案填在下表相應(yīng)題號的空格內(nèi))
-
1.我國“化學(xué)”一詞最早出于《化學(xué)鑒原》(1871年)。書把一種元素翻譯為“矽(xi)”。在地殼里,“矽”的含量在所有元素含量中占第二位,現(xiàn)代把這種“矽”元素命名為( )
A.錫 B.硒 C.氧 D.硅 組卷:935引用:54難度:0.9 -
2.人們可從鐵鈦礦(主要成分FeTiO3)制取金屬鈦(Ti),其在一定條件下的主要反應(yīng)有:
①FeTiO3+H2=Fe+TiO2+H2O;
②TiO2+2C+2Cl2=TiCl4+2CO;
③TiCl4+2Mg=2MgCl2+Ti
下列敘述正確的是( )A.反應(yīng)①中的H2被氧化 B.反應(yīng)②中鈦元素的化合價(jià)升高 C.反應(yīng)③是復(fù)分解反應(yīng) D.反應(yīng)②Cl2中的“Cl”得到電子 組卷:515引用:10難度:0.9 -
3.正常人胃液的pH在0.3~1.2之間,酸(一般以鹽酸表示)多了,需要治療.某些用以治療胃酸過多的藥物中含MgCO3、NaHCO3,還有用酒石酸鈉來治療的.這主要是由于( )
A.碳酸、酒石酸都不是強(qiáng)酸 B.對人體而言酒石酸是營養(yǎng)品 C.Na+、Mg2+都是人體必需的元素 D.MgCO3、NaHCO3與胃酸作用生成CO2,在服藥后有喝汽水的舒服感 組卷:176引用:16難度:0.9 -
4.下列制取物質(zhì)的設(shè)計(jì)中,不可能實(shí)現(xiàn)的是( )
A.CaCO3 CaO高溫Ca(OH)2H2ONaOH溶液Na2CO3溶液過濾B.Cu CuOO2△CuSO4稀H2SO4Cu(OH)2沉淀NaOH溶液過濾C.KMnO4 O2△SO3S點(diǎn)燃H2SO4H2OD.Ba(OH)2 BaCl2溶液鹽酸BaCO3沉淀通入CO2組卷:115引用:8難度:0.5 -
5.兩個(gè)或多個(gè)同種含氧酸分子之間可以脫水形成相對分子質(zhì)量更大的酸,如磷酸H3PO4可形成H4P2O7或H5P3O10等。下列物質(zhì)不屬于硫酸(H2SO4)脫水后形成的是( )
A.H2S2O7 B.H2S3O10 C.H2S2O8 D.H2S4O13 組卷:588引用:23難度:0.5 -
6.“碳捕捉技術(shù)”是指通過一定的方法,將工業(yè)生產(chǎn)中產(chǎn)生的CO2分離出來進(jìn)行儲存和利用。常利用NaOH溶液來“捕捉”CO2,過程如圖所示(部分條件及物質(zhì)未標(biāo)出)。下列說法正確的是( )
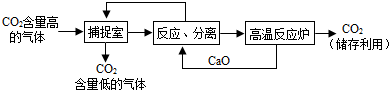
A.該方法的優(yōu)點(diǎn)是沒有能耗 B.該方法可減少碳排放 C.整個(gè)過程中,只有一種物質(zhì)可以循環(huán)利用 D.“反應(yīng)、分離”中,分離物質(zhì)的基本操作是蒸發(fā)、結(jié)晶 組卷:303引用:27難度:0.7 -
7.已知復(fù)分解反應(yīng)2CH3COOH+Na2CO3═2CH3COONa+H2O+CO2↑可進(jìn)行。在常溫下,測得相同濃度的下列六種溶液的pH:
表中數(shù)據(jù)揭示出復(fù)分解反應(yīng)的一條規(guī)律,即堿性較強(qiáng)的物質(zhì)發(fā)生類似反應(yīng)可以生成堿性弱的物質(zhì)。依照該規(guī)律,請你判斷下列反應(yīng)不能成立的是( )溶質(zhì) NaHCO3 CH3COONa NaClO NaCN Na2CO3 pH 8.6 8.8 10.3 11.1 11.6 A.CO2+H2O+2NaClO═Na2CO3+2HClO B.CO2+H2O+NaClO═NaHCO3+HClO C.CH3COOH+NaCN═CH3COONa+HCN D.NaClO+CH3COOH═HClO+CH3COONa 組卷:143引用:6難度:0.7 -
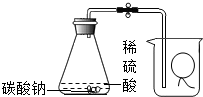 8.為測定氣球內(nèi)的氣體成分,有學(xué)生用超薄材料制成的氣球按如圖裝置進(jìn)行實(shí)驗(yàn)。開始時(shí)氣球沉于燒杯底部,打開開關(guān)后,過一會兒氣球從燒杯底部慢慢浮起,最后懸于燒杯口。氣球內(nèi)可能的氣體是( )
8.為測定氣球內(nèi)的氣體成分,有學(xué)生用超薄材料制成的氣球按如圖裝置進(jìn)行實(shí)驗(yàn)。開始時(shí)氣球沉于燒杯底部,打開開關(guān)后,過一會兒氣球從燒杯底部慢慢浮起,最后懸于燒杯口。氣球內(nèi)可能的氣體是( )A.甲烷 B.氧氣 C.二氧化硫 D.氫氣 組卷:166引用:8難度:0.9 -
9.在CuO和Fe的混合物中加入一定量的稀硫酸,微熱,待反應(yīng)停止后過濾,濾出不溶物后再往濾液里加入一枚鐵釘,若鐵釘無變化,則錯(cuò)誤的敘述是( )
A.不溶物中一定有銅 B.不溶物可能全部是鐵 C.濾液是硫酸亞鐵溶液 D.濾液是硫酸銅和硫酸亞鐵的混合溶液 組卷:134引用:9難度:0.9 -
10.某水溶液中含有以下離子中的若干種:K+、Cl-、Mg2+、Ba2+、SO42-、CO32-,現(xiàn)取兩份100mL溶液進(jìn)行如下實(shí)驗(yàn):
(1)第一份加入AgNO3溶液有沉淀產(chǎn)生.
(2)第二份加足量BaCl2溶液后,得沉淀物6.27g,經(jīng)足量硝酸洗滌、干燥后,沉淀質(zhì)量為2.33g,在所得濾液中加入AgNO3溶液有沉淀產(chǎn)生.
根據(jù)上述實(shí)驗(yàn),以下推測正確的是( )A.Cl-一定存在 B.100mL溶液中K+的質(zhì)量不小于2.34g C.K+一定存在 D.Ba2+一定不存在,Mg2+可能存在 組卷:269引用:5難度:0.5
四、計(jì)算題(本題包括2個(gè)小題,共10分)
-
30.有一瓶久藏的Na2SO3,欲測定該藥品變質(zhì)程度,進(jìn)行如下定量分析:將試樣烘干后稱取m g,用適量的蒸餾水配成溶液,加入足量的BaCl2溶液使沉淀完全.濾出的沉淀經(jīng)洗滌、干燥后,質(zhì)量為n g.
(1)若試樣部分變質(zhì),的范圍為nm.
(2)若取試樣m=10.0g,其中Na2SO3已有50%變質(zhì),則n為g.組卷:454引用:10難度:0.1
五、附加題:
-
 31.固體銨鹽A、B的成分可能是(NH4)2SO4、NH4HSO4或是兩者的混合物。甲、乙兩個(gè)研究性學(xué)習(xí)小組要確定A和B的成分,并測定B中氮元素的質(zhì)量分?jǐn)?shù)。
31.固體銨鹽A、B的成分可能是(NH4)2SO4、NH4HSO4或是兩者的混合物。甲、乙兩個(gè)研究性學(xué)習(xí)小組要確定A和B的成分,并測定B中氮元素的質(zhì)量分?jǐn)?shù)。
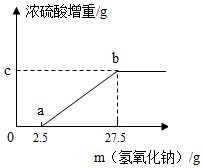
(1)甲實(shí)驗(yàn)小組的同學(xué)取了數(shù)份相同質(zhì)量的樣品A溶于水,然后加入40% NaOH溶液(圖中用氫氧化鈉質(zhì)量表示),水浴加熱至氣體全部逸出(此溫度下銨鹽不分解)。該氣體經(jīng)干燥后用足量濃硫酸完全吸收,濃硫酸增重的質(zhì)量如圖。分析該圖象并回答下列問題:
①寫出ab段涉及的化學(xué)方程式:。
②樣品A的成分是,c點(diǎn)的數(shù)值是。
(2)乙實(shí)驗(yàn)小組的同學(xué)取了數(shù)份不同質(zhì)量的樣品B,測定方法與甲組同學(xué)大部分相同,不同的是,他們將不同質(zhì)量的銨鹽分別加入到50.00mL NaOH溶液中(含8.12g NaOH),測定結(jié)果如下:
①分析實(shí)驗(yàn)數(shù)據(jù)可知,實(shí)驗(yàn)編號為實(shí)驗(yàn)編號 Ⅰ Ⅱ Ⅲ Ⅳ 銨鹽的質(zhì)量(g) 10.00 20.00 30.00 50.00 濃硫酸增加的質(zhì)量(g) m m 1.36 0 的實(shí)驗(yàn)中,氫氧化鈉足量,銨鹽中的銨根離子完全轉(zhuǎn)化成氣體。
②計(jì)算B中氮元素的質(zhì)量分?jǐn)?shù)。(保留兩位小數(shù))組卷:131引用:5難度:0.5


