2021-2022學年浙江省寧波市效實中學高一(下)期中化學試卷(學考)
發布:2024/4/20 14:35:0
一、選擇題(1~30每小題2分,31~35每小題2分,每小題只有一個選項符合題意。)
-
1.下列反應中,生成物總能量高于反應物總能量的是( )
A.NaOH溶液與稀鹽酸的反應 B.鎂與鹽酸反應 C.Ba(OH)2?8H2O與NH4Cl反應 D.鈉與水反應 組卷:10引用:3難度:0.8 -
2.下列烷烴具有同分異構現象的是( )
A.CH4 B.C2H6 C.C3H8 D.C4H10 組卷:14引用:2難度:0.5 -
3.下列關于原電池的說法中,正確的是( )
A.任何化學反應上都能設計成原電池 B.原電池工作時,陽離子向負極移動 C.原電池的負極發生氧化反應 D.原電池工作時,電子通過電解質溶液流向正極 組卷:58引用:5難度:0.6 -
4.在帶有活塞的密閉容器中發生如下反應:Fe2O3(s)+3H2(g)
2Fe(s)+3H2O(g),采取下列措施不能改變反應速率的是( )高溫A.將Fe2O3由塊狀粉碎成粉末狀 B.保持容器容積不變,增加H2通入量 C.保持容器內壓強不變,充入N2 D.保持容器容積不變,充入N2 組卷:40引用:2難度:0.7 -
5.下列各組反應(表中物質均為反應物)在反應剛開始時,放出H2的反應速率最大的是( )
選項 金屬(粉末狀)及其物質的量/mol 酸的濃度及體積 反應溫度/℃ A Mg 0.1 6mol?L-1鹽酸 10mL 30 B Zn 0.1 3mol?L-1鹽酸 10mL 60 C Fe 0.1 6mol?L-1鹽酸 10mL 30 D Mg 0.1 3mol?L-1硫酸 10mL 60 A.A B.B C.C D.D 組卷:25引用:4難度:0.8 -
6.某單液電池如圖所示,其反應原理為H2+2AgCl═2Ag+2HCl。下列說法正確的是( )

A.右側Pt電極為負極 B.左側電極上發生還原反應 C.溶液中H+向右側電極移動 D.右側電極的電極反應式為AgCl-e-═Ag+Cl- 組卷:37引用:3難度:0.7 -
7.反應4NH3(g)+5O2(g)?4NO(g)+6H2O(g),在不同情況下測得反應速率,反應最快的是( )
A.v(H2O)=0.24mol?L-1?s-1 B.v(O2)=12mol?L-1?min-1 C.v(NH3)=0.2mol?L-1?s-1 D.v(NO)=6mol?L-1?min-1 組卷:5引用:1難度:0.5 -
8.把A、B、C、D四種金屬浸在稀硫酸中,用導線兩兩相連可以組成各種原電池,若A、B相連時,陰離子移向A;C、D相連時,D上有氣泡逸出;A、C相連時,A極減輕;D插入B的鹽溶液中有B析出。則四種金屬的活潑性順序由大到小排列為( )
A.A>B>C>D B.A>C>B>D C.A>C>D>B D.B>D>C>A 組卷:92引用:4難度:0.6 -
9.如圖根據能量變化示意圖,下列說法正確的是( )

A.斷開1molHCl(g)中的H-Cl鍵需要吸收863.5kJ能量 B.反應H2(g)+Cl2(g)═2HCl(g),反應物的總能量小于生成物的總能量 C.H2(g)和Cl2(g)形成1molHCl(g)釋放184.4kJ的能量 D.2molHCl(g)分解成1molH2(g)和1molCl2(g)需要吸收184.4kJ熱量 組卷:23引用:3難度:0.7 -
10.在一定溫度下,一定體積的容器中,可逆反應:A(g)+3B(g)?2C(g)達到平衡的標志是( )
A.A、B、C的濃度相等 B.容器中壓強不再變化 C.單位時間消耗nmol A,同時生成2n mol C D.A、B、C的分子數比為1:3:2 組卷:32引用:4難度:0.9 -
11.下列裝置中,能構成原電池的是( )

A.只有甲 B.只有乙 C.只有丙 D.除乙之外均可以 組卷:103引用:13難度:0.7 -
12.一定溫度下,在固定體積的密閉容器中發生下列反應:2HI(g)?H2(g)+I2(g)。若c(HI)由0.1 mol?L-1降到0.08 mol?L-1時,需要20s,那么c(HI)由0.08mol?L-1降到0.07 mol?L-1時,所需反應的時間為( )
A.等于5s B.等于10s C.大于10s D.小于10s 組卷:203引用:9難度:0.5
二、解答題(共2小題,滿分20分)
-
36.下列物品或設施:
①光導纖維
②計算機芯片
③陶瓷餐具
④太陽能電池
(1)使用了硅單質的是:(填序號)。
(2)工業上用焦炭還原石英砂制粗硅,請寫出反應的化學方程式:。
(3)A~D是四種烴分子的球棍模型(如圖)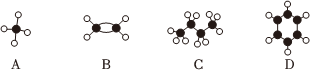
①與A互為同系物的是(填序號)。
②除去A中的B,可以用溴水,寫出相應的化學方程式:。
③C5H12的同分異構體數目為:。組卷:15引用:1難度:0.6 -
 37.某反應在體積為5L的恒容密閉的絕熱容器中進行,各物質的量隨時間的變化情況如圖所示(已知A、B、C均為氣體)。
37.某反應在體積為5L的恒容密閉的絕熱容器中進行,各物質的量隨時間的變化情況如圖所示(已知A、B、C均為氣體)。
(1)該反應的化學方程式為。
(2)反應開始至2分鐘時,B的平均反應速率為。
(3)能說明該反應已達到平衡狀態的是。
A.v(A)=2v(B)
B.容器內氣體密度不變
C.v逆(A)=v正(C)
D.各組分的物質的量相等
E.混合氣體的平均相對分子質量不再改變的狀態
(4)由圖求得平衡時A的轉化率為。
(5)在某一時刻采取下列措施能使該反應速率減小的是(填字號)。
A.加入正催化劑
B.降低溫度
C.恒溫恒容,充入O2
D.恒溫恒壓,充入He組卷:10引用:3難度:0.7


