2022-2023學年天津市西青區張家窩中學高二(上)期中化學試卷
發布:2024/9/29 1:0:1
一、選擇題(本題包括15.小題,每小題3分,共45分.每小題只有一個選項符合題意)
-
1.下列設備工作時,將化學能轉化為熱能的是( )
A. 
硅太陽能電池B. 
鋰離子電池C. 
太陽能集熱器D. 
燃氣灶組卷:359引用:45難度:0.9 -
2.下列說法正確的是( )
A.已知2H2(g)+O2(g)═2H2O(g)ΔH=-483.6kJ/mol,則氫氣的燃燒熱為241.8kJ/mol B.已知2C(s)+2O2(g)═2CO2(g)ΔH=akJ/mol,2C(s)+O2(g)═2CO(g)ΔH=bkJ/mol,則a>b C.可燃物的系數為1的燃燒反應的焓變即為該可燃物的燃燒熱 D.已知NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l) ΔH=-457.4kJ/mol,則含0.5mol NaOH的稀溶液與稀醋酸完全中和,放出的熱量小于228.7kJ 組卷:15引用:5難度:0.5 -
3.下列電離方程式書寫正確的是( )
A.H2O?H++OH- B.H2S?2H++S2- C.NaHCO3?Na++H++CO32- D.Fe(OH)3═Fe3++3OH- 組卷:33引用:5難度:0.9 -
4.一定溫度下,滿足下列條件的溶液一定呈堿性的是( )
A.能與金屬Al反應放出H2 B.pH=7.2 C.c(H+)<c(OH-) D.能使pH試紙呈紅色 組卷:19引用:4難度:0.9 -
5.高爐煉鐵產生的廢氣中的CO可進行回收,使其在一定條件下和H2反應制備甲醇:CO(g)+2H2(g)?CH3OH(g),若在溫度和容器相同的三個密閉容器中,按不同方式投入反應物,測得反應達到平衡時的有關數據如下表,則下列關系正確的是( )
容器 反應物投入的量 反應物的轉化率 CH3OH的濃度 能量變化(Q1、Q2、Q3均大于0) 甲 1molCO和2molH2 a1 c1 放出Q1KJ熱量 乙 1molCH3OH a2 c2 吸收Q2KJ熱量 丙 2molCO和4molH2 a3 c3 放出Q3KJ熱量 A.a1+a3=1 B.2Q1=Q3 C.c1=c2 D.2a1=a3 組卷:306引用:2難度:0.7 -
6.工業制硫酸的主要反映之一為2SO2(g)+O2(g)?2SO3(g),反應過程中能量變化如圖所示,下列說法錯誤的是( )
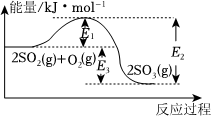
A.該反應的正反應為放熱反應 B.向反應體系中加入催化劑后,圖中E3不變 C.該反應的焓變ΔH=(E1-E2)kJ/mol D.升高溫度,E1變大 組卷:6引用:5難度:0.7
二、非選擇題(本題包括5小題,共55分)
-
19.某研究性學習小組用濃度為0.20mol?L-1的鹽酸標準液滴定含有一定量雜質的燒堿樣品(雜質與酸不反應)溶于水形成的溶液.
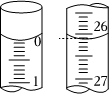
(1)準確量取一定體積的待測液需要使用的儀器是。
(2)若滴定開始和結束時,滴定管中的液面如圖所示,則消耗鹽酸標準液的體積為mL。
(3)用鹽酸標準液滴定待測燒堿樣品的溶液時,(填“左手”或“右手”,)握酸式滴定管的活塞,眼睛始終注視。
(4)滴定時,若以酚酞為指示劑,滴定達到終點的標志是。
(5)將準確稱取的5.0g燒堿樣品配制成250mL待測液,并用鹽酸標準液滴定.滴定前讀數及滴定后讀數如表所示。
由實驗數據可知,待測液的濃度為滴定次數 待測液體積(mL) 0.20mol/L的鹽酸體積(mL) 滴定前讀數 滴定后讀數 第一次 10.00 0.70 20.60 第二次 10.00 4.00 24.10 第三次 10.00 1.10 21.10 ;燒堿的純度為。
(6)下列操作會導致測得的待測液的濃度偏大的是(填標號)。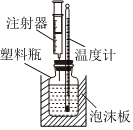
a.部分標準液滴出錐形瓶外
b.用待測溶液潤洗錐形瓶
c.錐形瓶洗凈后還留有蒸餾水組卷:5引用:1難度:0.5 -
20.如圖是某實驗小組改進的中和反應反應熱測定實驗裝置.在塑料瓶中事先加入50mL0.50mol?L-1鹽酸,然后通過注射器注入50mL0.55mol?L-1NaOH溶液,通過測定反應過程中所放出的熱量可計算反應熱.回答下列問題:
(1)塑料瓶外泡沫板的作用是。
(2)實驗小組按課本裝置和改進后的裝置分別進行實驗,測得實驗數據如下:
根據改進后裝置的實驗數據計算中和熱ΔH=實驗次數 起始溫度T1/℃ 終止溫度T2/℃ 溫度差(T2-T1)/℃ HCl NaOH 平均值 改進前 改進后 改進前 改進后 改進前 改進后 改進前 改進后 改進前 改進后 1 19.1 19.0 21.1 21.2 20.1 20.2 23.4 23.6 3.3 3.4 2 19.0 19.2 21.0 20.8 20.0 20.0 23.2 23.5 3.2 3.5 3 19.2 19.2 21.2 21.0 20.2 21.0 23.6 23.4 3.4 3.3 (計算結果保留兩位小數,近似認為鹽酸和NaOH溶液的密度都是1g?cm-3,中和后溶液的比熱容c=4.18j?g-1?℃-1)。
(3)如果用60mL0.50mol?L-1鹽酸與60mL0.55mol?L-1NaOH溶液進行反應,與上述實驗相比,所放出的熱量(填“相等”或“不相等”)。組卷:2引用:1難度:0.7


