2023年重慶市南開中學高考化學質檢試卷(八)
發布:2024/4/20 14:35:0
一、選擇題:本題共14小題,每小題3分,共42分。在每小題給出的四個選項中,只有一項是符合題目要
-
1.人類的健康離不開糖類、蛋白質、脂類等營養物質。下列有關說法正確的是( )
A.糖類也被稱為碳水化合物,所有糖類的化學組成均滿足Cn(H2O)m的通式 B.牛胰島素徹底水解的產物是純凈物 C.可以通過牛油的氫化生產人造奶油 D.食用蔬菜和水果可以為人體補充維生素 組卷:45引用:1難度:0.8 -
2.下列表示正確的是( )
A.乙烯的電子式: 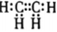
B.CH2Cl2的空間充填模型: 
C.果糖的結構簡式:HOCH2(CHOH)4CHO D.Fe2+的價電子排布式:[Ar]3d6 組卷:11引用:1難度:0.7 -
3.重慶大學潘復生院士在鎂合金技術研究領域做出巨大貢獻。下列說法正確的是( )
A.1個基態鎂原子中有2個未成對單電子 B.海水中含有豐富的鎂元素 C.鎂合金具有密度大、強度高的優點 D.工業上用H2在高溫下還原MgO制備Mg 組卷:8引用:1難度:0.7 -
4.經過下列操作后溶液呈堿性的是( )
A.通入少量SO2的NaHSO3溶液 B.通入足量NH3的AlCl3溶液 C.加入少量Fe的FeCl3溶液 D.加入足量P4O10的NaOH溶液 組卷:22引用:1難度:0.6 -
5.下列變化對應的離子方程式正確的是( )
A.MgO溶于NaHSO4溶液:3MgO+6H++3 ═3MgSO4↓+3H2OSO2-4B.向CuSO4溶液中通入H2S產生沉淀:Cu2++S2-═CuS↓ C.暴露在空氣中的NaOH溶液變質:CO2+2OH-═ +H2OCO2-3D.濃硝酸分解:4H++ ═2H2O+4NO2↑NO-3組卷:34引用:1難度:0.7 -
6.NA是阿伏加德羅常數的值。下列關于反應“S8+NaOH→Na2S+Na2SO3+H2O”(未配平)的說法不正確的是( )
A.1molS8參與反應,斷裂8NA個S-S鍵 B.生成1molNa2S,轉移2NA個電子 C.1LpH=12的NaOH溶液中有0.01NA個Na+ D.6.3gNa2SO3中有0.15NA個σ鍵 組卷:98引用:4難度:0.8
二、非選擇題:共58分。
-
17.綠色能源的開發利用是未來能源發展的重要方向,也是實現“碳中和”目標的重要舉措。CH4與CO2催化重整是實現碳中和的熱點研究課題。1991年,Ashcroft提出了甲烷二氧化碳重整的技術理論:氣體分子吸附至催化劑表面后發生反應。500℃時,反應原理如下:
反應Ⅰ.主反應:CH4(g)+CO2(g)?2CO(g)+2H2(g)ΔH1Kp1
反應Ⅱ.副反應:CO2(g)+H2(g)?CO(g)+H2O(g)ΔH2=+41.0kJ?mol-1
反應Ⅲ.積碳反應:2CO(g)?CO2(g)+C(s)
反應Ⅳ.積碳反應:CH4(g)?C(s)+2H2(g)
其中,副反應Ⅲ、Ⅳ形成的積碳易導致催化劑失去活性。
(1)在原料氣中添加微量O2有利于保持催化劑的活性,其原因是。
(2)ΔfHmθ為標準摩爾生成焓,其定義為標準狀態下,由穩定相態的單質生成1mol該物質的焓變.對于穩定相態單質,其ΔfHmθ為零。根據上述信息及下表所給數據,計算反應Ⅰ的反應熱ΔH1=。
(3)在恒溫恒容密閉容器中,通入一定量的CH4、CO2發生催化重整反應(假定只發生主反應1.當投料比物質 CH4 CO2 CO ΔfHmθ(kJ?mol-1) -74.8 -393.5 -110.5 =1.0時,CO2的平衡轉化率(α)與溫度(T)、初始壓強(p)的關系如圖所示。由圖可知:壓強p1n(Cl4)n(CO2)2MPa(填“>”、“<”或“=”);當溫度為T3、初始壓強為2MPa時,a點的v正v逆(填“>”、“<”或“=”)。起始時向1L恒容容器中加入2mol CH4和2mol CO2,在溫度為T0、初始壓強為2MPa條件下反應,用壓強表示該反應的平衡常數:Kp=(分壓=總壓×物質的量分數)。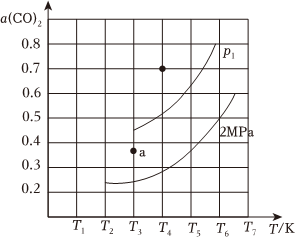
(4)用電化學方法還原CO2將其轉化為其它化學產品可以實現對CO2的綜合利用。如圖是在酸性條件下電化學還原CO2的裝置示意圖: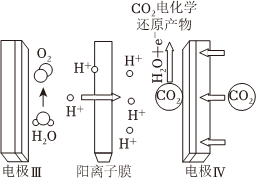
已知:法拉第效率(FE)的定義:FE(B)=×100%。控制pH=1、電解液中存在KCl時,電化學還原CO2過程中CH4(其他含碳產物未標出)和H2的法拉第效率變化如圖所示。n(生成B所用的電子)n(通過附極的電子)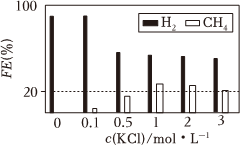
①寫出陰極產生CH4的電極反應:。
②結合上圖的變化規律,推測KCl可能的作用是。
③c(KCl)=3mol/L時,22.4L(已折合為標準狀況,下同)的CO2被完全吸收并還原為CH4和C2H4,分離H2后,將CH4和C2H4混合氣體通入如圖所示裝置(反應完全),出口處收集到氣體8.96L(不考慮水蒸氣),則FE(C2H4)=。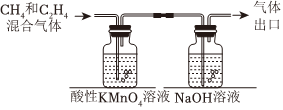 組卷:31引用:1難度:0.6
組卷:31引用:1難度:0.6 -
18.聚合物F的合成線路如圖所示:
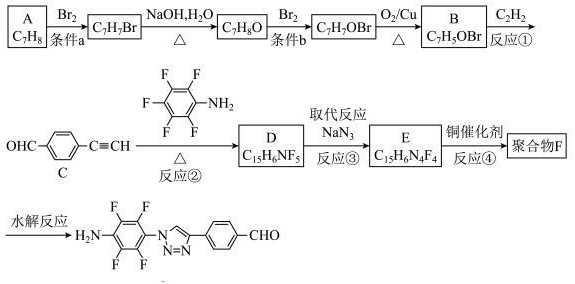
已知:(1)
(2)
(1)條件a為;反應①的反應類型是。
(2)關于B和C,下列說法正確的是(填字母)。
a.B可以發生氧化、取代、加成反應
b.利用質譜法可以鑒別B和C
c.可用Br2的CCl4溶液檢驗C中含有碳碳三鍵
(3)反應②的化學方程式為。
(4)化合物E的結構簡式為。
(5)H是C的同系物,H的相對分子質量比C大14,則H有種可能的結構(不考慮立體異構)。
(6)X與Y經以下兩種途徑均可獲得M。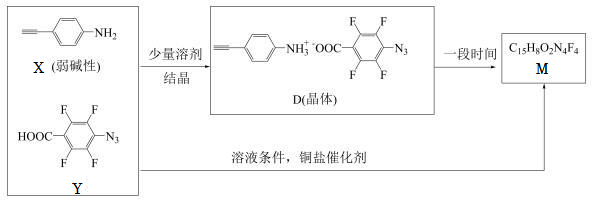
①M的結構簡式為。
②將Y更換為Y′(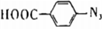 ),發現X與Y′無法形成晶體,證實了形成晶體時Y中苯環上氟原子的必要性。猜測氟原子可能的作用:影響晶體中分子的堆積方式、增強了-N3的活性和 。組卷:16引用:1難度:0.4
),發現X與Y′無法形成晶體,證實了形成晶體時Y中苯環上氟原子的必要性。猜測氟原子可能的作用:影響晶體中分子的堆積方式、增強了-N3的活性和 。組卷:16引用:1難度:0.4


