2020-2021學年遼寧省協作校高一(下)第一次月考化學試卷
發布:2024/4/20 14:35:0
一、選擇題(本題包括16小題,每小題3分,共48分。每小題只有一個選項符合題意)
-
1.化學與社會生活、科技有著密切的關系,下列說法正確的是( )
A.大理石雕像被酸雨腐蝕毀壞的過程中發生了氧化還原反應 B.包裝袋中裝有少量鐵屑作為食品的干燥劑 C.可使用含氯的殺菌消毒劑對生產和生活環境進行消毒 D.鋁合金硬度大、質量輕,工業上可用于制造盛放NaOH溶液的容器 組卷:12引用:2難度:0.5 -
2.硅及其化合物與科學、技術,社會,環境密切相關。下列有關說法不正確的是( )
A.單質硅是將太陽能轉變為電能的常用材料 B.硅主要以單質形式存在于自然界中 C.水晶、石英、瑪瑙等的主要成分是SiO2而不是硅酸鹽 D.傳統無機非金屬材料陶瓷、水泥、玻璃的主要成分是硅酸鹽 組卷:72引用:4難度:0.6 -
3.下列各裝置(電解質溶液都為稀硫酸)中,不能構成原電池的是( )




A B C D A.A B.B C.C D.D 組卷:17引用:2難度:0.6 -
4.下列物質分類組合正確的是( )
選項 酸 堿 鹽 酸性氧化物 電解質 A HNO3 Na2CO3 CaCO3 CO2 BaSO4 B H2SO4 NH3?H2O NH4Cl SO2 Cu C CH3COOH NaOH CaCl2 CO Na2SO3 D HCl KOH NaHCO3 SO3 NaCl A.A B.B C.C D.D 組卷:67引用:1難度:0.6 -
5.某化學反應在催化劑條件下的轉化過程的微觀示意圖如圖所示。下列有關說法不正確的是( )
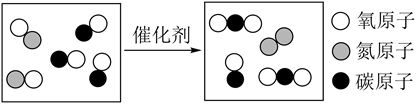
A.該反應中,氧化性:NO>CO2 B.該反應可表示為2NO+2CO N2+2CO2催化劑C.該反應中,被氧化與被還原的元素的質量之比為7:6 D.每生成標準狀況下2.24LN2,轉移的電子數為0.4NA 組卷:23引用:4難度:0.7 -
6.在5 L的恒容密閉容器中進行反應4NH3(g)+6NO(g)═5N2(g)+6H2O(g),2min后,NH3減少了0.4mol,則該反應的化學反應速率表示正確的是( )
A.v(NH3)=0.004mol?L-1?min-1 B.v(H2O)=0.001mol?L-1?s-1 C.v(NO)=0.006mol?L-1?s-1 D.v(N2)=0.005mol?L-1?min-1 組卷:16引用:1難度:0.8
二、非選擇題(本題包括4小題,共52分)
-
19.某小組為探究在適當溫度和催化劑的條件下,SO2與O2反應后的混合氣體的成分,設計了以下實驗。已知SO3的熔點是16.8℃,沸點是44.8℃。

(1)裝置A中反應的化學方程式為。
(2)導管a的用途是。
(3)裝置B中濃H2SO4的作用是。
(4)實驗中為使SO2有較高的轉化率,在加熱催化劑與滴加濃硫酸的順序中,應采取的操作是。
(5)實驗中發現SO2氣體產生緩慢,以致后續實驗現象不明顯,但又不存在氣密性問題,分析可能的原因為、。
(6)用a mol Na2SO3粉末與足量濃硫酸進行此實驗,當反應結束時,繼續通入O2一段時間,測得裝置C中收集到的晶體b g,則實驗中SO2的轉化率為。(用含a、b的代數式表示)組卷:30引用:2難度:0.7 -
20.將CO2轉化成有機物可有效實現碳循環.在容積為2L的恒溫恒容密閉容器中,充入1mol CO2和3mol H2,一定條件下發生反應CO2(g)+3H2(g)?CH3OH(g)+H2O(g),測得CO2和CH3OH(g)的物質的量隨時間的變化情況如下表。
(1)a=時間 0min 3min 6min 9min 12min n(CH3OH)/mol 0 0.50 0.65 0.74 0.74 n(CO2)/mol 1 0.50 0.35 a 0.26 ;3~9min內,v(CO2)=mol?L-1?min-1。
(2)能說明上述反應達到平衡狀態的是。(填標號)
A.反應中CO2與CH3OH的物質的量濃度之比為1:1
B.混合氣體的壓強不隨時間的變化而變化
C.單位時間內生成1mol H2,同時生成1mol CH3OH
D.混合氣體的平均相對分子質量不隨時間的變化而變化
(3)上述反應6min末時,已消耗掉的CO2的物質的量分數為。
(4)上述反應12min末時,混合氣體中CO2(g)和H2(g)的質量之比是。
(5)第3min時v正(CH3OH)(填“>”、“<”、“=”或“無法比較”)第9min時v逆(CH3OH).
(6)在恒溫條件下,若將一定量X和Y的混合氣體通入容積為2L的恒容密閉容器中,發生反應mX(g)?nY(g),X和Y的物質的量濃度隨時間的變化情況如下表。
①m:n=時間/min 0 5 10 15 20 c(X)/mol?L-1 0.2 c 0.6 0.6 0.6 c(Y)/mol?L-1 0.6 c 0.4 0.4 0.4 。
②c=。(保留兩位有效數字)組卷:25引用:4難度:0.5


