2021-2022學年黑龍江省哈爾濱六中高一(上)期中化學試卷
發布:2024/12/5 11:0:1
一、單選題(每題2分,共40分)
-
1.化學與生活是緊密相聯的,下列說法中不正確的是( )
A.用過氧化鈉作潛水艇的供氧劑 B.將少量食醋加入“84”消毒液中,會增強其殺菌消毒效果 C.小蘇打(NaHCO3)用于制作糕點 D.地震災區和洪澇災區都用漂白粉消毒,主要是利用漂白粉溶液的堿性 組卷:5引用:4難度:0.7 -
2.在堿性溶液中能大量共存且溶液為無色透明的離子組是( )
A.K+、 、Na+、Cl-MnO-4B.Na+、H+、 、NO-3SO2-4C.Fe3+、Na+、Cl-、 SO2-4D.K+、Na+、 、NO-3CO2-3組卷:73引用:159難度:0.9 -
3.下列實驗結論與實驗操作、現象對應正確的是( )
選項 實驗操作及現象 實驗結論 A 向某溶液中加入稀鹽酸,并將產生的氣體通入澄清石灰水中,澄清石灰水變渾濁 該溶液中一定含有CO32- B 將某白色固體置于試管中加熱,并將產生的氣體通入澄清石灰水中,澄清石灰水變渾濁 該固體中一定含有NaHCO3 C 向某無色溶液中,先加入適量稀硝酸酸化,無沉淀生成,再加入硝酸銀溶液,產生白色沉淀 該溶液中一定含有Cl- D 向某溶液中滴加酚酞,溶液呈紅色 該溶液可能是Na2CO3溶液 A.A B.B C.C D.D 組卷:20引用:4難度:0.5 -
4.小蘇打(NaHCO3)是一種抗酸藥,可以緩解胃酸過多,其與胃酸發生反應:HCl+NaHCO3=NaCl+CO2↑+H2O,該反應所屬反應類型是( )
A.化合反應 B.氧化還原反應 C.分解反應 D.復分解反應 組卷:34引用:6難度:0.6 -
5.某同學用以下裝置制備并檢驗Cl2的性質。下列說法正確的是( )
A. 
圖:若MnO2過量,則濃鹽酸可全部消耗完B. 
圖:證明新制氯水具有酸性C. 
圖:產生了棕黃色的霧D. 
圖:濕潤的有色布條褪色組卷:276引用:12難度:0.5 -
 6.某離子反應涉及到H2O、ClO-、、OH-、N2、Cl-等微粒,其中N2、ClO-的物質的量隨時間變化的曲線如圖所示,下列說法正確的是( )NH+4
6.某離子反應涉及到H2O、ClO-、、OH-、N2、Cl-等微粒,其中N2、ClO-的物質的量隨時間變化的曲線如圖所示,下列說法正確的是( )NH+4A.該反應中Cl-為氧化產物 B.消耗1 mol還原劑,轉移6 mol電子 C.反應后溶液的酸性減弱 D. 被ClO-氧化成N2NH+4組卷:262引用:8難度:0.9 -
7.下列敘述中,正確的是( )
A.等質量的CO與CO2中所含碳原子數之比為7:11 B.標準狀況下,若某氧氣和氮氣的混合氣體mg含有b個分子,則ng該混合氣體在標準狀況下的體積為 22.4nNAmbC.用膽礬配制950mL 0.2mol?L-1的硫酸銅溶液,需稱取膽礬的質量為50.0g D.98g H2SO4溶解于500mL水,所得溶液中硫酸的物質的量濃度為2mol?L-1 組卷:11引用:2難度:0.6 -
8.用如圖所示實驗裝置進行相關實驗探究,其中裝置不合理的是( )
A. 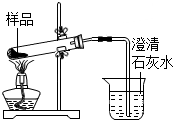
鑒別純堿與小蘇打B. 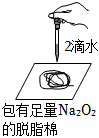
證明Na2O2與水反應放熱C. 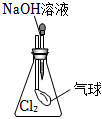
證明Cl2能與燒堿溶液反應D. 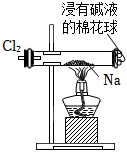
探究鈉與Cl2反應組卷:232引用:38難度:0.6 -
9.下列說法正確的是( )
A.摩爾是物質的數量單位,CO2的摩爾質量為44 B.16g O2的物質的量為0.5mol C.將0.1mol HCl通入1L水中所得鹽酸的濃度為0.1mol/L D.相同溫度和壓強下,等體積的NO和NO2具有相同的質量 組卷:84引用:3難度:0.8 -
10.Na2O2和Na2O是金屬鈉的兩種氧化物,下列有關說法正確的是( )
A.Na2O2和Na2O均能與水反應,且產物相同 B.Na2O2和Na2O均能使酚酞溶液先變紅后褪色 C.等物質的量的Na2O2和Na2O中,鈉離子數目之比為2:1 D.將等質量的Na2O2和Na2O均與足量水反應,產物NaOH的物質的量之比為31:39 組卷:13引用:4難度:0.6
三、非選擇題(本題型四道大題共50分)
-
30.在抗擊新冠肺炎疫情的戰役中,病毒在不斷發生變異,現有疫苗對變異病毒的有效性有待進一步的驗證,因此民眾的防疫意識不能松懈。
(1)口罩作為基礎防疫物資,可以有效防止飛沫的傳播。最新的研究表明新冠病毒可能通過氣溶膠傳播,氣溶膠屬于(填“膠體”或“溶液”);常利用區分溶液和膠體。
(2)為有效防止新冠病毒的傳播,除了戴口罩,還需加強對隔離場所的消毒。常用的消毒劑有雙氧水、醫用酒精以及含氯消毒劑,其中含氯消毒劑的家族最龐大、應用最廣泛。實驗室制Cl2有四種常用方法:
a.MnO2+4HCl(濃)MnCl2+Cl2↑+2H2O△
b.2KMnO4+16HCl(濃)→2KCl+2MnCl2+5Cl2↑+8H2O
c.KClO3+HCl(濃)→KCl+Cl2↑+H2O(未配平)
d.K2Cr2O7+14 HCl(濃)=2KCl+2CrCl3+3Cl2+7H2O
①反應c未配平,請寫出配平后的化學方程式,并用雙線橋法標出電子轉移數目。。
②寫出反應b對應的離子方程式。
③當a、b、c三個反應中,得到等質量的Cl2時,電子轉移數目最少的是反應。
(3)已知反應4HCl+O22Cl2+2H2O(g),該反應也能制得氯氣。提醒一下,反應條件越簡單反應越容易發生,說明性質越強烈。則MnO2、O2、KMnO4三種物質氧化性由強到弱的順序為催化劑△。組卷:12引用:1難度:0.7 -
31.我國化學家侯德榜發明了聯合制堿法,為世界制堿工業做出了巨大貢獻。聯合制堿法的主要過程如圖所示(部分物質已略去)。

(1)①~③所涉及的操作方法中,包含過濾的是(填序號)。
(2)根據上圖,將化學方程式補充完整:NH3+CO2++=NaHCO3↓+NH4Cl。
(3)下列說法中,正確的是(填字母)。
A.碳酸氫鈉分解產生的CO2可回收并循環使用
B.NH4Cl副產物可用作氮肥
C.溶液B中一定含有Na+、NH4+、Cl-
D.飽和氯化鈉溶液中應該先通二氧化碳再通入氨氣
(4)某種市售食用堿是純堿與小蘇打的混合物,可大量應用于食品加工,如:面條、面包、饅頭等,某校化學興趣小組利用如圖所示裝置進行實驗測定此種食用堿中純堿的質量分數。
實驗步驟:
①檢查裝置的氣密性,稱取樣品(僅由純堿與小蘇打組成)10g,加到裝置B中;
②連接裝置,打開彈簧夾,先通一段時間空氣后,關閉彈簧夾,打開分液漏斗活塞滴入稀硫酸至不再有氣體生成;
③關閉分液漏斗的活塞,打開彈簧夾,繼續通入一段時間空氣。實驗中記錄的數據如表所示:
請回答下列問題:裝置B 裝置C 干燥管1 實驗前稱得的質量/g 180.0 30.0 120.4 實驗后稱得的質量/g 174.2 31.5 124.8
①裝置a的儀器名稱是。
②試劑X為NaOH溶液,實驗開始前,先打開彈簧夾,通入一段時間空氣,其目的為,實驗結束后,需要繼續通入一段時間的空氣,其目的是將裝置內的CO2趕到干燥管中被吸收。
③干燥管II的作用是。
④有同學認為,表格中三組數據都可以計算該樣品中Na2CO3的質量分數,但也有同學認為不能用裝置C前后的質量差來計算,其理由是吸收的水蒸氣并不全部來自反應生成;通過實驗數據計算,食用堿中Na2CO3的質量分數為(保留三位有效數字)。組卷:11引用:2難度:0.6


